Tiempo de lectura estimado: 5 minutos
El balón de Morton o matrás Morton fue desarrollado por el químico americano Avery Arthur Morton en el marco de sus estudios en química organometálica, en especial sobre la química de compuestos órganosódicos
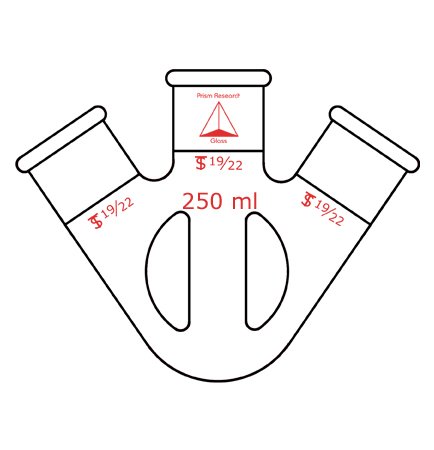
Un balón de Morton o estilo Morton es un balón o matraz de fondo redondo, de tres cuellos de pared gruesa con juntas exteriores cónicas estándar en el centro y cuellos laterales en ángulo de 20º. Las hendiduras aumentan la agitación del contenido del frasco durante la agitación.
Existen desafíos detrás de reproducir una reacción está lleno de peligros: la tasa de adición, la eficiencia de la mezcla, la temperatura, el vacío… todo puede marcar la diferencia. Y eso es antes de que nos atrevamos a cambiar la escala.
Pero nos guste o no, se deben resolver estos desafíos, y no puede haber una solución más fina que la del frasco de Morton, que abrió el mundo de la química organosódica.
El inventor de la solución, Avery Morton
Avery Arthur Morton nació en St. Lawrence, Dakota del Sur, EE.UU., en 1892, pero se trasladó a Betania, en las afueras de Lincoln, Nebraska, cuando era un niño pequeño. Poco se sabe de su infancia, pero estudió química en el Cotner College, una escuela confesional del vecindario. Continuó sus estudios de postgrado, primero en la Universidad de Chicago y luego en Harvard. Sin embargo, sus estudios se interrumpieron en 1919 cuando fue reclutado por los Marines y se sometió a un entrenamiento básico en la famosa base de Parris Island en Carolina del Sur.
Luego fue enviado a la República Dominicana que, junto con Haití, los EE.UU. habían invadido en 1914 con el pretexto de proteger el Canal de Panamá de la Alemania Imperial. En 1920, cuando Morton habría llegado, varios valientes periodistas habían empezado a informar sobre la brutalidad de la ocupación. Aunque se introdujeron importantes reformas, no puede haber sido un anuncio feliz.
Tan pronto como fue dado de alta en 1924, volvió al laboratorio, esta vez en el Instituto Tecnológico de Massachusetts (MIT) en Boston, donde hizo un doctorado en química orgánica física con James Norris. Su talento era tal que le ofrecieron un puesto de trabajo tan pronto como se graduó. Una persona rápida y nerviosa, jugó un juego de squash muy malo, luchando por la supremacía en la liga del MIT con otra estrella en ascenso, el ingeniero eléctrico Vannevar Bush.
Química organometálica y el balón de Morton
Morton se sintió atraído por las intrigantes posibilidades que ofrecía la química organometálica. Se pensaba que el acoplamiento de Wurtz – por el cual los haluros de alquilo pueden ser dimerizados o cruzados para hacer alcanos más altos, y su variante aromática, la reacción de Wurtz-Fittig, procedían a través de intermediarios organosódicos evasivos.
En 1936, uno de los padres de la química organometálica, Karl Ziegler, escribió con desesperación que los organosodios no se podían fabricar a partir de los halogenuros de alquilo. Ese mismo año, Morton publicó una obra que demostraba no sólo que los organosódicos podían prepararse en alto rendimiento, sino que también exponía con elegancia los requisitos cruciales para una preparación satisfactoria. En primer lugar, hay que evitar los éteres que serían atacados por el producto espectacularmente reactivo. En segundo lugar, la capacidad de dispersar finamente el sodio y de exponer rápidamente su superficie al haluro de alquilo entrante era fundamental.
Con este fin, Morton encontró dos soluciones. Empezó a usar agitadores de velocidad ultra alta capaces de hacer girar las mezclas heterogéneas hasta 10.000 rpm. En segundo lugar, modificó sus frascos para incluir varios pliegues cónicos profundos en los lados, cuya función era maximizar la turbulencia y el cizallamiento de la mezcla arremolinada. Comprobó la eficacia de la mezcla utilizando mezclas de arena y agua, observando la distribución uniforme de las partículas.
El cambio en la forma del frasco tuvo un impacto mágico en la dinámica del sistema y, en cuestión de segundos, pudieron obtener sodio de una textura parecida al azúcar molido más fino. Usando los frascos, Morton y sus estudiantes fueron capaces de obtener rendimientos cuantitativos de organosodios en minutos.
Aunque el grupo de Morton adquirió cierta notoriedad por sus incendios, eran experimentadores notables. Como resultado, Morton dirigió el curso avanzado de laboratorio orgánico sintético del MIT durante muchos años, a menudo ideando experimentos para estirar a los mejores estudiantes. A finales de los años 30 publicó un libro de texto «Técnicas de Laboratorio en Química Orgánica» que todavía se cita hoy en día.
Para más información Classic Kit: Morton flask
Como citar este artículo:
APA: (). Balón de Morton. Recuperado de https://quimicafacil.net/infografias/material-de-laboratorio/balon-de-morton/
ACS: . Balón de Morton. https://quimicafacil.net/infografias/material-de-laboratorio/balon-de-morton/. Fecha de consulta 2026-04-05.
IEEE: , "Balón de Morton," https://quimicafacil.net/infografias/material-de-laboratorio/balon-de-morton/, fecha de consulta 2026-04-05.
Vancouver: . Balón de Morton. [Internet]. [citado 2026-04-05]. Disponible en: https://quimicafacil.net/infografias/material-de-laboratorio/balon-de-morton/.
MLA: . "Balón de Morton." https://quimicafacil.net/infografias/material-de-laboratorio/balon-de-morton/. . Web.
Si tiene alguna pregunta o sugerencia, escribe a administracion@quimicafacil.net, o visita Como citar quimicafacil.net