Dmitri Ivanovich Mendeleev
Estimated reading time: 17 minutos
Dmitri Ivanovich Mendeleev (a menudo romanizado como Mendeleyev o Mendeleef) 8 de febrero de 1834 – 2 de febrero de 1907 [Calendario Gregoriano 27 de enero de 1834 – 20 de enero de 1907]) fue un químico e inventor ruso. Se le recuerda más por haber formulado la Ley Periódica y haber creado una versión previsora de la tabla periódica de elementos. Utilizó la Ley Periódica no sólo para corregir las propiedades entonces aceptadas de algunos elementos conocidos, como la valencia y el peso atómico del uranio, sino también para predecir las propiedades de ocho elementos que aún no habían sido descubiertos.

Biografía
Mendeleev nació en la aldea de Verkhnie Aremzyani, cerca de Tobolsk en Siberia, hijo de Iván Pavlovich Mendeleev (1783-1847) y Maria Dmitrievna Mendeleeva (de soltera Kornilieva) (1793-1850) Iván trabajó como director de escuela y profesor de bellas artes, política y filosofía en los gimnasios de Tambov y Saratov. El padre de Iván, Pavel Maximovich Sokolov, era un sacerdote ortodoxo ruso de la región de Tver. Según la tradición de los sacerdotes de la época, a los hijos de Pavel se les daban nuevos apellidos mientras asistían al seminario teológico, y a Iván se le dio el apellido Mendeleev en honor al nombre de un terrateniente local.
Maria Kornilieva procedía de una conocida familia de comerciantes de Tobolsk, fundadores de la primera imprenta siberiana que remontaba su ascendencia a Yakov Korniliev, un posadero del siglo XVII convertido en un rico comerciante. En 1889, un bibliotecario local publicó un artículo en el periódico de Tobolsk en el que afirmaba que Yakov era un Teleut bautizado, una minoría étnica conocida como «kalmyks blancos» en aquella época. Como no se proporcionaron fuentes ni se revelaron hechos documentados de la vida de Yakov, los biógrafos generalmente lo descartan como un mito.
En 1908, poco después de la muerte de Mendeleev, una de sus sobrinas publicó Family Chronicles. Recuerdos sobre D. I. Mendeleev, en las que expresaba «una leyenda familiar» sobre el abuelo de María que se casó con «una belleza kirguisa o tártara a la que quería tanto que cuando ella murió, él también murió de pena». Sin embargo, esto contradice las crónicas familiares documentadas, y ninguna de esas leyendas está respaldada por la autobiografía de Mendeleev ni por las memorias de su hija o su esposa. Sin embargo, algunos estudiosos occidentales siguen refiriéndose a la supuesta ascendencia «mongola», «tártara», «tártara» o simplemente «asiática» de Mendeleev como un hecho.
Dmitri Mendeleev fue criado como un cristiano ortodoxo, su madre lo animó a «buscar pacientemente la verdad divina y científica«. Su hijo le informaría más tarde que se alejó de la Iglesia y abrazó una forma de «deísmo romántico»
Mendeleev era el menor de 17 hermanos, de los cuales «sólo 14 permanecieron vivos para ser bautizados» según el hermano de Mendeleev, Pavel, lo que significa que los demás murieron poco después de su nacimiento. El número exacto de hermanos de Mendeleev difiere entre las fuentes y sigue siendo objeto de alguna disputa histórica. Lamentablemente para el bienestar financiero de la familia, su padre quedó ciego y perdió su puesto de profesor. Su madre se vio obligada a trabajar y reinició la fábrica de vidrio abandonada de su familia. A la edad de 13 años, tras el fallecimiento de su padre y la destrucción de la fábrica de su madre por un incendio, Mendeleev asistió al Gimnasio de Tobolsk.
En 1849, su madre llevó a Mendeleev a través de Rusia desde Siberia a Moscú con el objetivo de que se matriculara en la Universidad de Moscú. La universidad de Moscú no lo aceptó. La madre y el hijo continuaron en San Petersburgo hasta el alma mater del padre. La ahora pobre familia Mendeleev se trasladó a San Petersburgo, donde entró en el Instituto Pedagógico Principal en 1850. Después de graduarse, contrajo tuberculosis, por lo que se trasladó a la península de Crimea en la costa norte del Mar Negro en 1855. Mientras estaba allí, se convirtió en un maestro de ciencias del 1er Gimnasio de Simferopol. En 1857, regresó a San Petersburgo con la salud completamente restaurada.

Entre 1859 y 1861, trabajó en la capilaridad de los líquidos y en el funcionamiento del espectroscopio en Heidelberg. Más tarde, en 1861, publicó un libro de texto llamado Química Orgánica. Esto le valió el Premio Demidov de la Academia de Ciencias de San Petersburgo.
El 4 de abril de 1862 se comprometió con Feozva Nikitichna Leshcheva, y se casaron el 27 de abril de 1862 en la iglesia del Instituto de Ingeniería Nikolaev en San Petersburgo (donde enseñaba).
Mendeleev se convirtió en profesor del Instituto Tecnológico de San Petersburgo y de la Universidad Estatal de San Petersburgo en 1864 y 1865, respectivamente. En 1865, se convirtió en Doctor en Ciencias por su disertación «Sobre las combinaciones de agua con alcohol». En 1867 obtuvo la titularidad en la Universidad de San Petersburgo y comenzó a enseñar química inorgánica, sucediendo al mismo tiempo a Voskresenskii en este puesto; en 1871, había transformado San Petersburgo en un centro de investigación química reconocido internacionalmente.
Desarrollo de la tabla periódica

En 1863, había 56 elementos conocidos y se descubrían elementos nuevos a un ritmo de aproximadamente uno por año. Otros científicos habían identificado previamente la periodicidad de los elementos. John Newlands describió una Ley de Octavas, anotando su periodicidad según el peso atómico relativo en 1864, publicándola en 1865. Su propuesta identificó el potencial de nuevos elementos como el germanio. El concepto fue criticado y su innovación no fue reconocida por la Sociedad de Químicos hasta 1887. Otra persona que propuso una tabla periódica fue Lothar Meyer, quien publicó un artículo en 1864 describiendo 28 elementos clasificados por su valencia, pero sin predicciones de nuevos elementos.
Después de convertirse en profesor en 1867, Mendeleev escribió el libro de texto definitivo de su época: Principios de Química (dos volúmenes, 1868-1870). Fue escrito mientras preparaba un libro de texto para su curso. Fue entonces cuando hizo su descubrimiento más importante. Mientras intentaba clasificar los elementos según sus propiedades químicas, notó patrones que le llevaron a postular su tabla periódica; afirmó haber previsto la disposición completa de los elementos en un sueño:
Vi en un sueño una mesa en la que todos los elementos encajaban en su lugar, según se requería. Despertando, inmediatamente lo escribí en un pedazo de papel, sólo en un lugar pareció necesaria una corrección posterior.
Dmitri Mendeleev
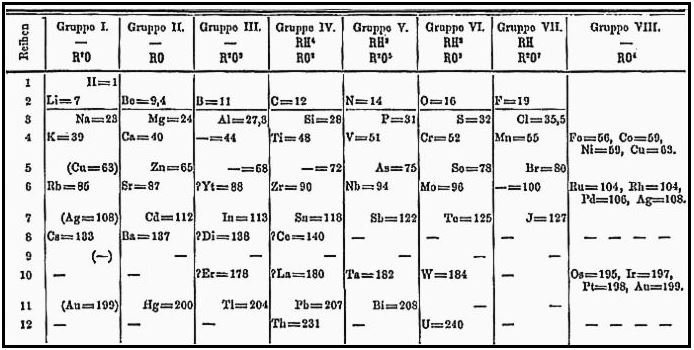
Desconociendo el trabajo anterior sobre las tablas periódicas que se realizaban en la década de 1860, hizo la siguiente tabla:
Añadiendo elementos adicionales siguiendo este patrón, Dmitri Mendeleev desarrolló su versión extendida de la tabla periódica. El 6 de marzo de 1869, hizo una presentación formal a la Sociedad Química Rusa, titulada La dependencia entre las propiedades de los pesos atómicos de los elementos, que describía los elementos según el peso atómico (ahora llamado masa atómica relativa) y la valencia. En esta presentación declaró que
- Los elementos, si se ordenan según su peso atómico, muestran una aparente periodicidad de propiedades.
- Los elementos que son similares en cuanto a sus propiedades químicas tienen pesos atómicos similares (por ejemplo, Pt, Ir, Os) o tienen sus pesos atómicos aumentando regularmente (por ejemplo, K, Rb, Cs).
- La disposición de los elementos en grupos de elementos en el orden de sus pesos atómicos corresponde a sus llamadas valencias, así como, en cierta medida, a sus propiedades químicas distintivas; como se aprecia entre otras series en la de Li, Be, B, C, N, O y F.
- Los elementos más difundidos tienen pequeños pesos atómicos.
- La magnitud del peso atómico determina el carácter del elemento, así como la magnitud de la molécula determina el carácter de un cuerpo compuesto.
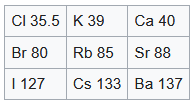
- Debemos esperar el descubrimiento de muchos elementos aún desconocidos, por ejemplo, dos elementos, análogos al aluminio y al silicio, cuyos pesos atómicos estarían entre 65 y 75.
- El peso atómico de un elemento puede a veces ser modificado por el conocimiento de los de sus elementos contiguos. Así pues, el peso atómico del telurio debe situarse entre 123 y 126, y no puede ser 128. (El peso atómico del telurio es 127,6, y Mendeleev se equivocó al suponer que el peso atómico debe aumentar con la posición dentro de un período).
- Ciertas propiedades características de los elementos pueden predecirse a partir de sus pesos atómicos.
Mendeleev publicó su tabla periódica de todos los elementos conocidos y predijo varios elementos nuevos para completar la tabla en una revista en ruso. Sólo unos meses después, Meyer publicó una tabla prácticamente idéntica en una revista en lengua alemana. Mendeleev tiene la distinción de predecir con precisión las propiedades de lo que llamó ekasilicio, ekaaluminio y ekaboron (germanio, galio y escandio, respectivamente).
Dmitri Mendeleev también propuso cambios en las propiedades de algunos elementos conocidos. Antes de su trabajo, se suponía que el uranio tenía valencia 3 y peso atómico alrededor de 120. Mendeleev se dio cuenta de que estos valores no encajaban en su tabla periódica, y duplicó ambos a valencia 6 y peso atómico 240 (cerca del valor moderno de 238).

Para sus predicciones de ocho elementos, usó los prefijos de eka, dvi y tri (sánscrito uno, dos, tres) para nombrarlos. Mendeleev cuestionó algunos de los pesos atómicos actualmente aceptados (en ese momento sólo podían medirse con una precisión relativamente baja), señalando que no se correspondían con los sugeridos por su Ley Periódica.
Señaló que el telurio tiene un peso atómico más alto que el yodo, pero los colocó en el orden correcto, prediciendo incorrectamente que los pesos atómicos aceptados en ese momento eran defectuosos. Estaba desconcertado sobre dónde poner los lantánidos conocidos, y predijo la existencia de otra fila que eran los actínidos que eran algunos de los más pesados en peso atómico. Algunos desestimaron a Mendeleev por predecir que habría más elementos, pero se demostró que estaba en lo cierto cuando se encontró Ga (galio) y Ge (germanio) en 1875 y 1886 respectivamente, encajando perfectamente en los dos espacios que faltaban.
El borrador original hecho por Mendeleev se encontraría años más tarde y se publicaría bajo el nombre de Sistema Tentativo de Elementos.
A Dmitri Mendeleev se le suele llamar el Padre de la Tabla Periódica. Llamó a su tabla o matriz, «el Sistema Periódico».
Últimos años de Mendeleev
En 1876 se obsesionó con Anna Ivanova Popova y comenzó a cortejarla; en 1881 le propuso matrimonio y amenazó con suicidarse si ella se negaba. Su divorcio de Leshcheva finalizó un mes después de haberse casado con Popova (el 2 de abril) a principios de 1882. Incluso después del divorcio, Mendeleev era técnicamente bígamo; la Iglesia Ortodoxa Rusa exigía al menos siete años antes de volver a casarse legalmente.
Su divorcio y la controversia que lo rodeaba contribuyeron a que no fuera admitido en la Academia Rusa de Ciencias (a pesar de su fama internacional en ese momento). La hija de su segundo matrimonio, Lyubov, se convirtió en la esposa del famoso poeta ruso Alexander Blok. Sus otros hijos fueron el hijo Vladimir (marinero, participó en el notable viaje al Este de Nicolás II) y la hija Olga, de su primer matrimonio con Feozva, y el hijo Ivan y los gemelos de Anna.
Aunque Mendeleev fue ampliamente honrado por organizaciones científicas de toda Europa, incluyendo (en 1882) la Medalla Davy de la Royal Society de Londres (que más tarde también le concedió la Medalla Copley en 1905), renunció a la Universidad de San Petersburgo el 17 de agosto de 1890. Fue elegido miembro extranjero de la Royal Society (ForMemRS) en 1892, y en 1893 fue nombrado director de la Oficina de Pesos y Medidas, puesto que ocupó hasta su muerte.

Mendeleev también investigó la composición del petróleo y ayudó a fundar la primera refinería de petróleo en Rusia. Reconoció la importancia del petróleo como materia prima para los productos petroquímicos. Se le atribuye la observación de que quemar petróleo como combustible «sería como encender una estufa de cocina con billetes de banco».
En 1905, Mendeleev fue elegido miembro de la Real Academia Sueca de Ciencias. Al año siguiente, el Comité Nobel de Química recomendó a la Academia Sueca que otorgara el Premio Nobel de Química de 1906 a Mendeleev por su descubrimiento del sistema periódico. La Sección de Química de la Academia Sueca apoyó esta recomendación.
Se suponía que la Academia debía aprobar la elección del Comité, como lo ha hecho en casi todos los casos. Inesperadamente, en la reunión de la Academia, un miembro disidente del Comité Nobel, Peter Klason, propuso la candidatura de Henri Moissan, a quien favorecía. Svante Arrhenius, aunque no era miembro del Comité del Nobel de Química, tuvo una gran influencia en la Academia y también presionó para que se rechazara a Mendeleev, argumentando que el sistema periódico era demasiado antiguo para reconocer su descubrimiento en 1906. Según los contemporáneos, Arrhenius estaba motivado por el rencor que le guardaba a Mendeleev por su crítica a la teoría de la disociación de Arrhenius. Después de acaloradas discusiones, la mayoría de la Academia eligió a Moissan por un margen de un voto. Los intentos de nominar a Mendeleev en 1907 se vieron de nuevo frustrados por la absoluta oposición de Arrhenius.
En 1907, Mendeleev murió a la edad de 72 años en San Petersburgo a causa de la gripe. Sus últimas palabras fueron para su médico: «Doctor, usted tiene la ciencia, yo tengo la fe», que es posiblemente una cita de Julio Verne.
Otros aportes a la ciencia y la química de Mendeleev
Mendeleev hizo otras contribuciones importantes a la química. El químico e historiador de la ciencia ruso Lev Chugaev lo caracterizó como «un químico de genio, físico de primera clase, un investigador fructífero en los campos de la hidrodinámica, la meteorología, la geología, ciertas ramas de la tecnología química (explosivos, petróleo y combustibles, por ejemplo) y otras disciplinas adyacentes a la química y la física, un profundo experto de la industria química y la industria en general, y un pensador original en el campo de la economía». Mendeleev fue uno de los fundadores, en 1869, de la Sociedad Química Rusa. Trabajó en la teoría y la práctica del comercio proteccionista y en la agricultura.
En un intento de concepción química del éter, planteó la hipótesis de que existían dos elementos químicos inertes de menor peso atómico que el hidrógeno, de los cuales pensó que el más ligero era un gas omnipresente y penetrante, y el ligeramente más pesado era un elemento propuesto, el coronium.
Mendeleev dedicó mucho estudio e hizo importantes contribuciones a la determinación de la naturaleza de tales compuestos indefinidos como soluciones.
En otro apartado de química física, investigó la expansión de los líquidos con calor, e ideó una fórmula similar a la ley de Gay-Lussac de la uniformidad de la expansión de los gases, mientras que en 1861 anticipó la concepción de Thomas Andrews de la temperatura crítica de los gases definiendo el punto de ebullición absoluto de una sustancia como la temperatura a la que la cohesión y el calor de la vaporización se vuelven iguales a cero y el líquido cambia a vapor, independientemente de la presión y el volumen.
Se le da crédito a Mendeleev por la introducción del sistema métrico en el Imperio Ruso.
Inventó el pirocollodion, una especie de polvo sin humo basado en la nitrocelulosa. Este trabajo había sido encargado por la Armada Rusa, que sin embargo no adoptó su uso. En 1892 Mendeleev organizó su fabricación.
Mendeleev estudió el origen del petróleo y concluyó que los hidrocarburos son abiogénicos y se forman en las profundidades de la tierra. Escribió: «El hecho capital a destacar es que el petróleo nació en las profundidades de la tierra, y es sólo allí donde debemos buscar su origen«. (Dmitri Mendeleev, 1877)

A partir del decenio de 1870, publicó ampliamente más allá de la química, examinando aspectos de la industria rusa y cuestiones técnicas de la productividad agrícola. Exploró cuestiones demográficas, patrocinó estudios del Mar Ártico, trató de medir la eficacia de los fertilizantes químicos y promovió la marina mercante.
Fue especialmente activo en la mejora de la industria petrolera rusa, haciendo comparaciones detalladas con la industria más avanzada de Pensilvania. Aunque no estaba bien fundamentado en la economía, había observado la industria a lo largo de sus viajes por Europa, y en 1891 ayudó a convencer al Ministerio de Hacienda de que impusiera aranceles temporales con el fin de fomentar las industrias incipientes rusas.
En 1890 renunció a su cátedra en la Universidad de San Petersburgo a raíz de una disputa con funcionarios del Ministerio de Educación sobre el trato a los estudiantes universitarios. En 1892 fue nombrado director de la Oficina Central de Pesos y Medidas de Rusia, y lideró el camino para estandarizar los prototipos fundamentales y los procedimientos de medición. Estableció un sistema de inspección e introdujo el sistema métrico en Rusia.

Debatía contra las afirmaciones científicas del espiritualismo, argumentando que el idealismo metafísico no era más que una superstición ignorante. Lamentó la amplia aceptación del espiritismo en la cultura rusa, y sus efectos negativos en el estudio de la ciencia
Mito del vodka
Una historia rusa muy popular atribuye a Mendeleev el establecimiento del 40% de la graduación del vodka. Por ejemplo, el vodka estándar ruso se anuncia: «En 1894, Dmitri Mendeleev, el más grande científico de toda Rusia, recibió el decreto para establecer el estándar de calidad imperial para el vodka ruso y nació el ‘Estándar Ruso'» Otros citan «la más alta calidad de vodka ruso aprobada por la comisión del gobierno real encabezada por Mendeleev en 1894».
De hecho, la norma del 40% ya fue introducida por el gobierno ruso en 1843, cuando Mendeleev tenía nueve años. Es cierto que Mendeleev en 1892 se convirtió en jefe del Archivo de Pesos y Medidas de San Petersburgo, y lo convirtió en una oficina del gobierno al año siguiente, pero esa institución estaba encargada de estandarizar los pesos y medidas comerciales rusos, no de establecer ningún estándar de calidad en la producción. También, la disertación doctoral de Mendeleev de 1865 se tituló «Un discurso sobre la combinación de alcohol y agua», pero sólo discutió las concentraciones de alcohol de fuerza médica por encima del 70%, y nunca escribió nada sobre el vodka.
Para más información Mendeleev – the man and his legacy…