Tiempo de lectura estimado: 7 minutos
La densidad es una propiedad fundamental que permite clasificar soluciones de acuerdo con su concentración.
La densidad es una propiedad física fundamental de la materia. Las propiedades físicas son las características que pueden ser determinadas sin cambiar la identidad química de las sustancias. Entre las propiedades físicas podemos encontrar el punto de fusión, el punto de ebullición, la solubilidad entre otras.
En el trabajo de laboratorio, la estimación de los valores de las diversas propiedades que se miden se realiza a través de instrumentos y la ayuda de los sentidos. Sin embargo, la manipulación manual, así como las limitaciones en la capacidad de medición de los instrumentos, introducen pequeños errores que se deben tener en cuenta en el tratamiento estadístico de los datos obtenidos.
Densidad de soluciones
La densidad es una de las principales propiedades físicas de la materia. La densidad se define como la relación que existe entre la masa de un objeto con su volumen, entre mayor masa a un volumen constante, mayor su densidad. De manera reciproca, a menor volumen a una masa constante, mayor va a ser la densidad de la sustancia. La densidad puede expresarse en diversas unidades, generalmente en kg/m3, pero a nivel laboratorio se emplean unidades mas pequeñas como g/cm3, g/mL o mol/mL.
La densidad es una característica propia de cada sustancia y sirve para diferenciar una sustancia pura de otras. En el caso de soluciones, su densidad puede ser usada para determinar su concentración. Sin embargo, una sola medida de densidad puede tener un alto porcentaje de error, así que, para obtener una medida mas cercana a su valor real, se deben realizar múltiples mediciones y aplicar herramientas estadísticas que permitan calcular dicho valor y su desviación de la medida central obtenida.
Introducción a la estadística en el laboratorio
El valor promedio de una serie de datos (x¯ ) se define como la suma de todos los valores (∑) dividido en la cantidad de medidas (N)

Por otra parte, la desviación estándar (s) se define como:

E indica el grado en el cual los valores medidos se desvían del valor promedio de los mismos. Los conjuntos de valores que tienen rangos amplios tienen valores de desviación estándar grandes y están asociados a una menor precisión en los valores medidos. En ocasiones uno o mas valores medidos se alejan del comportamiento general del resto de valores, estos son conocidos como datos atípicos y deben ser excluidos para evitar que afecten de manera negativa al resto de valores.
Materiales
- Pipeta volumétrica de 10 mL
- Propipeta o pera neumática
- Bureta de 50 mL
- 2 Erlenmeyer de 50 mL
- Probeta de 100 mL
- 2 beaker de 100 mL
- 1 beaker de 100 mL
- Balanza electrónica*
- Botella de lavado
- Soporte universal
- Llave para bureta
Reactivos
- Agua destilada
- 2 bebidas carbonatadas desgasificadas (1 normal y 1 dietética)**
* La balanza electrónica se sugiere por su facilidad de uso, sin embargo, también se puede emplear una balanza mecánica
** para desgasificar las bebidas se calientan en un beaker hasta ebullición y dejar enfriar toda la noche antes de realizar las mediciones.
Procedimiento – densidad de soluciones
Precisión del material volumétrico
Todo el material de vidrio debe ser enjuagado con agua destilada antes de su uso.
En un beaker de 100 mL, obtener aproximadamente 50 mL de agua destilada. Pesar un beaker de 50 mL seco en la balanza y anotar su masa.
Llenar la probeta de 100 mL con aproximadamente 10 mL de agua destilada, anotar el volumen vertido teniendo en cuenta que la medición se debe hacer en la parte inferior del menisco generado por el líquido. Transferir este liquido al beaker previamente pesado y medir la masa del conjunto. Después de la medición desechar el agua destilada y secar de nuevo el beaker.
Empleando la pipeta aforada o volumétrica de 10 mL transferir exactamente 10 mL de agua destilada al beaker seco y pesado. Anotar los valores obtenidos. Después de la medición desechar el liquido y secar de nuevo el beaker.
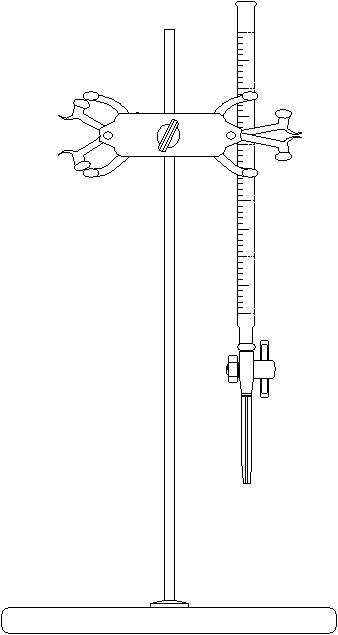
Con el soporte universal y la pinza para bureta, realizar el montaje adecuado para el uso de la bureta. Llenar la bureta con el liquido restante en el beaker de 100 mL y anotar el valor inicial de la bureta. Vaciar aproximadamente 10 mL del agua en la bureta en el beaker seco y pesado previamente. Anotar el volumen transferido (volumen final – volumen inicial en la bureta) y la masa del beaker con el agua contenida.
Calcular la densidad del agua destilada para cada una de las mediciones obtenidas (probeta – pipeta – bureta) teniendo en cuenta que la masa del agua se debe calcular restando la masa del beaker seco previamente obtenida. Compartir los datos con los demás grupos de laboratorio y obtener mínimo 10 datos de densidad para cada uno de los instrumentos empleados en la práctica. Si no hay suficientes grupos en el laboratorio, repetir las mediciones hasta obtener los 10 datos necesarios.
Densidad de bebidas carbonatadas desgasificadas
El procedimiento se llevará a cabo primero con la bebida regular y después se debe repetir con la bebida dietética.
Empleando un montaje con bureta, dispensar volúmenes precisos de la bebida. La bureta debe primero lavarse con agua destilada y posteriormente con una pequeña cantidad de la bebida a emplear antes de llenarla totalmente.
Usando un beaker de 100 mL, obtener aproximadamente 60 mL de la bebida regular, llenar la bureta con este liquido y anotar el volumen inicial.
Secar y pesar un Erlenmeyer de 50 mL usando la balanza. Anotar su masa. Vaciar de la bureta 5 mL de bebida en el Erlenmeyer y anotar el volumen final en la bureta. Medir la masa del Erlenmeyer mas el liquido y anotar la masa.
A continuación, agregar 5 mL mas de liquido desde la bureta al Erlenmeyer. De nuevo anotar el volumen final en la bureta y medir la masa del conjunto Erlenmeyer – liquido. Repetir este procedimiento cuatro veces más.
Repetir todo el procedimiento con la bebida dietética y anotar las observaciones.
Despues del experimento
Realizar una tabla con los valores de densidad obtenidos con los tres instrumentos volumétricos trabajados. Calcular la densidad promedio y la desviación estándar de cada uno de los conjuntos de datos obtenidos para la probeta, la pipeta y la bureta. Graficar empleando una herramienta de calculo (como por ejemplo Microsoft Excel ®) los valores de densidad de soluciones obtenidos para cada instrumento e identificar posibles datos atípicos. Eliminar dichos datos atípicos y recalcular el valor promedio y la desviación estándar.
Analizar que instrumento posee mayor desviación estándar y que valor promedio es el mas cercano al valor teórico de la densidad del agua (densidad = 1 g/mL).
Para los datos obtenidos con las bebidas carbonatadas, calcular la densidad de cada medición y obtener un valor promedio de densidad de cada una de las bebidas trabajadas. ¿Qué bebida tiene mas densidad?, ¿puede tener una explicación química esta diferencia de densidad? ¿las bebidas carbonatadas son más densas o menos densas que el agua? ¿Por qué es necesario desgasificar las bebidas y dejarlas enfriar antes de realizar las mediciones?
Recomendaciones de seguridad
En todo momento se deben utilizar los elementos de seguridad básicos en el laboratorio de química (bata de laboratorio, guantes, gafas de seguridad y demás que sean exigidos por las normas internas, locales o nacionales. Los residuos generados por la practica deben ser dispuestos de manera adecuada según las normas de laboratorio y las normas locales y nacionales respectivas.
The Densities of Solutions and Solids (Experiment)
Clasificación
Nivel: Universitario
Tipo: Practica de enseñanza
Riesgo: bajo