John Newlands
Tiempo de lectura estimado: 7 minutos
John Alexander Reina Newlands (26 de noviembre de 1837 – 29 de julio de 1898) fue un químico británico que trabajó en relación con la periodicidad de los elementos.
Newlands fue uno de los precursores de Mendeleev en la formulación del concepto de periodicidad en las propiedades de los elementos químicos. Fue el segundo hijo de un ministro presbiteriano, William Newlands, de quien recibió su educación general. En 1856 ingresó en el Real Colegio de Química, donde estudió durante un año con A. W. Hofmann. Luego se convirtió en asistente de J. T. Way, químico de la Real Sociedad Agrícola. Permaneció en Way hasta 1864, excepto por un breve interludio en 1860, cuando sirvió como voluntario con Garibaladi en Italia. La madre de Newlands, Mary Sarah Reina, era de ascendencia italiana..
Infancia y educación
Fue educado en casa por su padre, y luego estudió en el Royal College of Chemistry. Estaba interesado en la reforma social y durante 1860 sirvió como voluntario con Giuseppe Garibaldi en su campaña militar para unificar Italia.
En 1864 se estableció como químico analítico y complementó sus ingresos enseñando química. Parece que hizo un estudio especial de la química del azúcar y en 1868 se convirtió en jefe químico en una refinería perteneciente a James Duncan, con quien desarrolló un nuevo sistema de limpieza del azúcar e introdujo una serie de mejoras en el procesamiento.
El negocio decayó como resultado de la competencia extranjera, y en 1886 dejó la refinería y se estableció de nuevo como analista, esta vez en asociación con su hermano, B. E. R. Newlands. Los hermanos colaboraron con C. G. W. Lock, uno de los autores anteriores, en la revisión de un tratado establecido sobre el cultivo y la refinación del azúcar. Newlands murió en 1898; le sobrevivieron su esposa, una hija y un hijo.
Newlands y los elementos
Los primeros trabajos de Newlands fueron sobre compuestos orgánicos, el primero sugiriendo una nueva nomenclatura, el segundo proponiendo la elaboración de tablas para mostrar las relaciones entre los compuestos, estaban viciados por la ausencia en ese momento de ideas claras sobre la estructura y la valencia; pero son interesantes porque muestran el rumbo de su mente hacia la sistematización.
Newlands fue la primera persona en diseñar una tabla periódica de elementos químicos dispuestos en orden de sus masas atómicas relativas.
Triadas y octavas
Su primera comunicación (Chemical News, 7 de febrero de 1863) sobre las relaciones numéricas existentes entre los pesos atómicos de elementos similares fue una síntesis, con algunas de sus propias observaciones, de lo que habían señalado otros (de los que sólo mencionó a Dumas). Se habían observado dos fenómenos principales: a) existían «tríadas» (observadas por primera vez por Döbereiner), grupos de tres elementos de propiedades similares, siendo el peso atómico de uno la media numérica de los otros, y b) se constató también que la diferencia entre los pesos atómicos de elementos análogos parecía ser a menudo un múltiplo de ocho.
Continuando el trabajo de Johann Wolfgang Döbereiner con las tríadas y las familias de elementos similares de Jean-Baptiste Dumas, publicó en 1865 su ‘Ley de las octavas’, que afirmaba que ‘cualquier elemento dado exhibirá un comportamiento análogo al octavo elemento que lo sigue en la tabla ‘
Al igual que muchos de sus contemporáneos, Newlands utilizó en un principio los términos «equivalente» y «peso atómico» sin distinción de significado, y en este primer trabajo hizo una distinción de significado, y en este primer trabajo empleó los valores aceptados por sus predecesores. En una carta de julio de 1864 utilizó los valores de A. W. Williamson, que se basaban en el sistema de Cannizzaro. La carta contiene una tabla de los sesenta y un elementos conocidos en el orden de sus «nuevos» pesos atómicos. En una segunda tabla agrupó treinta y siete elementos en diez clases, la mayoría de las cuales contenían una o más tríadas.
La incertidumbre sobre las propiedades de los nuevos elementos
El carácter incompleto de la tabla se atribuyó a la incertidumbre sobre las propiedades de algunos de los elementos más recientemente descubiertos y también a la posible existencia de elementos no descubiertos. Consideraba que el silicio (peso atómico 28) y el estaño (peso atómico 118) eran las extremidades de una tríada, cuyo término medio se desconocía; de ahí que sea válida su posterior afirmación de haber predicho la existencia del germanio (peso atómico 73) antes de Mendeleev
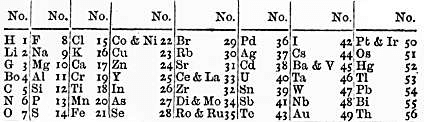
Aproximadamente un mes después dijo que si los elementos se numeraban en el orden de sus pesos atómicos (dando el mismo número a dos cualesquiera con el mismo peso) se observaba «que los elementos que tienen números consecutivos frecuentemente pertenecen al mismo grupo u ocupan posiciones similares en otros grupos». En la siguiente tabla se muestra una ilustración de las ideas de Newlands:

La diferencia entre el número del miembro más bajo de un grupo y el inmediatamente superior era de siete: «en otras palabras, el octavo elemento a partir de uno dado es una especie de repetición del primero, como la octava nota en una octava de música«. Se habían hecho una o dos transposiciones para dar una agrupación aceptable; el elemento omitido (nº 51) habría sido el mercurio, que claramente no podía ser agrupado con los halógenos.
La ley de octavas de Newlands
Newlands iba a tientas hacia un importante descubrimiento, aunque no suscitaba muchos comentarios. Un año más tarde (agosto de 1865) volvió a llamar la atención sobre la diferencia de siete (o un múltiplo de ellos) entre los números ordinales de los elementos del mismo grupo horizontal: «Esta peculiar relación la propongo llamar provisionalmente la ‘Ley de las Octavas’.» Esta vez puso los sesenta y dos elementos (incluyó el recién descubierto indio) en su tabla:

Pero este forzamiento de los elementos en un marco demasiado rígido debilitó su caso. Parecía excluir (conclusión que posteriormente negó) la posibilidad de que hubiera lagunas en la secuencia que, al ser llenadas, llevarían a una agrupación más aceptable. Las anomalías resultantes fueron aprovechadas por sus críticos cuando el 1 de marzo de 1866 leyó un documento de la Sociedad Química que presentaba la misma tabla, con la excepción de que los elementos de la última columna aparecían ahora en orden numérico. Se ha citado a menudo la pregunta jocosa de G. C. Foster, profesor de física del University College de Londres, sobre si Newlands había examinado alguna vez los elementos colocados en orden alfabético; pero Foster también hizo la crítica contundente de que no se podía aceptar ningún sistema de clasificación que separara el cromo del manganeso y el hierro del cobalto y el níquel.
Mala recepción de la propuesta
La recepción hostil de su documento y la renuencia de la Sociedad a publicarlo (debido a su naturaleza puramente teórica) parecen haber desalentado a Newlands a seguir sus ideas hasta después de la publicación de la tabla de Mendeleev en 1869. Después de que apareciera esa tabla, Newlands siguió buscando relaciones numéricas entre los pesos atómicos, mientras intentaba, en una serie de cartas a Chemical News, establecer su prioridad. Expuso sus reclamos más específicamente en diciembre de 1882, al enterarse de la concesión de la Medalla Davy de la Royal Society a Mendeleev y Lothar Meyer. Su persistencia fue finalmente recompensada en 1887, cuando se le concedió la medalla.
Fallecimiento
John Newlands murió debido a complicaciones de una cirugía en su casa en Lower Clapton, Middlesex, y fue enterrado en el cementerio de West Norwood. Su negocio continuó después de su muerte por su hermano menor, Benjamin.
Para más información Newlands’ Periodic Table