Tiempo de lectura estimado: 3 minutos
A inicios del siglo XX se realizaron ajustes en la tabla periódica para incluir nuevos elementos descubiertos, así como a los gases nobles.
Los gases nobles y la tabla periódica
El químico inglés Henry Cavendish, descubridor del hidrógeno en 1766, descubrió que el aire está compuesto de más gases que el nitrógeno y el oxígeno y registró estos hallazgos en 1784 y 1785; entre ellos, encontró un gas entonces no identificado que era menos reactivo que el nitrógeno.
En 1895, William Ramsay y Lord Rayleigh aislaron el argón del aire y determinaron que era un elemento nuevo.
Tras este descubrimiento, Ramsay señaló que en la tabla periódica faltaba todo un grupo de gases, los gases nobles. Usando la destilación fraccionada para separar el aire, Ramsay descubrió tres gases nobles más en 1898: neón, criptón y xenón.
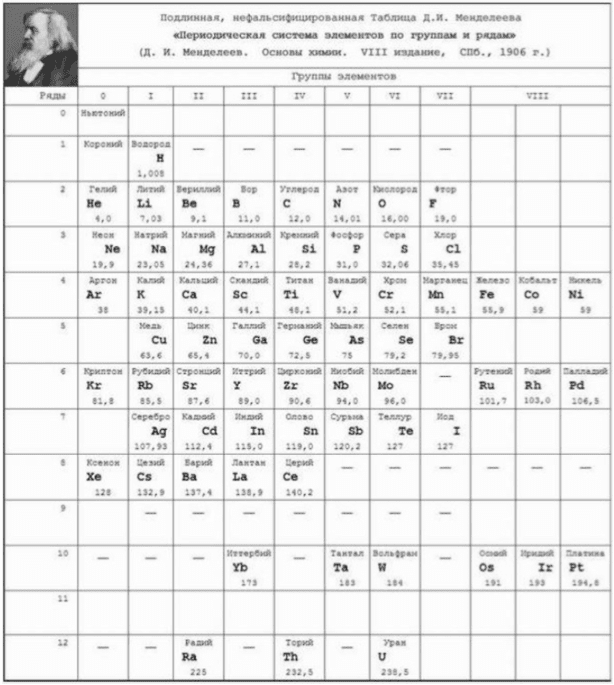
Aunque la tabla de Mendeleev predijo varios elementos no descubiertos, no predijo la existencia de gases nobles. Mendeleev los añadió a la tabla como Grupo 0 en 1902, sin alterar el concepto básico de su la tabla periódica.
Reordenando la tabla
Además de las predicciones de escandio, galio y germanio, la tabla de 1871 de Mendeleev dejó muchos más espacios para elementos no descubiertos, aunque no proporcionó predicciones detalladas de sus propiedades.
En total, predijo dieciocho elementos, aunque sólo la mitad correspondían a elementos que fueron descubiertos más tarde. Observó que una fila entera de su tabla parecía faltar entre el cerio y el tántalo, atribuyendo esta anomalía a la supuesta naturaleza de estos elementos.
Esta disposición se utilizó para mantener la coherencia con la estructura de ocho columnas, así como la colocación de los elementos desde el osmio hasta el oro, que eran conocidos por ser análogos de los elementos desde el rutenio hasta la plata.
Sin embargo, predijo los pesos atómicos de algunos de estos elementos, desde 140 para el eka-molibdeno hasta 175 para el eka-caesio. Mientras que los elementos con estos pesos atómicos fueron descubiertos más tarde, su química no se correspondía con los huecos en la tabla de Mendeleev.
Se predijeron correctamente varios análogos más pesados, como el tri-manganeso (renio) y el dvi-yodo (astato), aunque más tarde se descubrió que ocupaban las posiciones de dvi-manganeso y eka-yodo respectivamente.
Este uso impreciso de prefijos fue causado por una ruptura en la estructura de la tabla -la aparente «zona muerta» entre el cerio y el tántalo, en sí misma una consecuencia de la estricta adherencia de Mendeleev a la estructura de ocho columnas.
En 1904, la tabla periódica de Mendeleev reorganizó varios elementos e incluyó los gases nobles junto con la mayoría de los elementos recientemente descubiertos.
Artículos en esta serie
- Historia de la tabla periódica I
- Historia de la tabla periódica II
- Historia de la tabla periódica III
- Historia de la tabla periódica IV
- Historia de la tabla periódica IX
- Historia de la tabla periódica V
- Historia de la tabla periódica VI
- Historia de la tabla periódica VII
- Historia de la tabla periódica VIII
- Historia de la tabla periódica X