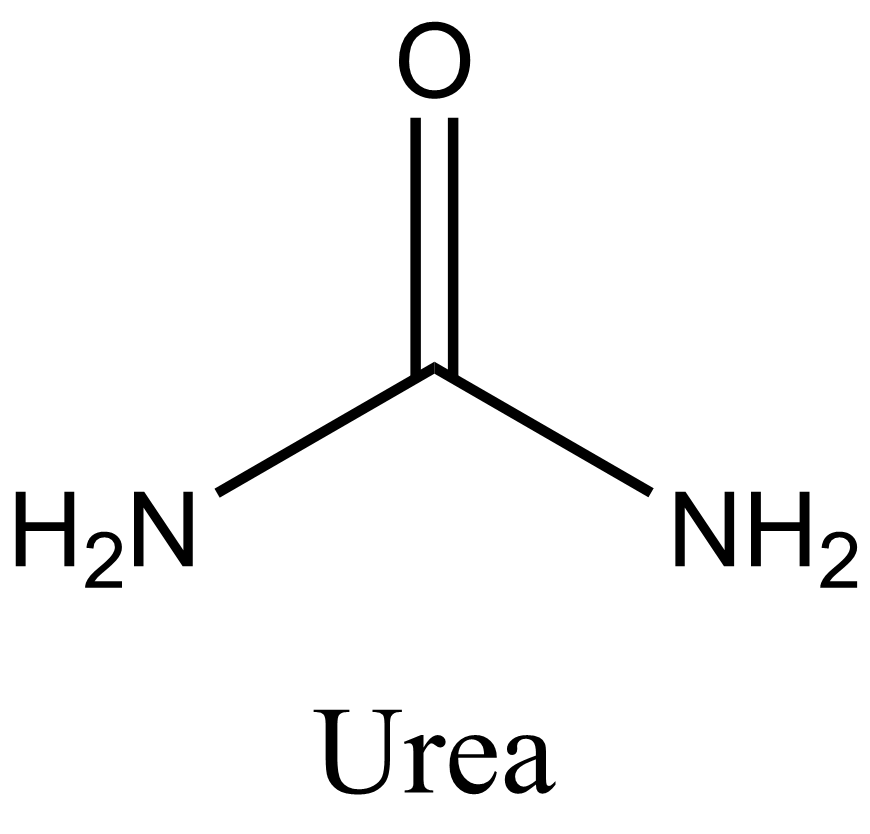
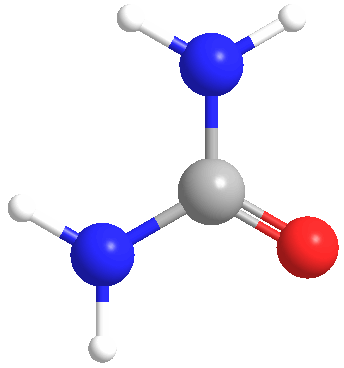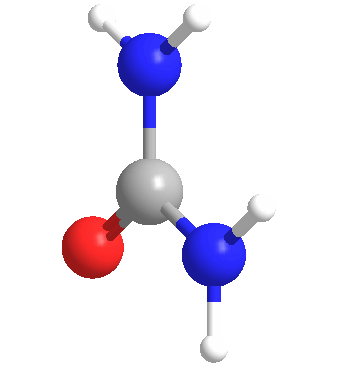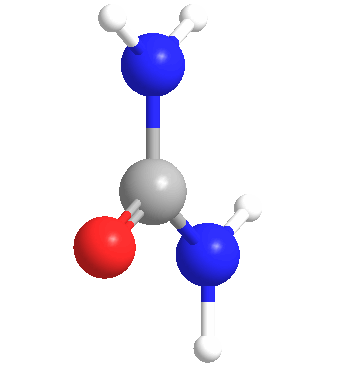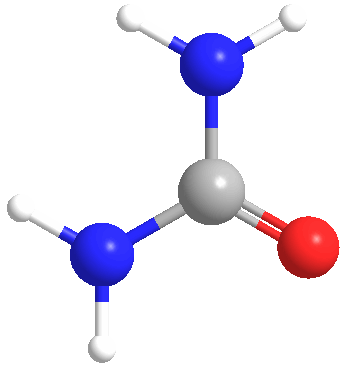
Urea
Estimated reading time: 9 minutos
La urea (también conocida como carbamida) es un producto de desecho de muchos organismos vivos y es el principal componente orgánico de la orina humana. Esto se debe a que está al final de la cadena de reacciones que descomponen los aminoácidos que componen las proteínas. Estos aminoácidos son metabolizados y convertidos en el hígado en amoníaco, CO2, agua y energía.
Pero el amoníaco es tóxico para las células, y por lo tanto debe ser excretado del cuerpo. Las criaturas acuáticas, como los peces, pueden expulsar el amoníaco directamente al agua, pero los animales terrestres necesitan otro método de eliminación. Así que el hígado convierte el amoníaco en un compuesto no tóxico, la urea, que puede ser transportado con seguridad por la sangre a los riñones, donde se elimina en la orina.
Un adulto típicamente excreta unos 25 gramos de urea por día. Cuando la urea se vuelve rancia, las bacterias la convierten de nuevo en amoníaco, lo que da el conocido olor acre de los lavabos. Cualquier condición que impida la eliminación de urea por los riñones puede conducir a la uremia, una acumulación de urea y otros desechos de nitrógeno en la sangre que puede ser fatal. Para revertir esta condición, se debe eliminar la causa de la insuficiencia renal, o el paciente debe someterse a una diálisis de sangre para eliminar los desechos de la sangre.
Historia de la urea
¿Qué tienen en común las cremas para la piel, los pretzels y los fertilizantes? Todos ellos son usos de la urea, la primera molécula de un organismo vivo que se sintetiza en un laboratorio.
La urea tiene una historia bastante interesante. Fue descubierta y aislada por primera vez de la orina humana por H.M. Rouelle en 1773, y luego fue sintetizada con éxito en 1828 por Friedrich Wohler. La síntesis fue casi un accidente, ya que Wohler había estado tratando de hacer otro compuesto, el cianato de amonio, para continuar un estudio de los cianatos en los que había estado trabajando durante los años anteriores. Cuando añadió cianato de plata a la solución de cloruro de amonio obtuvo un material cristalino blanco, que resultó ser idéntico a la urea obtenida a partir de la orina.
Este descubrimiento fue muy importante, ya que hizo de la urea el primer compuesto orgánico que se sintetizó a partir de materiales de partida totalmente inorgánicos. Wohler escribió triunfalmente a Berzelius:
«Debo decirles que puedo hacer urea sin el uso de los riñones, ya sea hombre o perro. El cianato de amonio es urea».
Este descubrimiento supuso un duro golpe para una creencia muy extendida en aquella época llamada «vitalismo». Esta teoría sostenía que los organismos vivos, como las plantas y los animales, estaban hechos de diferentes materiales para inanimar objetos como las rocas.
La creencia era que los organismos vivos poseían una «fuerza vital» desconocida que les permitía fabricar productos químicos orgánicos, y como los objetos inanimados no poseían esta fuerza, no podían crear ni transformarse en los productos químicos de la vida.
El descubrimiento de Wohler demostró que no sólo los químicos orgánicos podían ser modificados por la química, sino que también podían ser producidos a través de la química. En efecto, había demostrado que estamos hechos de los mismos materiales que el resto de la Naturaleza, y por lo tanto somos parte del mundo que nos rodea.
La urea antes de Wöhler
Antes de Wohler, todavía era posible conseguir urea, pero no suena agradable – Herman Boerhaave purificó la urea de la orina 100 años antes. Boerhaave, de Leiden en los Países Bajos, es más conocido ahora como médico y fundador de la enseñanza clínica, y en ese momento no se consideraba a sí mismo como un gran químico. De hecho, sólo publicó su trabajo de química porque se vio obligado a hacerlo cuando sus estudiantes lo publicaron en su nombre. Incluso escribió en su libro: «Nada estaba antes más lejos de mis pensamientos que el hecho de que debería molestar al mundo con algo de química.
Tal vez debido a esta actitud, el trabajo de Boerhaave sobre la urea fue de alguna manera olvidado y 50 años más tarde un método para purificar la urea fue redescubierto por la química francesa Hilaire Rouelle. Desafortunadamente, como pasaron doscientos años hasta que se descubrió el trabajo de Boerhaave, la confusión sobre quién descubrió la urea persiste hasta hoy, aunque Boerhaave está obteniendo lentamente el reconocimiento que merece.
Urea en el cuerpo humano
El cuerpo humano produce urea a partir del amoníaco y el exceso de aminoácidos. Los aminoácidos suelen utilizarse para fabricar las proteínas que necesitamos para funcionar, pero si tenemos más que suficiente pueden ser metabolizados para producir una pequeña cantidad de energía. El amoníaco, por otro lado, es tóxico y por lo tanto es vital que el cuerpo tenga una forma de deshacerse de él.
El amoníaco se produce naturalmente en el curso de la metabolización de los alimentos, pero elevaría el pH a niveles tóxicos si se permitiera que se acumulara en las células. Aunque cuesta energía hacerlo, el amoníaco se convierte en urea, que es prácticamente inofensiva. La urea también es una buena opción porque puede ser eliminada fácilmente a través de la orina e incluso un poco a través del sudor.
Aunque la urea es un componente importante de la orina, en realidad es incolora e inodora. Sin embargo, se descompone fácilmente para convertirse en amoníaco, que es lo que da a la orina su olor característico. Esta es también la razón por la que la orina rancia huele más fuerte que la fresca.
Producción y usos de la urea
Industrialmente, se sintetizan 100 millones de toneladas de urea cada año. Entonces, ¿para qué se utiliza todo esto? Bueno, el 90% se destina a fertilizantes, proporcionando una fuente esencial de nitrógeno para que los cultivos crezcan lo más rápido posible.
La urea se produce comercialmente en varios pasos, que comienzan con la reacción directa del amoníaco con el dióxido de carbono en un reactor de alta presión y temperatura. Es un material de partida muy importante en varias síntesis químicas, y se utiliza a escala industrial para la fabricación de fertilizantes, productos farmacéuticos y resinas.
Fertilizantes
La urea es popular porque tiene el mayor porcentaje de contenido de nitrógeno de los fertilizantes sólidos, lo que significa que se requiere menos peso y por lo tanto es más barato de transportar. La urea se descompone típicamente en amoníaco, que puede ser absorbido por las plantas. Sin embargo, el amoníaco tiende a evaporarse, reduciendo la cantidad de nitrógeno disponible en el suelo. Para evitar esto, particularmente durante el verano, los agricultores esparcirán la urea en los campos justo antes de que se produzca lluvia.
El amoníaco también puede ser oxidado por las bacterias del suelo, creando nitratos. Los nitratos son fácilmente absorbidos por las plantas, pero pueden ser fácilmente llevados por el agua de lluvia, que se escapa a los lagos y ríos cercanos. Esto se está convirtiendo en un problema cada vez mayor porque fomenta el crecimiento de las plantas en el agua, lo que puede perturbar el ecosistema local. En la región de Bretaña, Francia, se observan floraciones masivas de algas cada verano debido a la gran industria agrícola de la zona. Cada año, se requieren excavadoras para limpiar las toneladas de algas que se dejan pudrir en las playas.
Desde Wohler, el método para sintetizar la urea ha sido adaptado. El proceso Bosch-Meiser reacciona con amoníaco y dióxido de carbono, bajo alta temperatura y presión, para formar carbonato de amonio que luego se descompone en urea y agua. Aunque fue desarrollado por primera vez en 1922, sigue siendo la forma estándar de producir urea, gracias a los reactivos baratos que se utilizan.
Otros usos
La urea es uno de los precursores de los diversos barbitúricos, que se utilizan ampliamente como sedantes y somníferos. La urea también se utiliza en la producción de uretanos, que luego se polimerizan para formar espumas de poliuretano. Otra aplicación importante es en la fabricación de resinas y polímeros. La urea puede reaccionar con el formaldehído para fabricar las resinas de urea-formaldehído, que son muy importantes en los plásticos moldeados.
Otro producto derivado de la urea es la melamina, que se forma por la deshidratación de la urea, y se utiliza principalmente en la producción de resinas de melamina-formaldehído que tienen una dureza y una resistencia a las manchas mucho mayores que las resinas de urea-formaldehído. Ambos tipos de resinas poliméricas tienen usos muy variados, incluyendo adhesivos, laminados, compuestos para moldear, revestimientos y acabados textiles. Otros usos poco conocidos incluyen suavizante de piel en cremas cosméticas y colorante para pretzels.
Hay pocas moléculas que tengan un lugar tan importante en la historia de la química. La historia de la urea tiene casi 300 años, desde sus orígenes bastante malolientes hasta la fertilización de los cultivos del mundo. Su síntesis puede haber sido un accidente afortunado, pero sentó las bases de la química orgánica de hoy en día.
Para más información Urea in the history of organic chemistry: Isolation from natural sources. Frederick Kurzer and Phyllis M. Sanderson. Journal of Chemical Education 1956 33 (9), 452. DOI: 10.1021/ed033p452