Tiempo de lectura estimado: 7 minutos
Al ser una técnica compleja, en el revelado de placas de cromatografía de capa fina o TLC pueden ocurrir problemas que impidan la correcta visualización de los compuestos. A continuación, se encuentra una lista de los problemas más comunes, sus posibles orígenes y soluciones.
El compuesto no apareció
Incluso cuando un compuesto se ha aplicado con certeza en la línea de base de una placa de TLC, es posible que el compuesto no se vea en el revelado de la placa de cromatografía después de la elución. Hay varias razones posibles para esto:
El compuesto puede estar demasiado diluido.
Una solución simple a un problema de dilución es añadir más compuesto a la muestra original y ejecutar la cromatografía de nuevo usando una nueva placa. Si se espera que el compuesto sea activo en luz UV (es decir, si contiene un anillo aromático), es una buena idea ver la placa de TLC bajo luz UV antes de eluir la placa (Figura 1a). Cuando la marca de la muestra no es visible antes de la elución, no lo será después, ya que los compuestos se difunden durante la elución.
Al determinarse que la muestra está sólo ligeramente demasiado diluida, el material puede depositarse varias veces antes de la elución (Figura 1b). Para ello, se coloca un pequeño punto de muestra en la línea de base y se deja secar completamente (ayuda a soplar sobre él) antes de entregar otro punto sobre el primero. Si no se deja secar los puntos entre las aplicaciones, el punto será demasiado grande. Si se espera que el compuesto sea activo en la luz UV, compruebe la plancha bajo la luz UV y, si es necesario, remarque la mancha más veces antes de la elución.

El compuesto puede haberse evaporado.
Una placa de TLC debe ser visualizada inmediatamente después de la elución, por lo que si ha transcurrido un tiempo moderado entre la ejecución de la cromatografía en capa delgada y su revelado, la evaporación puede ser la causa del problema. Una solución a este problema es volver a ejecutar la cromatografía y visualizarla inmediatamente.
Si el compuesto tiene un punto de ebullición bajo, probablemente se evaporó durante la elución. Por ejemplo, el 2-penteno (punto de ebullición 36°C) fue visto en el carril número 1 de la figura 1.45c no se tiñó con permanganato después de la elución, aunque el compuesto es reactivo a la tinción (una muestra no diluida y sin eluir de 2-penteno se tiñó un poco en una placa de TLC de desecho, Figura 1d). Los compuestos con puntos de ebullición inferiores a aproximadamente 120°C son difíciles de analizar a través de TLC.
El compuesto puede no reaccionar a la técnica de visualización.
Las técnicas de visualización a menudo se adaptan a ciertos grupos funcionales. Por ejemplo, la luz ultravioleta suele ser buena para visualizar compuestos aromáticos pero mala para otros grupos funcionales. Si la luz ultravioleta, el yodo o una tinción no logran visualizar un compuesto, podría significar que el compuesto simplemente no es reactivo a la técnica, por lo que debería probarse otro método.
Por ejemplo, en la figura 2 se muestran, para diferentes compuestos visualizados con UV (figura 2a), la tinción de p-anisaldehído (figura 2b) y el yodo (figura 2c). El compuesto en el carril 1 de todas las placas (4-heptanona) sólo fue visible con la tinción de anisaldehído (mancha azul), y no con UV o I2. El compuesto en el carril 4 de todas las placas (benzoato de etilo) no era reactivo al teñido con anisaldehído, pero podía ser visualizado con UV y I2. La impureza presente en la línea de base del carril 3 (ácido cinámico) era fuertemente activa a la luz UV, pero difícilmente podía ser vista con las otras manchas.

La marca obtenida con UV es diferente de la tinción
La luz ultravioleta es a menudo la primera técnica de visualización que se intenta en una placa de TLC eluida, porque no es destructiva y es bastante simple de llevar a cabo. Si se ve una mancha oscura con una lámpara ultravioleta, se acostumbra a rodear la mancha con un lápiz (como en la figura 2b), ya que la mancha será invisible cuando se retire la lámpara. A menudo se realiza otra técnica de visualización después de ver la placa bajo UV, y no es raro que la mancha posterior se extienda a una región más pequeña o grande que la marca realizada con lápiz.
Por ejemplo, el compuesto del carril 2 de la figura 2 (acetofenona) puede verse fácilmente con luz ultravioleta (figura 2a), pero en la placa visualizada con yodo (figura 2c), las marcas de lápiz encapsulan una región más grande que la que se ve oscurecida por el yodo. Esto se debe a que la acetofenona es muy fuertemente activa con la luz ultravioleta, pero sólo ligeramente compleja con el yodo. No es infrecuente que una técnica visualice un compuesto más eficazmente que otra.
Por lo tanto, es importante ser prudente al utilizar la cromatografía en capa delgada para interpretar la cantidad de material presente en una muestra, por ejemplo, al evaluar la cantidad de una impureza (como en el carril Nº 3 de la figura 2, que contiene cinamaldehido y su impureza ácido cinámico). Es probable que una mancha grande esté presente en mayor cantidad que una mancha pequeña, pero también podría ser que la mancha grande responda mejor a la técnica de visualización.

La tinción no tiene sentido
Ciertos métodos de visualización funcionan mejor para ciertos grupos funcionales, por lo que un resultado positivo con una mancha puede dar pistas sobre la identidad de una mancha desconocida. Sin embargo, a veces un compuesto se tiñe cuando no se «supone», y esto puede ser confuso.
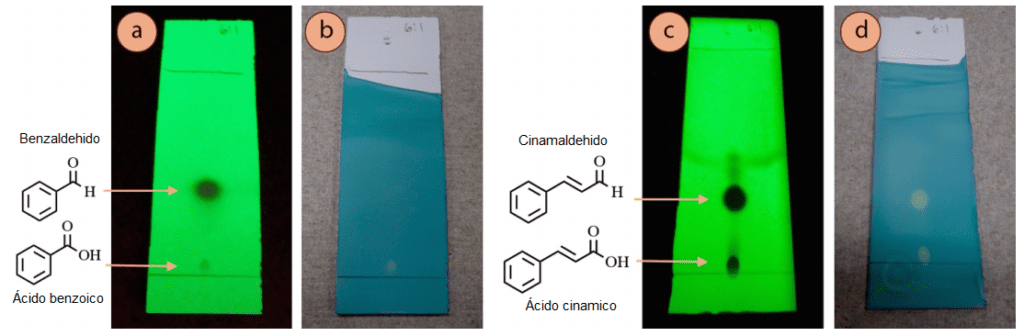
Por ejemplo, un revelado de cromatografía TLC de benzaldehído visualizada con luz ultravioleta (Figura 4a) muestra dos manchas, y basado en el Rf relativo tendría sentido que la mancha oscura sea de benzaldehído y la más débil cerca de la línea de base sea de ácido benzoico (causado por una oxidación de benzaldehído).
La tinción de la placa con verde de bromocresol (una tinción para compuestos ácidos), apoya esta hipótesis ya que la mancha ácida inferior se visualiza con este método (Figura 4b). Este es un ejemplo de cuando los resultados de la tinción «tienen sentido estructural», y pueden incluso apoyar la identificación de manchas desconocidas.
Sin embargo, en un experimento similar con el cinamaldehido, tanto las manchas de aldehído como las de ácido carboxílico se visualizaron fuertemente con el verde de bromocresol (Figura 4d), aunque sólo una es un compuesto ácido. Este resultado no «tiene sentido» en un principio, y sólo se pueden postular teorías sobre por qué el aldehído reaccionó con la mancha.
La importancia de la figura 4 es que la interpretación de la tinción o la falta de tinción puede utilizarse a veces para inferir la estructura, pero puede haber excepciones difíciles de explicar.
Para más información Visualizing TLC Plates