Introducción a la cromatografía
Tiempo de lectura estimado: 6 minutos
La cromatografía es una técnica utilizada para separar los componentes de una mezcla. Puede utilizarse como técnica analítica para obtener información sobre lo que está presente en una mezcla, o como técnica de purificación para separar y recoger los componentes de una mezcla. La cromatografía en el laboratorio de química puede clasificarse en varias categorías amplias:
- Cromatografía en capa delgada (Thin layer cromatography – TLC) – Método analítico para el análisis de mezclas.
- Cromatografía en columna – Método de purificación para la separación y recolección de componentes.
- Cromatografía de gases – Técnica instrumental para el análisis de mezclas
Estas técnicas siguen los mismos principios generales en cuanto a la forma en que son capaces de separar las mezclas, que se examinarán colectivamente a continuación. Los detalles específicos de cada técnica se examinarán en las siguientes secciones.
Principios de la cromatografía
Los primeros usos de la cromatografía implicaron la separación de los componentes coloreados de las plantas a principios de 1900. Los pigmentos de una planta pueden ser separados en colores amarillo, naranja y verde (xantófilas, carotenos y clorofilas respectivamente) a través de este método. El nombre griego para el color es chroma, y grafina es «escribir», así que la cromatografía puede ser comprendido como «escritura en color».
La idea general de la cromatografía puede demostrarse con los colorantes alimentarios en su cocina. El colorante comercial verde para alimentos no contiene ningún componente de color verde en absoluto, y la cromatografía puede mostrar que el colorante verde para alimentos es en realidad una mezcla de colorantes azules y amarillos.
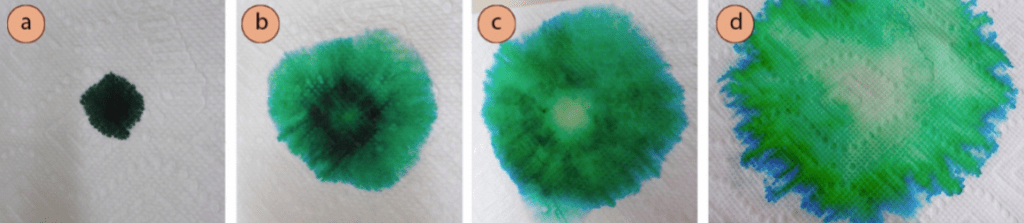
Si se coloca una gota de colorante alimentario verde en el centro de una toalla de papel seguida de unas pocas gotas de agua, el agua se arrastrará hacia afuera mientras moja el papel (Figura 1). A medida que el agua se expande, el tinte viajará con ella. Si dejas que el tinte se expanda lo suficiente, verás que los bordes se teñirán de azul (Figura 1d). Este es el comienzo de la separación de los componentes azul y amarillo en el tinte verde por el papel y el agua.
Cromatografía de papel
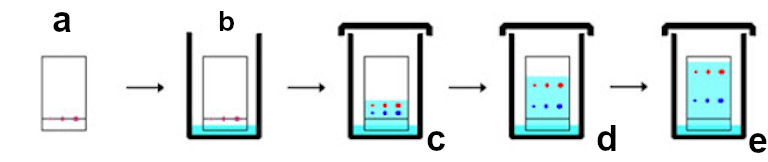
Una separación completa del colorante alimentario verde puede lograrse mediante la cromatografía de papel. Se deposita una muestra diluida en el borde inferior de un trozo de papel, se enrolla el papel en un cilindro, se grapa y se coloca verticalmente en un recipiente cerrado que contiene una pequeña cantidad de disolvente* (Fig. 2a). Se deja que el disolvente absorba el papel por acción capilar (llamada «elución», Fig. 2b), y mediante este método se puede lograr una separación completa de los componentes azul y amarillo (Fig. 2d).

* El disolvente utilizado en esta separación es una solución hecha de una relación de volumen de 1:3:1 de NH4OH 6M:1-pentanol:etanol.
Teoría general de la cromatografía
Las principales técnicas cromatográficas (cromatografía en capa fina, cromatografía en columna y cromatografía de gases) siguen los mismos principios generales en cuanto a la forma en que son capaces de separar las mezclas.
En todos los métodos cromatográficos, una muestra se aplica primero sobre un material estacionario que absorbe o adsorbe la muestra: la adsorción es cuando las moléculas o los iones de una muestra se adhieren a una superficie, mientras que la absorción es cuando las partículas de la muestra penetran en el interior de otro material.
Una toalla de papel absorbe agua porque las moléculas de agua forman fuerzas intermoleculares (en este caso el hidrógeno se une) con la celulosa de la toalla de papel. En la cromatografía, una muestra se adsorbe típicamente a una superficie, y puede formar una variedad de fuerzas intermoleculares con esta superficie.
Después de la adsorción, la muestra se expone a un líquido o gas que viaja en una dirección. La muestra puede superar sus fuerzas intermoleculares con la superficie estacionaria y transferirse al material en movimiento, debido a alguna atracción o suficiente energía térmica. La muestra más tarde se readaptará al material estacionario, y la transición entre los dos materiales en un equilibrio constante (Ecuación 1). Para que haya alguna separación entre los componentes de una mezcla, es fundamental que haya muchos «pasos» de equilibrio en el proceso
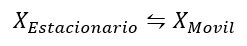
El material en el que se adsorbe la muestra se denomina «fase estacionaria» porque conserva la posición de la muestra. El material en movimiento se denomina «fase móvil» porque puede hacer que la muestra se mueva de su posición original.
Interacción fase móvil – fase estacionaria
El principio fundamental que permite a la cromatografía separar los componentes de una mezcla es que los componentes pasarán diferentes cantidades de tiempo interactuando con las fases estacionaria y móvil. Un compuesto que pasa una gran cantidad de tiempo móvil se alejará rápidamente de su ubicación original, y se separará de un compuesto que pasa una mayor cantidad de tiempo estacionario.
El mecanismo fundamental que determina la cantidad de tiempo que se pasa en las fases es la fuerza de las fuerzas intermoleculares experimentadas en cada fase. Si un compuesto tiene fuertes fuerzas intermoleculares con la fase estacionaria, permanecerá adsorbido durante un mayor tiempo que un compuesto que tiene fuerzas intermoleculares más débiles. Esto hace que los compuestos con diferentes fuerzas intermoleculares se muevan a diferentes velocidades.
La forma en que estas ideas generales se aplican a cada técnica cromatográfica (cromatografía en capa fina, cromatografía en columna y cromatografía de gases) se explicará con mayor detalle en cada técnica.
Para más información 2.0: Prelude to Chromatography



