Tiempo de lectura estimado: 13 minutos
Como otras técnicas cromatográficas, la cromatografía de capa delgada (TLC) depende del principio de separación y de su correcto procedimiento. La separación se basa en la afinidad relativa de los compuestos hacia ambas fases. Los compuestos de la fase móvil se mueven sobre la superficie de la fase estacionaria.
El movimiento se produce de tal manera que los compuestos que tienen una mayor afinidad con la fase estacionaria se mueven lentamente mientras que los otros compuestos se desplazan rápidamente. Por lo tanto, se logra la separación de la mezcla. Una vez completado el proceso de separación, los componentes individuales de la mezcla aparecen como manchas en los niveles respectivos de las placas. Su carácter y naturaleza se identifican mediante técnicas de detección adecuadas.
Procedimiento general de una Cromatografía en capa delgada (TLC)
La cromatografía en capa delgada o TLC ilustrada a continuación muestra la elución de una placa de TLC que contiene varias muestras de colorante alimentario rojo a diferentes diluciones acuosas (0 = sin diluir, 3 = 1 gota de colorante + 3 gotas de agua, etc.).

Tiempo necesario: 3 horas
Paso a paso de una cromatografía en capa delgada o TLC
- Disolver las muestras
Disuelva todas las muestras que desee analizar (sólidas y líquidas) en pequeños frascos utilizando un disolvente volátil en el que sean solubles (por ejemplo, acetona, éter dietílico o diclorometano). Lo ideal sería que los viales tuvieran una tapa para reducir al mínimo los vapores y preservar las muestras si se voltean (figura 2a).
La concentración óptima para la cromatografía en capa fina se suele determinar empíricamente, pero un buen punto de partida es utilizar entre 50 y 100 veces más disolvente que la muestra (por ejemplo, una gota de muestra para ∼1mL solvente). Si ya se ha preparado una muestra de RMN (∼5mg/0,75mL para RMN de campo alto), se puede utilizar esa muestra directamente.
Etiquetar los viales. Prepare también un vial de acetona limpia (u otro disolvente, por ejemplo, CH2Cl2) que se utilizará para enjuagar los sembradores en un paso posterior. (Un vial de agua para enjuagar se muestra en la figura 2a, ya que las soluciones de colorante son solubles en agua).
- Preparación de la cámara y la placa de TLC
Tomar una cámara de TLC con tapa. Se puede hacer una cámara económica usando un vaso de precipitados y un vidrio de reloj (Figura 2b). Corte un trozo de papel de filtro (o dos) para que cuando se coloque en la cámara, el papel de filtro encaje dentro de la cámara y sea plano en el fondo, pero sin oscurecer la vista del interior (Figura 2c).
El papel filtro mantiene la cámara saturada de vapores, de manera que cuando el eluyente sube a la placa no se evapora fácilmente, sino que sigue subiendo y se somete a la cromatografía. Si el eluyente se evaporara, el movimiento se detendría, pero también podría cambiar la composición local de un eluyente mezclado y afectar los resultados.Anuncio Añada una porción de un disolvente preparado para la cromatografía (Figura 2c, 5 -10mL para este tipo de cámara de TLC). Cierre la tapa (o coloque el vidrio de reloj) e incline la cámara para humedecer el papel de filtro.
Insertar una placa de TLC, tocando la placa sólo en la parte posterior o en los bordes, pero no en la superficie blanca. Utilice una regla para dibujar ligeramente una línea recta con un lápiz (el grafito no será eluido por el solvente, pero un marcador sí) aproximadamente a 1 cm del fondo. No dañe la superficie de la sílice o la alúmina.
Etiquete con lápiz las áreas donde planea colocar las muestras (Figura 2d). Una placa de TLC de una pulgada de ancho puede acomodar cómodamente tres muestras (tiene tres carriles), y si el tamaño del punto se mantiene pequeño puede caber en un máximo de cinco puntos. Si se necesitan más de cinco puntos en una placa, las placas de TLC se pueden comprar en hojas y cortarse de más de una pulgada de ancho.
Los carriles no deben colocarse demasiado cerca del borde (mantener al menos 5mm de distancia de cada borde), ya que no es raro que el disolvente viaje ligeramente «rápido» por el borde donde la acción capilar del disolvente es mayor (Figura 3).
Tampoco deben colocarse demasiado cerca unos de otros, ya que los puntos pueden superponerse después de la elución. Un punto es siempre más grande después de la elución en comparación con su tamaño original (Figura 3 b+c) porque la difusión se produce en todas las direcciones (el contacto con un líquido propaga el material tanto en la dirección horizontal como en la vertical). La ampliación también se produce cuando los solutos en la fase móvil se mueven a diferentes velocidades, ya que el flujo de eluyente es más débil cerca de la superficie de adsorción.
Esto puede incluso a veces causar que los compuestos se atasquen en los poros adsorbentes donde el flujo de eluyente es especialmente débil.4. El ensanchamiento puntual significa que las muestras depositadas una al lado de la otra en la línea base de una placa de TLC probablemente se desangrarán juntas durante la elución.
- Siembra de la placa de TLC con la muestra
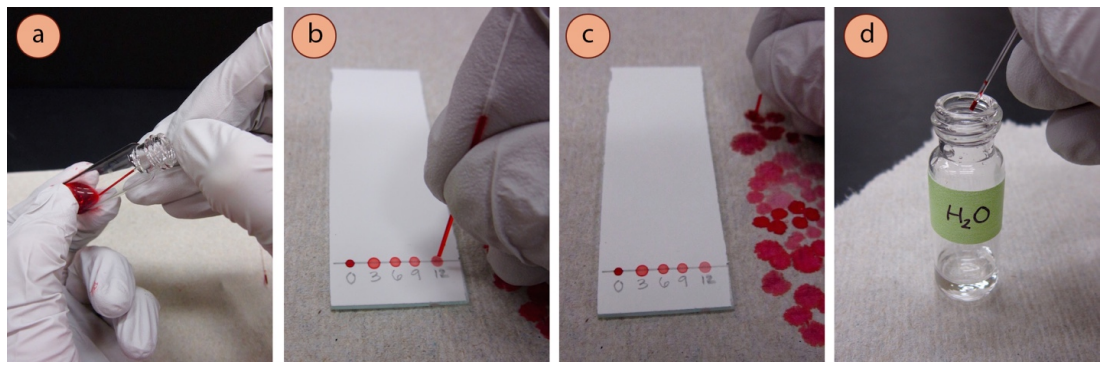
Obtener un sembrador capilar (un trozo de vidrio hueco muy delgado abierto en ambos extremos). En algunas instituciones, es posible que tenga que hacer su propio sembrador estirando una pipeta ablandada. Coloque su sembrador en la muestra diluida que desea analizar para retirar el líquido en el sembrador a través de la acción capilar. Si el nivel de líquido es bajo en su vial y su sembrador corto, puede que tenga que inclinar el vial para retirar el líquido (Figura 4a).
 Anuncio
Anuncio Manteniendo el sembrador mayormente vertical, haga un «spot» o punto de siembra de práctica en una toalla de papel o en un pedazo de sílice o alúmina de desecho para familiarizarse con la forma en que el líquido sale del sembrador. Las manchas deben ser muy pequeñas, alrededor de 2 mm en diámetro. Coloque un punto muy pequeño de material en la línea de lápiz del carril apropiado (Figura 4b) usando un rápido movimiento de «arriba y abajo» con su mano. No raye la sílice o la alúmina con el sembrador.
Manteniendo el sembrador en posición vertical, toque inmediatamente el sembrador con una toalla de papel para eliminar todo el líquido que quede en el sembrador (Figura 4c). Si el sembrador se coloca en el suelo sin drenar inmediatamente el líquido, puede entrar aire en el sembrador, lo que hace imposible dispensarlo y utilizarlo de nuevo.
Enjuague el sembrador con acetona (u otro disolvente volátil con el que sus compuestos sean solubles, Figura 4d). Coloque el sembrador vacío en su vial de enjuague para extraer el líquido y drene el disolvente en una toalla de papel. Enjuague una o dos veces antes de reutilizar el sembrador para otras muestras.
- Colocar la placa de TLC en la cámara para «eluir»
Utilice unas pinzas para colocar delicadamente la placa de TLC en la cámara (Figura 5a). No permita que el líquido salpique sobre la placa.
El nivel de líquido debe estar por debajo de la línea del lápiz donde las muestras están manchadas o los compuestos se disolverán en el charco de eluyente en lugar de subir por la placa. Tapar la cámara con delicadeza mientras se mantiene vertical, y no volver a tocarla hasta que la cromatografía esté completa. Anuncio
Anuncio Permita que la cromatografía en capa delgada se desarrolle (Figura 5b-d). A medida que el líquido suba por la placa de TLC aparecerá transparente y húmedo. Un fondo oscuro permitirá que el frente del disolvente se vea más fácilmente. Si el eluyente es muy polar (por ejemplo, contiene grandes cantidades de etanol o agua), la elución llevará un tiempo relativamente largo (puede ser de 30-40 minutos). Si el eluyente es muy no polar (por ejemplo, contiene grandes cantidades de hexano o éter de petróleo), la elución será relativamente rápida (puede ser de 2 a 5 minutos para una placa de unos 10 cm de alto).
Dependiendo de los objetivos del experimento de TLC, la cromatografía puede ser detenida cuando el nivel de disolvente se encuentra entre la mitad y aproximadamente 0,5 cm. de la parte superior del plato. Lo mejor es dejar que la TLC corra hasta unos 0,5 cm de la parte superior de la placa para obtener la mejor separación de los puntos y para minimizar el error en los cálculos de Rf.
- Retirar la placa de TLC de la cámara
Abra la cámara de TLC y retire la placa de cromatografía con pinzas. Marque inmediatamente la línea del disolvente con un lápiz (Figura 5e) para permitir un cálculo de Rf, ya que a menudo el disolvente se evapora fácilmente. Alternativamente, la sílice puede ser ligeramente raspada con las pinzas para marcar el frente del disolvente.
Si los compuestos de la placa de TLC están coloreados, el proceso está completo. Si los compuestos son incoloros, necesitan ser visualizados o revelados a continuación.
Anuncio
Solución de problemas de TLC
Las manchas son rayadas o » borrosas»
Los componentes de una muestra pueden aparecer como largas rayas o manchas » borrosas » en una placa de TLC si las muestras se ejecutan a una concentración demasiado alta.
Por ejemplo, la figura 6b muestra una placa de TLC eluida que contiene cinco muestras de colorante alimentario rojo de diferentes concentraciones (el carril 0 contiene el colorante en la concentración que se encuentra en la tienda de comestibles; el carril 3 contiene 1 gota de colorante diluido con 3 gotas de agua, etc.). Después de la elución, los componentes rojos y rosados del colorante sin diluir (carril 0) se rayaron severamente, ya que la placa de TLC estaba «sobrecargada». Cuando esto ocurre no se produce el equilibrio adecuado entre las fases estacionaria y móvil. Con una mayor dilución (carril 12), las rayas desaparecieron y las formas de las manchas se agudizaron.
Si se ven rayas en una placa de TLC, la muestra debe diluirse y volverse a correr.

La figura 6c también demuestra cómo la dilución puede mejorar la forma de una mancha después de la elución. En esta TLC, las muestras de alquenos y alquinos se mancharon a concentraciones algo altas, mientras que en la Figura 6d se utilizó una dilución mejorada. Obsérvese cómo el Rf parece cambiar en las dos placas de cromatografía. El Rf más exacto es el de la muestra diluida. La ejecución de la cromatografía de capa delgada en muestras concentradas da valores Rf inexactos y puede ocultar múltiples manchas.
Las manchas corren de manera desigual
A veces el frente del disolvente puede funcionar de forma desigual en una placa de TLC. Esto puede ocurrir si la placa se colocó en la cámara con una ligera inclinación, si el eluyente salpicó sobre la placa durante la colocación en la cámara, o si la cámara se empujó durante la elución. En los casos en que el frente es dramáticamente diferente de una posición a otra, el frente debe ser medido para cada carril de la placa (si se calcula un Rf) en lugar de sólo una vez.
Haciendo Capilares sembradores para cromatografía
Aunque se pueden comprar sembradores capilares para cromatografía en capa delgada, algunos químicos prefieren crear los suyos propios estirando pipetas Pasteur (Figura 7). Para hacer un sembrador, sostenga una pipeta por los bordes mientras usa guantes gruesos y coloque el centro de la pipeta en la llama de un gran quemador Meker (Figura 7a). Caliente la pipeta hasta que el vidrio se vuelva bastante flexible (el vidrio de borosilicato se ablanda a 820°C, por lo que esto llevará algún tiempo). Sólo rote, pero no estire la pipeta en absoluto mientras la pipeta esté en la llama. A continuación, retire la pipeta de la llama e inmediata y rápidamente tire de la pipeta a la distancia de un brazo. Las secciones delgadas pueden romperse en segmentos de 6 a 12 pulgadas y usarse para TLC.

Figura 7: a) Calentando una pipeta en un quemador Meker, b+c) Estirando la pipeta.
Registro de los TLC
Algunos químicos escanean, fotografían o registran electrónicamente sus placas de TLC reveladas, pero es mucho más común copiar a mano un esquema de una placa de cromatografía en un cuaderno de laboratorio. Es importante copiar una placa de TLC «a escala», lo que significa que las dimensiones deben ser las mismas en el cuaderno que en la realidad.
Para ello, la placa de TLC se puede colocar sobre la página de un cuaderno y crear una representación al lado. La parte posterior de la placa de TLC debe ser previamente limpiada o de lo contrario los reactivos de revelado o solventes pueden degradar el papel. Es importante copiar la placa de TLC con la mayor precisión posible, dibujando las manchas exactamente como aparecen, incluso si son rayadas o con manchas. Todas las manchas que se vean en un carril deben ser registradas, incluso si son débiles. Un buen registro significa registrar todas las observaciones, incluso si se desconoce su importancia; un punto débil e inesperado puede ser relevante en un momento posterior.
Varias otras anotaciones deben hacerse junto con el boceto de la placa de TLC. Se debe registrar el sistema de disolventes y la identidad de lo que se ha visto en cada carril. Para cada mancha se debe calcular un Rf (algunos químicos gustan de escribir las medidas en la placa de TLC) junto con la anotación de la actividad UV y el color de la mancha. Si una mancha cambia de aspecto con el tiempo, como por ejemplo una mancha naranja que se desvanece a verde claro con el tiempo, debe registrarse el aspecto inicial.
Para más información 2.2E: Step-by-Step Procedures for Thin Layer Chromatography