Química de los alquinos
Tiempo de lectura estimado: 4 minutos
En química orgánica, un alquino es un hidrocarburo insaturado que contiene al menos un triple enlace carbono-carbono. Los alquinos acíclicos más simples con un solo triple enlace y sin otros grupos funcionales forman una serie homóloga con la fórmula química general CnH2n-2. Los alquinos se conocen tradicionalmente como acetilenos, aunque el nombre acetileno también se refiere específicamente al C2H2, conocido formalmente como eteno según la nomenclatura IUPAC. Al igual que otros hidrocarburos, los alquinos son generalmente hidrofóbicos.
Los alquinos son hidrocarburos en los que el carbono está hibridado sp. Entre dos átomos de carbono hay un doble enlace formado por un enlace de tipo σ y dos enlaces π debido a la superposición de los orbitales p no hibridados de los dos átomos de carbono implicados en el enlace.
En el acetileno, los ángulos de enlace H-C≡C son de 180°. En virtud de este ángulo de enlace, los alquinos tienen forma de barra. En consecuencia, los alquinos cíclicos son raros. La bencina no puede aislarse. La distancia de enlace C≡C de 121 picómetros es mucho más corta que la distancia C=C de los alquenos (134 pm) o el enlace C-C de los alcanos (153 pm).
Materiales
- Capsula de porcelana
- Soporte para tubos de ensayo
- 2 tubos de ensayo
- Tubo de vidrio doblado en U
- Tapones de goma
Reactivos
- Carburo de calcio
- Agua de bromo
- Fenolftaleína 1 % sol.
Procedimiento
Primera parte: preparación de acetileno a partir de carburo de calcio:
Llene una cápsula de porcelana (u otro recipiente similar) con agua hasta 2 cm del borde y deje caer en ella un pequeño trozo, de unos 2 o 3 g de carburo de calcio. Inmediatamente se observa un fuerte desarrollo de acetileno según la reacción:
La formación de un ligero precipitado blanquecino en el agua de la cápsula y su comportamiento básico, verificable con fenolftaleína, identifican con certeza la formación de hidróxido de calcio.
Acercando una llama al acetileno en formación se produce un encendido inmediato del mismo, con una llama poco brillante y que deja residuos de hollín.
La reacción de combustión es típica de los hidrocarburos:
Segunda parte: adición de bromo al acetileno (etileno):
Disponer en un soporte dos tubos de ensayo. En uno se ponen 2 ó 3 mL de agua saturada de bromo y unos 10 mL de agua destilada; en el otro, para generar el acetileno, se vierten unos 10 mL de agua y se deja caer unos 1 g de carburo de calcio y se cierra rápidamente con el tapón del tubo revelador. El mismo tubo revelador se introduce en el primer tubo de ensayo para burbujear el gas. En definitiva, se observa una decoloración completa del agua de bromo, lo que indica que la reacción de halogenación ha tenido lugar.
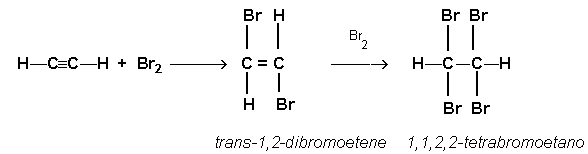
Esta reacción se produce en dos etapas:
Después del laboratorio
Investigar diferentes métodos de síntesis de alquinos.
Recomendaciones de seguridad
En todo momento se deben utilizar los elementos de seguridad básicos en el laboratorio de química (bata de laboratorio, guantes, gafas de seguridad y demás que sean exigidos por las normas internas, locales o nacionales. Los residuos generados por la práctica deben ser dispuestos de manera adecuada según las normas de laboratorio y las normas locales y nacionales respectivas.
Para más información Preparation of Alkynes