Estequiometria en soluciones – reactivo limite
Tiempo de lectura estimado: 5 minutos
La estequiometría es el cálculo de los reactivos y productos en las reacciones químicas, se fundamenta en la ley de conservación de las masas que establece que la masa total de los reactivos es igual a la masa total de los productos, relacionadas a través de números enteros positivos, llamados coeficientes estequiométricos.
¿Que es la estequiometria?
Los cálculos de estequiometria en soluciones son de vital importancia ya que muchos compuestos son manejados en solución, al igual que muchas reacciones suceden en un solvente.
La estequiometría permite calcular la masa de los productos si se conoce la masa total de los reactivos, igualmente, si se conocen las masas de los productos es posible calcular la masa inicial de los reactivos y así sucesivamente.
Cuando uno de los reactivos se encuentra en menor cantidad que la necesaria para completar la reacción con los demás reactivos, este reactivo limitará la cantidad de producto generado en la reacción y recibe el nombre de reactivo limite. Por su parte, si un reactivo no se agota en la reacción química (parte de su masa queda sin reaccionar) se le llama reactivo en exceso.
Estequiometría en solución
El termino estequiometría fue empleado por primera vez por el químico alemán Jeremias Benjamin Richter en 1792 en el primer volumen de Richter’s Stoichiometry or the Art of Measuring the Chemical Elements. El termino se deriva que las palabras griegas stoicheion que significa elemento y metron, que significa medida.
Una cantidad estequiométrica, o relación estequiométrica de un reactivo es la cantidad optima que, asumiendo que la reacción es completa, hace que todo el reactivo sea consumido, que no haya deficiencia de reactivo y no exista exceso de este.
Los cálculos relacionados con la estequiometría son de suma importancia en la ciencia y la ingeniería, ya que permiten determinar la cantidad a producirse en una reacción determinada y la cantidad de reactivos necesarios para sintetizar un producto específico.
Materiales
- 2 Pipetas graduadas de 10 mL
- 2 propipetas o pipeteadores
- Gradilla
- 16 tubos de ensayo
Reactivos
- Solución de nitrato de plomo (Pb(N03)2) 0.25 M
- Solución de carbonato de sodio (Na2C03) 0.25 M
Procedimiento
Tiempo necesario: 1 hora y 30 minutos
Laboratorio – Estequiometria en soluciones
-
Tomar 8 tubos de ensayo y marcarlos con números del 1 al 8 y Pb(N03)2, después tomar otros tubos de ensayo y marcarlos con números del 1 al 8 y Na2C03. Empleando las pipetas de 10 mL y las propipetas, servir las soluciones de nitrato de plomo y carbonato de sodio según la siguiente tabla (tener cuidado de no contaminar cada pipeta con la otra solución).
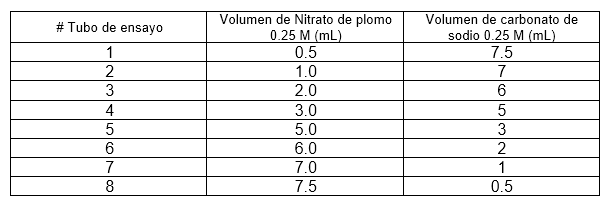
-
Mezclar los contenidos de los tubos, según la numeración (tubo 1 de Pb(N03)2 con tubo 1 de Na2C03 etc.) Verter siempre el volumen mayor en el menor. Después de mezclar agitar unos segundos el tubo, sin colocar el dedo en la boca del tubo Dejar reposar los tubos de ensayo por espacio de 10 minutos.
Anuncio -
Luego de los diez minutos se observará la generación de un precipitado blanco de carbonato de plomo. Medir la altura del precipitado de carbonato de plomo PbCO3 en cada tubo con la ayuda de una regla. Registrar esta altura en mm.
Después del experimento
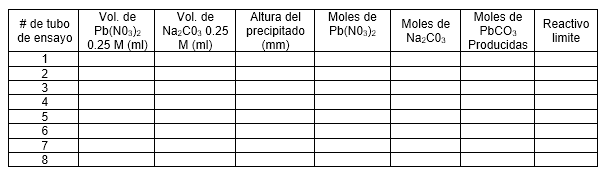
Completar la siguiente tabla con los datos obtenidos en la práctica y resultantes de los cálculos estequiométricos realizados con las cantidades de las soluciones de trabajo en cada tubo de ensayo.
Determinar cuál de las dos soluciones es el reactivo limite en cada pareja de tubos. Graficar en un mismo plano la cantidad de moles de nitrato de plomo, de carbonato de sodio y de carbonato de plomo y la altura del precipitado versus el número de tubo. ¿Cómo influye la cantidad de moles de cada reactivo con respecto a la altura del precipitado? ¿Cómo se relacionan las cantidades de moles de cada reactivo y del producto en el máximo de altura del precipitado?
Graficar altura del precipitado versus número de moles de carbonato de plomo producido ¿Cómo es la relación entre estas dos variables?
Recomendaciones de seguridad
En todo momento se deben utilizar los elementos de seguridad básicos en el laboratorio de química (bata de laboratorio, guantes, gafas de seguridad y demás que sean exigidos por las normas internas, locales o nacionales. Los residuos generados por la práctica deben ser dispuestos de manera adecuada según las normas de laboratorio y las normas locales y nacionales respectivas.
Para más información Overall equations for precipitation reactions