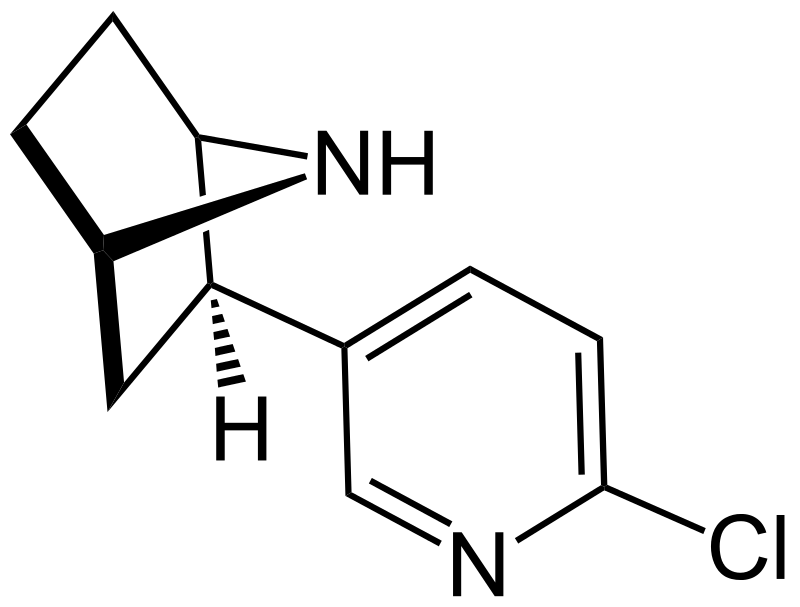
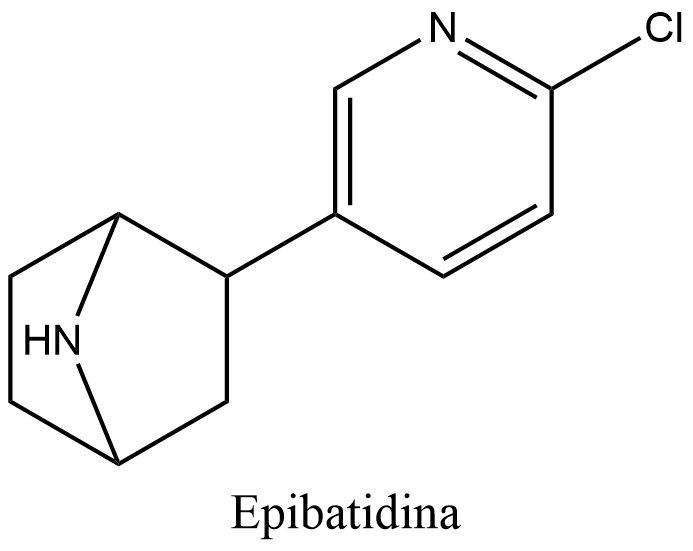
Epibatidina
Tiempo de lectura estimado: 9 minutos
La epibatidina es un alcaloide clorado que segrega la rana ecuatoriana Epipedobates anthonyi y las ranas de dardo venenosas del género Ameerega. Fue descubierta por John W. Daly en 1974, pero su estructura no fue totalmente dilucidada hasta 1992.
Sigue siendo controvertido si la epibatidina es el primer ejemplo observado de un alcaloide clorado, debido a las dificultades para identificar de manera concluyente el compuesto a partir de las limitadas muestras recogidas por Daly. Cuando se utilizó la espectrometría de alta resolución en 1991, quedaba menos de un miligramo de extracto de las muestras de Daly, lo que suscitaba preocupación por la posible contaminación. Las muestras de otros lotes de la misma especie de rana no produjeron epibatidina.
La epibatidina es tóxica. Su toxicidad se debe a su capacidad de interactuar con los receptores nicotínicos y muscarínicos de la acetilcolina. Estos receptores están involucrados en la transmisión de sensaciones dolorosas y en el movimiento, entre otras funciones. La epibatidina causa entonces entumecimiento y, eventualmente, parálisis. Las dosis son letales cuando la parálisis causa un paro respiratorio. Originalmente, se pensó que la epibatidina podría ser útil como droga. Sin embargo, debido a su inaceptable índice terapéutico, ya no se está investigando para posibles usos terapéuticos.
Historia
La epibatidina fue descubierta por John W. Daly en 1974. Fue aislada de la piel de las ranas Epipdobates anthonyi recolectadas por Daly y su colega, Charles Myers. Entre 1974 y 1979, Daly y Myers recolectaron las pieles de casi 3000 ranas de varios sitios en el Ecuador, después de encontrar que una pequeña inyección de una preparación de su piel causaba efectos analgésicos (dolorosos) en ratones que se parecían a los de un opiáceo.
A pesar de que su nombre común – la rana Flecha Venenosa de Anthony – sugiere que fue utilizada por los nativos cuando cazaban, un documento escrito por Daly en el año 2000 afirmaba que no había folclore local o medicina popular alrededor de las ranas y que eran consideradas en gran medida sin importancia por los locales.
La estructura de la epibatidina fue dilucidada en 1992, esfuerzo que se vio obstaculizado por el hecho de que la E. anthonyi obtuviera el estatus de protección de la UICN en 1984. Además, estas ranas no producen la toxina cuando se crían y se ponen en cautiverio, porque no sintetizan la epibatidina por sí mismas. Como otras ranas de dardo venenosas, en su lugar la obtienen a través de su dieta y luego la almacenan en su piel. Las fuentes dietéticas más probables son escarabajos, hormigas, ácaros y moscas. Superando las dificultades, la estructura fue finalmente determinada, y la primera síntesis de epibatidina fue completada en 1993. Desde entonces se han desarrollado muchos otros métodos de síntesis.
Debido a su efecto analgésico, hubo un intenso interés en el uso de la epibatidina como droga, porque se descubrió que no era un opiáceo, lo que significaba que podía utilizarse potencialmente sin temor a la adicción. Sin embargo, pronto se descubrió que no se puede usar en humanos porque la dosis que produce síntomas tóxicos es demasiado baja para que sea segura.
Estructura química
La epibatidina es una piridina con una estructura similar a la de la nicotina. Es una sustancia aceitosa higroscópica que es una base.
Síntesis total
Se han ideado varias rutas de síntesis total debido a la relativa escasez de epibatidina en la naturaleza.
Tras el descubrimiento de la estructura de la epibatidina, se han ideado más de cincuenta formas de sintetizarla en el laboratorio. En el primer ejemplo notificado, un procedimiento de nueve pasos produce la sustancia como un racemato (en cambio, el compuesto que se produce naturalmente es el (+)-enantiómero; el (-)-enantiómero no se produce naturalmente).
Posteriormente se determinó que los enantiómeros (+) y (-) tenían efectos analgésicos y tóxicos equivalentes. El proceso ha demostrado ser bastante productivo, con un rendimiento de alrededor del 40%.
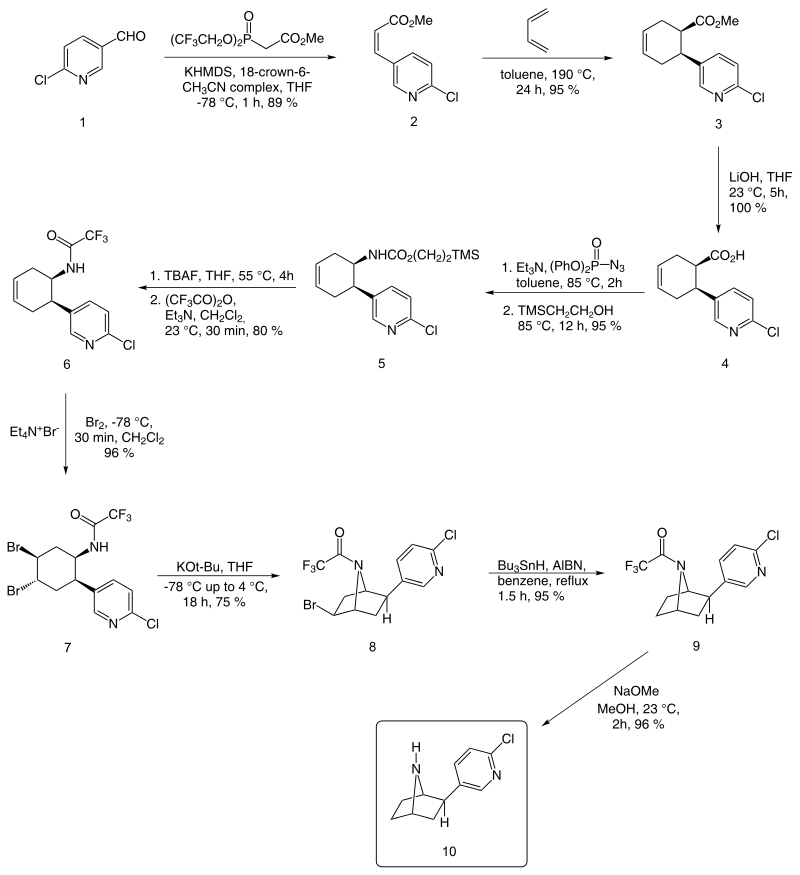
A continuación, se describe una síntesis enantioselectiva comunicada por E J Corey a partir del cloronicotinaldehído:
Además del método de Corey, otros métodos notables son los de Broka, Huang & Shen, y Clayton & Regan.
Análogos sintéticos
Se han intentado varios enfoques para descubrir análogos estructurales de la epibatidina que mantengan los efectos analgésicos, pero sin la toxicidad. Por ejemplo, Abbott Laboratories ha producido derivados de la epibatidina, incluido el ABT-594. Otros análogos de la epibatidina incluyen el ABT-418, la epiboxidina y sus derivados. En 1999 se publicó una síntesis de la epibatidina, utilizando una hidroxilación microbiana de un carbono no activado en un 7-azanorbornano.
Mecanismo de acción
La epibatidina tiene dos mecanismos de acción: puede unirse a los receptores de acetilcolina nicotínica (nAChR) o a los receptores de acetilcolina muscarínica (mAChR). Concretamente, se cree que la propiedad analgésica de la epibatidina se produce por su unión al subtipo α4/β2 de receptores nicotínicos. La epibatidina también se une al subtipo α3/β4 y, en mucho menor medida, a los receptores α7 (afinidad 300 veces menor que para α4/β2). El orden de clasificación de las afinidades es αε > αγ > αδ.
Los receptores de acetilcolina nicotínica se encuentran en las membranas post-sinápticas de las células nerviosas. Propagan la neurotransmisión en el sistema nervioso central y periférico. Cuando los neurotransmisores se unen a estos receptores, los canales de iones se abren, permitiendo que los iones Na+ y Ca2+ se muevan a través de la membrana.
Esto despolariza la membrana post-sináptica, induciendo un potencial de acción que propaga la señal. Esta señal finalmente inducirá la liberación de dopamina y norepinefrina, resultando en un efecto antinociceptivo en el organismo. El neurotransmisor habitual para el nAChR es la acetilcolina. Sin embargo, otras sustancias (como la epibatidina y la nicotina) también son capaces de unirse al receptor e inducir una respuesta similar, si no idéntica. La epibatidina tiene una afinidad extremadamente alta por los nAChR, dependiendo del subtipo de receptor, desde 0,05 nM en el subtipo α4β2 hasta 22 nM en el subtipo α7. Tanto la afinidad como la eficacia (y por lo tanto también la potencia) son mucho mayores que para la nicotina.
La propiedad paralizante de la epibatidina tiene lugar después de su unión a los receptores nicotínicos de tipo muscular.
Las dosis bajas de epibatidina sólo afectarán a los nAChRs, debido a una mayor afinidad con los nAChRs que con los mAChRs. Sin embargo, dosis más altas harán que la epibatidina se una a los mAChRs.
Ambos (+)- y (-)-enantiómeros de la epibatidina son biológicamente activos, y ambos tienen afinidades de unión similares a los nAChRs. Sólo el (+)-enantiómero no induce tolerancia. Si bien esto puede ser una ventaja terapéutica potencial sobre la morfina, la epibatidina no ha entrado en los ensayos clínicos porque incluso las dosis muy pequeñas son letales para los roedores.
Sintomas de envenamiento por epibatidina
La epibatidina tiene varias consecuencias tóxicas. Los efectos empíricamente probados incluyen la descarga del nervio simpático esplánico y el aumento de la presión arterial. Los efectos de la descarga del nervio pueden causar antinocicepción parcialmente mediada por el agonismo de los receptores centrales de acetilcolina nicotínica en dosis bajas de epibatidina; 5 µg/kg.
Sin embargo, en dosis más altas, la epibatidina causará parálisis y pérdida de conciencia, coma y eventualmente la muerte. La dosis letal media (DL50) de epibatidina se sitúa entre 1,46 µg/kg y 13,98 µg/kg.[26] Esto hace que la epibatidina sea algo más tóxica que la dioxina (con una DL50 media de 22,8 µg/kg). Debido a la pequeña diferencia entre su concentración tóxica y la concentración antinociceptiva, sus usos terapéuticos son muy limitados.
En la investigación en ratones, la administración de dosis superiores a 5 μg/kg de epibatidina causó un efecto paralizante dependiente de la dosis en el organismo. Con dosis superiores a 5 μg/kg, los síntomas incluían hipertensión (aumento de la presión sanguínea), parálisis en el sistema respiratorio, convulsiones y, en última instancia, la muerte. Sin embargo, los síntomas cambian drásticamente cuando se administran dosis más bajas. Los ratones se volvieron resistentes al dolor y al calor sin ninguno de los efectos negativos de las dosis más altas.
Posibles usos médicos
La epibatidina tiene una alta potencia analgésica, como se ha indicado anteriormente. Los estudios demuestran que tiene una potencia al menos 200 veces superior a la de la morfina. Como el compuesto no era adictivo ni causaba habituación, se pensó inicialmente que era muy prometedor para sustituir a la morfina como analgésico. Sin embargo, la concentración terapéutica está muy cerca de la concentración tóxica. Esto significa que incluso a una dosis terapéutica (5 µg/kg), algo de epibatidina podría unirse a los receptores de acetilcolina muscarínicos y causar efectos adversos, como hipertensión, bradicardia y paresia muscular.
En comparación con el patrón oro en el tratamiento del dolor, la morfina, la epibatidina sólo necesitó 2,5 μg/kg para iniciar un efecto analgésico, mientras que el mismo efecto requirió aproximadamente 10 mg/kg de morfina (4.000 veces la eficacia.) Actualmente, sólo se han realizado investigaciones rudimentarias sobre los efectos de la epibatidina; la droga se ha administrado sólo a roedores para su análisis en este momento.
El antídoto de la epibatidina es la mecamilamina, un antagonista del receptor de la acetilcolina nicotínica que no es selectivo ni competitivo.
Para más información Epibatidine: Natural Frog Poison with a Surprising Benefit to Humans