batracotoxina
Tiempo de lectura estimado: 9 minutos
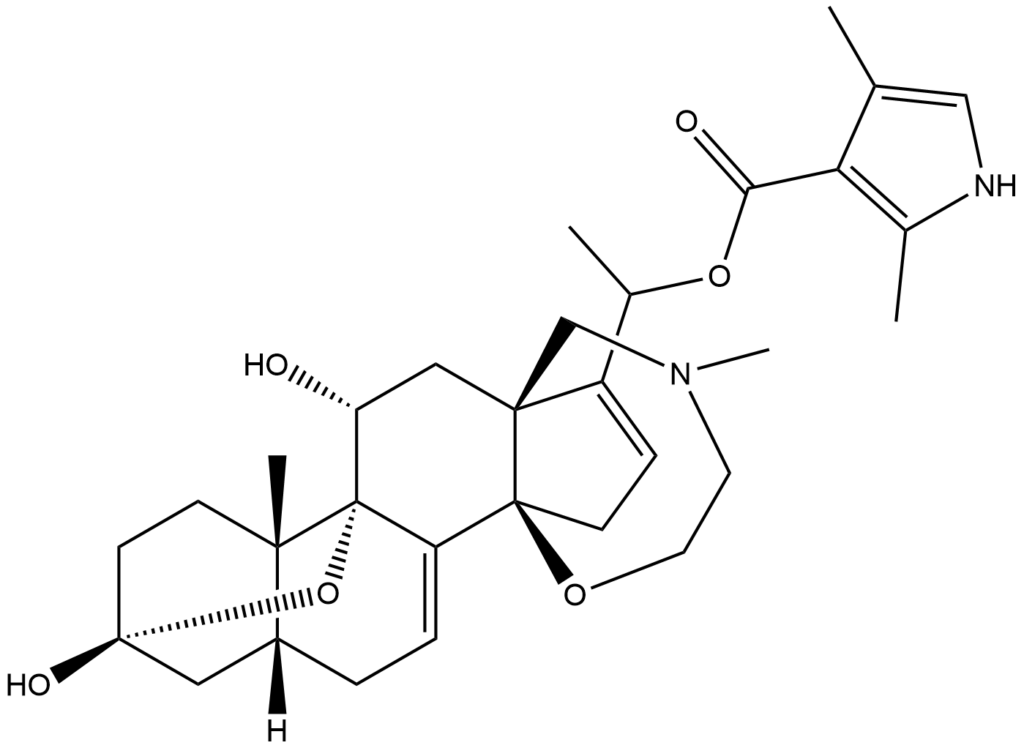
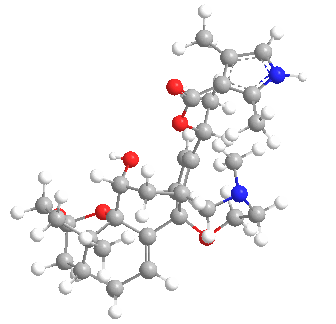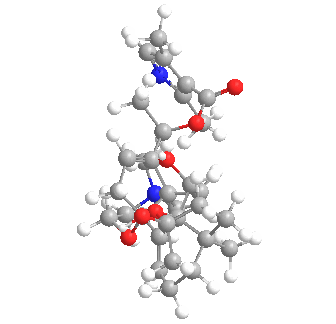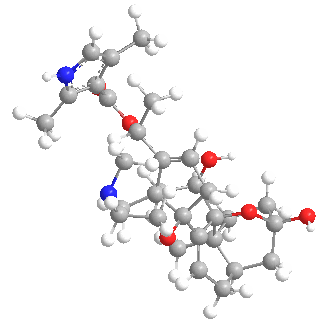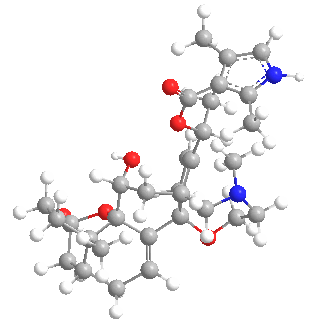
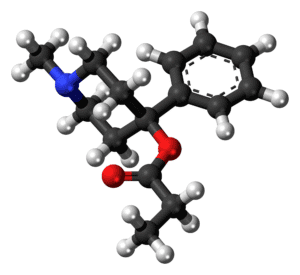
La batracotoxina (BTX) es un alcaloide esteroide extremadamente potente, cardio y neurotóxico, que se encuentra en ciertas especies de escarabajos, aves y ranas. Su nombre procede de la palabra griega βάτραχος, bátrachos, ‘rana’.
Los compuestos químicos estructuralmente relacionados suelen denominarse colectivamente batracotoxinas. Se trata de un alcaloide extremadamente venenoso. En ciertas ranas, este alcaloide está presente sobre todo en la piel. Estas ranas se encuentran entre las que se utilizan para envenenar dardos. La batracotoxina se une a los canales de sodio de las células nerviosas y los abre de forma irreversible, impidiendo que se cierren, lo que provoca parálisis y muerte. No se conoce ningún antídoto.
Historia
La batracotoxina fue descubierta por Fritz Märki y Bernhard Witkop, en el Instituto Nacional de Artritis y Enfermedades Metabólicas, Institutos Nacionales de Salud, Bethesda, Maryland, EE.UU. Märki y Witkop separaron la potente fracción de alcaloides tóxicos de Phyllobates bicolor y determinaron sus propiedades químicas en 1963. Aislaron cuatro alcaloides esteroides tóxicos principales, entre los que se encontraban la batracotoxina, la isobracotoxina, la pseudobatracotoxina y la batracotoxina A.
Debido a la dificultad de manipular una toxina tan potente y a la minúscula cantidad que podía recogerse, la determinación exhaustiva de la estructura entrañaba varias dificultades. Sin embargo, Takashi Tokuyama, que se unió a la investigación más tarde, convirtió uno de los compuestos congéneres, la batracotoxina A, en un derivado cristalino y su estructura esteroidal única se resolvió con técnicas de difracción de rayos X (1968).
Cuando se compararon el espectro de masas y el espectro de RMN de la batracotoxina y de los derivados de la batracotoxina A, se vio que ambos compartían la misma estructura esteroidal y que la batracotoxina era la batracotoxina A con una única fracción de pirrol adicional. De hecho, la batracotoxina podía hidrolizarse parcialmente con hidróxido de sodio en un material con reacciones de color y TLC idénticas a las de la batracotoxina A. La estructura de la batracotoxina se estableció en 1969 mediante la recombinación química de ambos fragmentos. La batracotoxina A fue sintetizada por Michio Kurosu, Lawrence R. Marcin, Timothy J. Grinsteiner y Yoshito Kishi en 1998.
Toxicidad de la batracotoxina
La toxina se libera a través de las secreciones incoloras o lechosas de las glándulas situadas en la espalda y detrás de las orejas de las ranas del género Phyllobates. Cuando una de estas ranas se agita, se siente amenazada o siente dolor, la toxina se libera por reflejo a través de varios canales.
Según los experimentos con roedores, la batracotoxina es uno de los alcaloides más potentes que se conocen: su DL50 intravenosa en ratones es de 2-3 µg/kg. Mientras tanto, su derivado, la batracotoxina A, tiene una toxicidad mucho menor con una DL50 de 1000 µg/kg.
Como neurotoxina, afecta al sistema nervioso. La función neurológica depende de la despolarización de las fibras nerviosas y musculares debido al aumento de la permeabilidad de los iones de sodio de la membrana celular excitable.
Las toxinas liposolubles, como la batracotoxina, actúan directamente sobre los canales iónicos de sodio implicados en la generación del potencial de acción y modificando tanto su selectividad iónica como su sensibilidad al voltaje. La batracotoxina (BTX) se une de forma irreversible a los canales de Na+ lo que provoca un cambio conformacional en los canales que obliga a los canales de sodio a permanecer abiertos. La batracotoxina no sólo mantiene abiertos los canales de sodio con voltaje, sino que también reduce la conductancia de un solo canal. En otras palabras, la toxina se une al canal de sodio y mantiene la membrana permeable a los iones de sodio de una manera «todo o nada».
Esto tiene un efecto directo en el sistema nervioso periférico (SNP). La batracotoxina en el SNP produce un aumento de la permeabilidad (selectiva e irreversible) de la membrana celular en reposo a los iones de sodio, sin modificar la concentración de potasio o de calcio. Esta afluencia de sodio despolariza la membrana celular anteriormente polarizada.
La batracotoxina también altera la selectividad iónica del canal iónico al aumentar la permeabilidad del canal hacia cationes mayores. Los canales de sodio sensibles al voltaje se vuelven persistentemente activos en el potencial de membrana en reposo. La batracotoxina mata bloqueando permanentemente la transmisión de señales nerviosas a los músculos.
La batracotoxina se une a los canales de sodio de las células nerviosas y los abre de forma irreversible, impidiendo su cierre. La neurona ya no puede enviar señales y esto provoca una parálisis.
Aunque generalmente se clasifica como una neurotoxina, la batracotoxina tiene efectos marcados en los músculos del corazón y sus efectos están mediados por la activación de los canales de sodio. La conducción cardíaca se ve alterada, lo que provoca arritmias, extrasístoles, fibrilación ventricular y otros cambios que conducen a la asistolia y al paro cardíaco. La batracotoxina induce una liberación masiva de acetilcolina en los nervios y los músculos, así como la destrucción de las vesículas sinápticas. La batracotoxina R es más tóxica que la batracotoxina A relacionada.
Los cambios estructurales en los nervios y los músculos se deben a una afluencia masiva de iones de sodio, que produce alteraciones osmóticas. Se ha sugerido que también puede haber un efecto en el sistema nervioso central, aunque actualmente no se sabe cuál puede ser ese efecto.
La actividad de la batracotoxina depende de la temperatura, con una actividad máxima a 37 °C (99 °F). Su actividad también es más rápida a un pH alcalino, lo que sugiere que la forma no protonada puede ser más activa.
Tratamiento
Actualmente, no existe ningún antídoto eficaz para el tratamiento de la intoxicación por batracotoxina. La veratridina, la aconitina y la grayanotoxina -al igual que la batracotoxina- son venenos liposolubles que alteran de forma similar la selectividad iónica de los canales de sodio, lo que sugiere un lugar de acción común. Debido a estas similitudes, el tratamiento de la intoxicación por batracotoxina podría modelarse mejor después de, o basarse en, los tratamientos para uno de estos venenos. El tratamiento también puede modelarse a partir del de los digitálicos, que producen efectos cardiotóxicos algo similares.
Aunque no se trata de un antídoto, la despolarización de la membrana puede evitarse o revertirse con la tetrodotoxina (del pez globo), que es un inhibidor no competitivo, o con la saxitoxina («marea roja»). Ambos tienen efectos antagónicos a los de la batracotoxina en el flujo de sodio. Algunos anestésicos pueden actuar como antagonistas de los receptores de la acción de este veneno alcaloide, mientras que otros anestésicos locales bloquean totalmente su acción actuando como antagonistas competitivos.
Fuentes
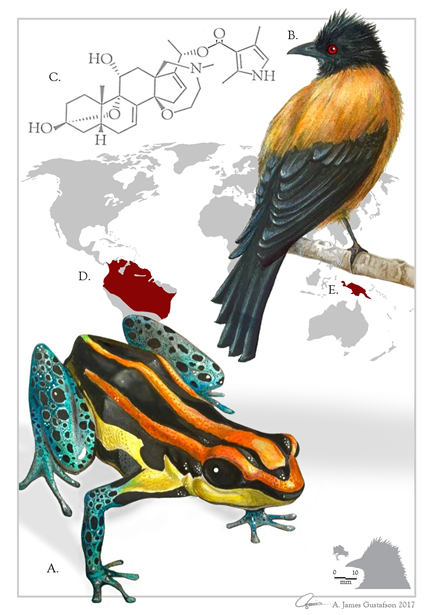
La batracotoxina se ha encontrado en cuatro especies de escarabajos de Papúa, todos del género Choresine de la familia Melyridae; C. pulchra, C. semiopaca y C. rugiceps.
Varias especies de aves endémicas de Nueva Guinea tienen la toxina en su piel y en sus plumas: el ifrit de cabeza azul (Ifrita kowaldi), el pequeño alcaudón (también conocido como alcaudón rufo, Colluricincla megarhyncha), y las siguientes especies de pitohui el pitohui encapuchado (Pitohui dichrous, la más tóxica de las aves), el pitohui crestado (Ornorectes cristatus), el pitohui negro (Melanorectes nigrescens), el pitohui oxidado (Pseudorectes ferrugineus), y el pitohui variable, que ahora se divide en tres especies: el pitohui variable del norte (Pitohui kirhocephalus), el pitohui de Raja Ampat (P. cerviniventris) y el pitohui variable del sur (P. uropygialis).
Aunque no se sabe con certeza el motivo de la toxicidad en estas aves, la presencia de batracotoxinas en estas especies es un ejemplo de evolución convergente. Se cree que estas aves obtienen la toxina de los insectos que contienen batracotoxina que comen y luego la secretan a través de la piel.
La batracotoxina también se ha encontrado en algunas especies de ranas colombianas: la rana venenosa dorada (Phyllobates terribilis), la rana venenosa de patas negras (P. bicolor) y la rana venenosa Kokoe (P. aurotaenia). La rana venenosa Kokoe solía incluir a P. sp. aff. aurotaenia, ahora reconocida como distinta. Las cuatro especies de ranas pertenecen a la familia de las ranas venenosas.
Las ranas no producen la batracotoxina por sí mismas. Al igual que en las aves, se cree que estas ranas obtienen la toxina de los insectos que contienen batracotoxina que comen, y luego la secretan a través de la piel. Los escarabajos del género Choresine no se encuentran en Colombia, pero se cree que las ranas podrían obtener la toxina de escarabajos de otros géneros dentro de la misma familia (Melyridae), varios de los cuales se encuentran en Colombia.
Las ranas criadas en cautividad no producen batracotoxina, por lo que pueden ser manipuladas sin riesgo. Sin embargo, esto limita la cantidad de batracotoxina disponible para la investigación, ya que de 10.000 ranas sólo se obtuvieron 180 mg de batracotoxina. Como estas ranas están en peligro de extinción, su recolección no es ética. Los estudios biosintéticos también se ven dificultados por la lenta tasa de síntesis de la batracotoxina.
El hábitat nativo de las ranas venenosas es las regiones cálidas de América Central y del Sur, en las que la humedad ronda el 80%.
Usos
El uso más común de esta toxina es el de los indígenas Noanamá y Emberá de los Embera-Wounaan ubicados en el oeste de Colombia para envenenar los dardos de las cerbatanas que se utilizan en la caza.
Los indigenas preparan los dardos envenenados empalando primero una rana en un trozo de madera. Se forman burbujas de veneno cuando la piel de la rana empieza a ampollarse. Las puntas de los dardos se preparan tocándolas con la toxina, o se puede coger la toxina en un recipiente y dejarla fermentar. Los dardos envenenados hechos con batracotoxina fresca o fermentada son suficientes para cazar monos y pájaros. La parálisis nerviosa es casi instantánea. Otros relatos dicen que se introduce un palo siurukida («diente de bambú») por la boca de la rana y se hace salir por una de sus patas traseras. Esto hace que la rana transpire profusamente por su espalda, que se cubre de una espuma blanca. Los dardos se sumergen o enrollan en la espuma, conservando su poder letal hasta un año.
Para más información batrachotoxin