Dimercaprol – BAL
Tiempo de lectura estimado: 7 minutos
El dimercaprol, también llamado anti-Lewisita británico (British anti-Lewisite – BAL), es un medicamento utilizado para tratar el envenenamiento agudo por arsénico, mercurio, oro y plomo. También puede utilizarse para el envenenamiento por antimonio, talio o bismuto, aunque las pruebas de estos usos no son muy sólidas.
Los efectos secundarios más comunes son la hipertensión, el dolor en el lugar de la inyección, los vómitos y la fiebre. No se recomienda a las personas alérgicas a los cacahuetes, ya que suele estar formulado en forma de suspensión en aceite de cacahuete. No está claro si su uso durante el embarazo es seguro para el bebé. El dimercaprol es un quelante y actúa uniéndose a los metales pesados.
El dimercaprol se fabricó por primera vez durante la Segunda Guerra Mundial y figura en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud.
Historia del dimercaprol
El desarrollo del dimercaprol debe comenzar primero con su némesis: La lewisita. La lewisita es una combinación de acetileno y tricloruro de arsénico y también ha sido conocida como el «Rocío de la Muerte». La lewisita tiene su origen en el acetileno. En el siglo XIX, el mundo no lograba dar con un caucho sintético.
Un joven llamado Julius Arthur Nieuwland era estudiante de posgrado en la Universidad Católica de América en Washington D.C. Estaba investigando sobre el acetileno con la esperanza de encontrar una solución para el caucho sintético (el padre Nieuwland descubrió más tarde cómo hacer caucho sintético a partir del acetileno en 1923).
Posteriormente, el padre Nieuwland se interesó por el gas acetileno. Su tesis doctoral de 1904, titulada «Algunas reacciones del acetileno», esbozaba la síntesis de un gas venenoso a partir del acetileno y el tricloruro de arsénico (también conocido como lewisita). Sin embargo, siendo un católico honesto, considera que es mejor no presentar al mundo un gas venenoso. Esto no es cierto en su redescubrimiento.
El descubrimiento del capitán Lewis
En 1918, el soldado W. Lee Lewis comienza su búsqueda de agentes químicos de guerra. Estaba destinado en la Universidad Católica de América donde descubrió la tesis del padre Nieuwland. El capitán Lewis perfecciona la síntesis de la lewisita refiriéndose a ella como «¡el material al lado del cual el gas mostaza se convierte en un olor suave!»
Aunque se desarrolló demasiado tarde para ser utilizada durante la Primera Guerra Mundial, la lewisita siguió figurando en la lista de posibles agentes químicos de guerra. Con el comienzo de la Segunda Guerra Mundial, el Ministerio de Suministros británico apoyó los experimentos de la Universidad de Oxford para encontrar antídotos contra este y otros agentes.
El grupo de bioquímicos de Oxford desarrolló con éxito el dimercaprol o BAL (inicialmente llamado OX 217) el 21 de julio de 1940. Por razones de seguridad, el anuncio público de este éxito no se publicó hasta 1945. El BAL fue recibido por primera vez en los Estados Unidos en 1941, después de lo cual una variedad de agencias gubernamentales cooperaron en el estudio de su preparación, fabricación, bioquímica, toxicología, farmacología, terapéutica experimental y aplicación clínica.
Las mejoras en la síntesis condujeron al desarrollo de soluciones y ungüentos terapéuticos. Las pruebas de estas soluciones y pomadas durante la Segunda Guerra Mundial revelaron una eficacia notable. Por ejemplo, tras la aplicación de una cantidad de lewisita suficiente para destruir el ojo de un conejo, la instilación de una solución de BAL al 5% hasta 5 minutos después de la contaminación produjo una recuperación casi completa.
Se obtuvieron resultados similares en experimentos con lesiones cutáneas en conejos y en voluntarios humanos. En consecuencia, el dimercaprol fue fabricado por DuPont durante la Segunda Guerra Mundial, y se estudió la posibilidad de producir 200.000 libras de BAL por año porque se creía que tal cantidad podría ser necesaria (es decir, si las potencias del Eje hubieran utilizado armas químicas contra las tropas estadounidenses).
Química y bioquímica del dimercaprol
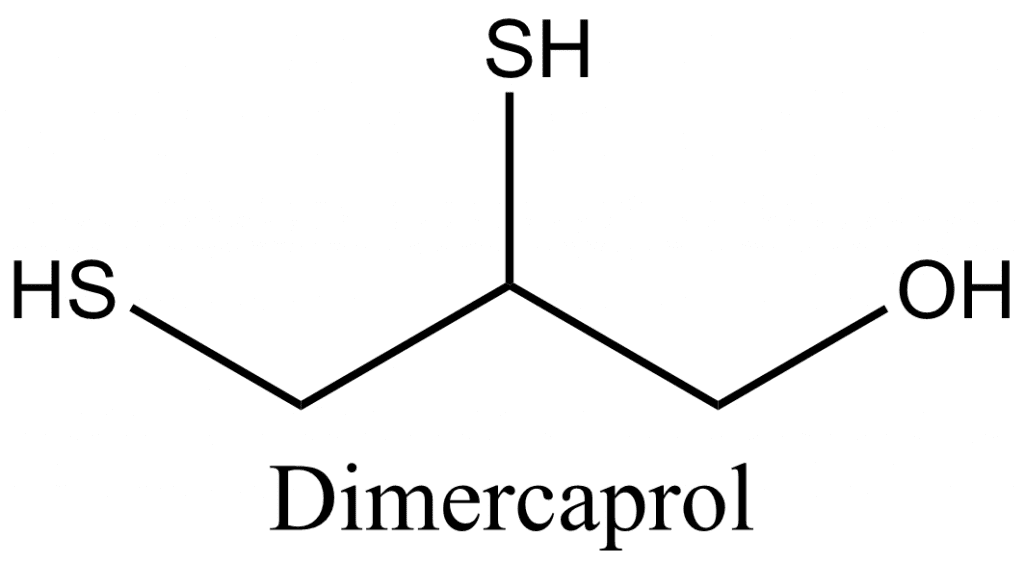
El dimercaprol tiene una columna vertebral de 3 carbonos con dos grupos sulfhidrilos (-SH) y un grupo hidroxilo. Las primeras investigaciones sobre el mecanismo de eficacia del BAL surgieron del trabajo con los grupos de arsénico y azufre en la proteína del cabello. En ese momento se conjeturó que los metales se unen a los grupos sulfhidrilos de varias enzimas como mecanismo para su importante toxicidad.
El Grupo de Oxford había estado probando el glutatión (C10H17N3O6S un polipéptido de glicina, cistina y ácido glutámico) con un grupo sulfhidrilo en el tratamiento de la intoxicación por arsénico sin mucho éxito. Utilizando el cabello humano con abundantes grupos tiol pudieron dilucidar el mecanismo del dimercaprol.
Con el tiempo se descubrió que los grupos sulfhidrilos del ácido lipoico eran el objetivo de la intoxicación por arsénico. El ácido lipoico es un componente clave de dos importantes enzimas: la piruvato deshidrogenasa (PDH) y la alfa-cetogluterato deshidrogenasa (KDH). La PDH convierte el producto final de la glucólisis en acetil coenzima A, que puede entrar en el ciclo del ácido tricarboxílico (TCA).
La KDH es una enzima del ciclo TCA. El ácido lipoico es un ditiol de 8 carbonos que está unido covalentemente a una subunidad del complejo PDH y KDH (figura 1). En presencia de arsénico, los dos grupos sulfhidrilos se unen al arsénico para formar un anillo de seis miembros (figura 2). El dimercaprol presenta dos grupos sulfhidrilos al ácido arsénico-lipoico unido y forma un anillo de cinco miembros más estable (figura 3), liberando así a la PDH y a la KDH de la inhibición por arsénico.
Como se ha mencionado anteriormente, otros metales también forman complejos con grupos sulfhidrilos. Los complejos más estables entre el BAL y los iones metálicos se forman con los metales de clase B (arsénico, mercurio y oro). El plomo es un metal de clase A y la quelación se consigue mejor añadiendo un segundo quelante como el ácido meso-2,3-dimercaptosuccínico (DMSA) o el ácido etilendiaminotetracético (EDTA).
En los Estados Unidos, el dimercaprol es fabricado únicamente por Akorn, Inc. (Decatur, IL). Se presenta en ampollas de 3 ml (100 mg/mL) disueltas en aceite de cacahuete. El componente de aceite de cacahuete hace que esté contraindicado en cualquier persona alérgica a los derivados del cacahuete.
En la época en que se fabricó por primera vez el BAL, el aceite de cacahuete era un disolvente barato y común para compuestos liposolubles como el dimercaprol. Además, el BAL se hidroliza en una solución acuosa, pero es estable en el aceite de cacahuete. Desafortunadamente, el cambio de disolventes a uno que es menos probable que desencadene reacciones alérgicas (por ejemplo, el aceite de sésamo) requeriría ensayos clínicos de la Administración de Alimentos y Medicamentos de los Estados Unidos y no se considera comercialmente factible.
Para más información British anti-Lewisite (dimercaprol): an amazing history