Tiempo de lectura estimado: 5 minutos
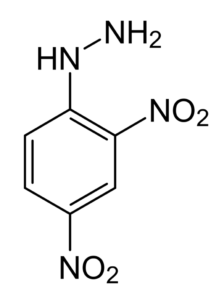
La 2,4-dinitrofenilhidrazina (2,4-DNPH o DNPH) es el compuesto orgánico C6H3(NO2)2NHNH2. La DNPH es un sólido de color rojo a naranja. Es una hidrazina sustituida. El sólido es relativamente sensible a impactos y fricción. Por esta razón, la DNPH suele manipularse como un polvo húmedo. La DNPH es un precursor del fármaco Sivifene.
Síntesis del DNPH
La síntesis del 2,4-Dinitrofenilhidrazina (DNPH) a partir del benceno implica un proceso de tres etapas que abarca la bromación, la nitroación y una inesperada reacción de sustitución.
1. Bromación (Sustitución Electrofílica):
– La primera etapa es la bromación del benceno. Esto implica tratar el benceno con bromo (\(Br_2\)) en presencia de un catalizador ácido de Lewis, típicamente hierro o bromuro de aluminio. La reacción de bromación sustituye un átomo de hidrógeno en el anillo de benceno por un átomo de bromo, produciendo bromobenceno.
2. Nitroación (Sustitución Electrofílica):
– La segunda etapa implica la nitroación de bromobenceno. La nitroación se logra tratando bromobenceno con ácido nítrico (\(HNO_3\)) y un catalizador, a menudo ácido sulfúrico (\(H_2SO_4\)). Este proceso introduce un grupo nitro (\(-NO_2\)) en el anillo de benceno, resultando en nitrobromobenceno.
3. Reacción de Sustitución Inesperada:
– La reacción final e inesperada implica tratar nitrobromobenceno con hidrazina (\(N_2H_4\)) bajo condiciones específicas. Esta reacción conduce a la sustitución de los grupos bromo y nitro por hidrazina, formando 2,4-Dinitrofenilhidrazina.
Las condiciones específicas para esta etapa dependerían de los parámetros de reacción elegidos, como la temperatura, el solvente y la presencia de catalizadores o reactivos que faciliten la inesperada sustitución. El resultado es la formación de 2,4-Dinitrofenilhidrazina, un sólido de color rojo a naranja, que generalmente se maneja como un polvo húmedo debido a su sensibilidad al impacto y la fricción.
Uso
La DNPH es un reactivo utilizado en laboratorios de análisis orgánico cualitativo. El reactivo de Brady o reactivo de Borche se prepara disolviendo DNPH en una solución que contiene metanol y algo de ácido sulfúrico concentrado.
Esta solución se utiliza para detectar cetonas y aldehídos. Una prueba positiva se señala por la formación de un precipitado amarillo, naranja o rojo de la dinitrofenilhidrazona. Las cetonas aromáticas dan precipitados rojos, mientras que las cetonas alifáticas dan un color más amarillo. La reacción entre DNPH y una cetona genérica para formar una hidrazona se muestra a continuación:
Esta reacción es, en general, una reacción de condensación, ya que dos moléculas se unen con la pérdida de agua. Mecánicamente, es un ejemplo de reacción de adición-eliminación: adición nucleofílica del grupo -NH2 al grupo carbonilo C=O, seguida por la eliminación de una molécula de H2O.
Las hydrazonas derivadas de DNP tienen puntos de fusión característicos, facilitando la identificación del grupo carbonilo. En particular, el uso de DNPH fue desarrollado por Brady y Elsmie. Técnicas espectroscópicas y espectrométricas modernas han reemplazado estas técnicas.
La DNPH no reacciona con otros grupos funcionales que contienen carbonilo, como ácidos carboxílicos, amidas y ésteres, para los cuales hay una estabilidad asociada a la resonancia ya que un par solitario de electrones interactúa con el orbital p del carbono carbonílico, lo que resulta en una mayor delocalización en la molécula.
Esta estabilidad se perdería por la adición de un reactivo al grupo carbonilo. Por lo tanto, estos compuestos son más resistentes a las reacciones de adición. Además, con los ácidos carboxílicos, hay un efecto del compuesto actuando como una base, dejando al carboxilato resultante cargado negativamente y, por lo tanto, ya no vulnerable al ataque nucleofílico.
Seguridad
La DNPH en estado seco es sensible a la fricción y al impacto. Por esta razón, se suministra húmeda o «mojada» cuando una escuela la adquiere de un proveedor de productos químicos. Si la DNPH se almacena de manera inadecuada y se deja secar, puede volverse explosiva. Es un disociador artificial de la cadena de transporte de electrones (ETC).
En el 2016, escuadrones de manejo de explosivos tuvieron que detonar de manera controlada varios lotes de DNPH en escuelas en el Reino Unido debido a que se habían almacenado de manera inadecuada y se había vuelto explosiva.
Para más información Reactions of Primary Amine Derivatives
Como citar este artículo:
APA: (). 2,4-dinitrofenilhidrazina – DNPH. Recuperado de https://quimicafacil.net/compuesto-de-la-semana/24-dinitrofenilhidrazina-dnph/
ACS: . 2,4-dinitrofenilhidrazina – DNPH. https://quimicafacil.net/compuesto-de-la-semana/24-dinitrofenilhidrazina-dnph/. Fecha de consulta 2026-04-19.
IEEE: , "2,4-dinitrofenilhidrazina – DNPH," https://quimicafacil.net/compuesto-de-la-semana/24-dinitrofenilhidrazina-dnph/, fecha de consulta 2026-04-19.
Vancouver: . 2,4-dinitrofenilhidrazina – DNPH. [Internet]. [citado 2026-04-19]. Disponible en: https://quimicafacil.net/compuesto-de-la-semana/24-dinitrofenilhidrazina-dnph/.
MLA: . "2,4-dinitrofenilhidrazina – DNPH." https://quimicafacil.net/compuesto-de-la-semana/24-dinitrofenilhidrazina-dnph/. . Web.
Si tiene alguna pregunta o sugerencia, escribe a administracion@quimicafacil.net, o visita Como citar quimicafacil.net