Estimated reading time: 3 minutos
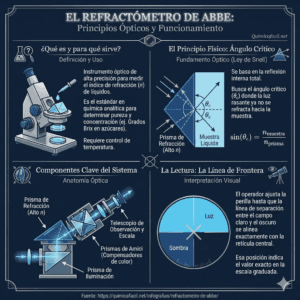
El refractómetro Abbe, que lleva el nombre de su inventor Ernst Abbe (1840-1905), fue el primer instrumento de laboratorio para la determinación precisa del índice de refracción de los líquidos. El principio de medición de un refractómetro Abbe se basa en el principio de la reflexión total.
Funcionamiento de un refractometro
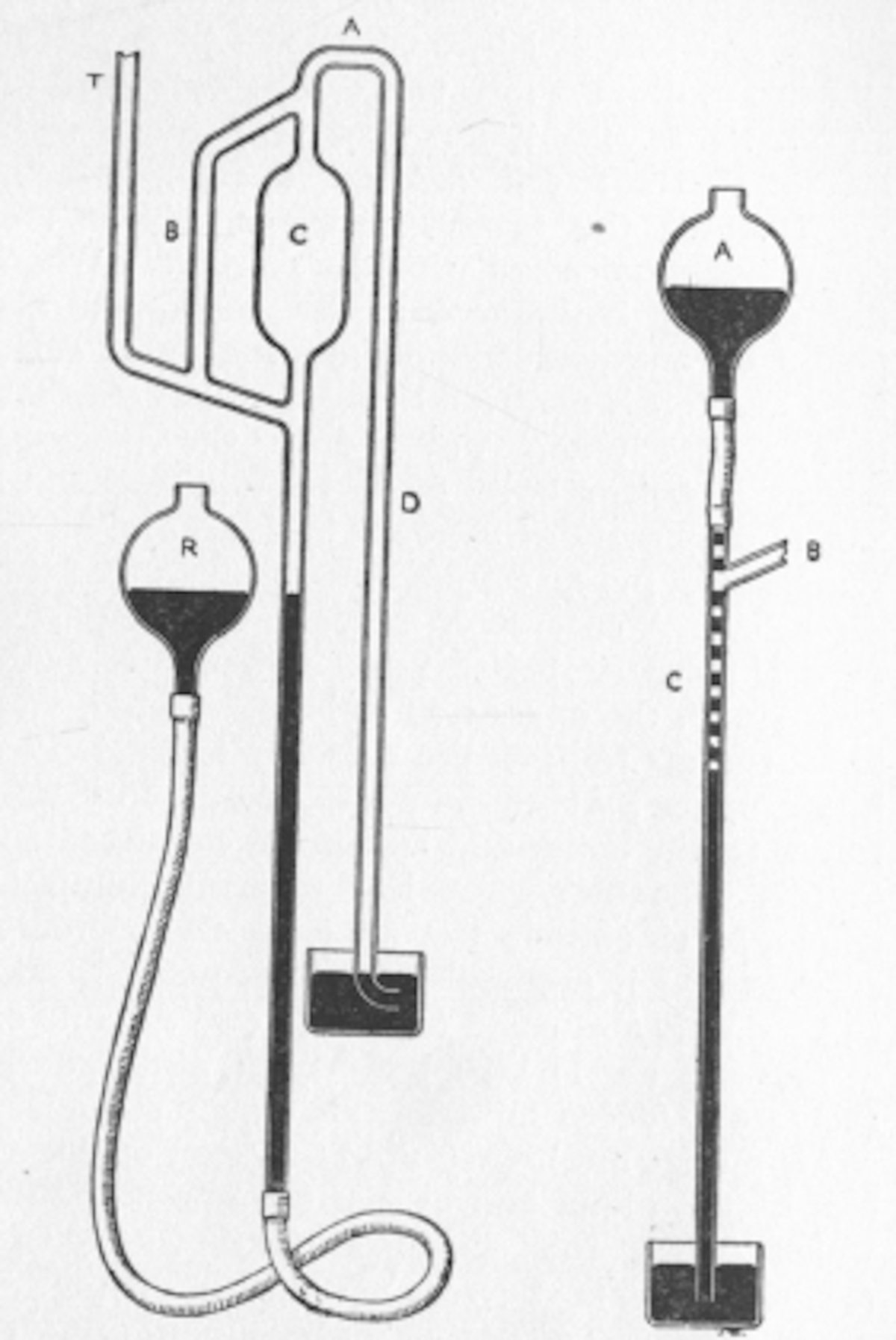
Los refractómetros de Abbe se utilizan para medir líquidos. Los vasos de medios de referencia (prismas) pueden seleccionarse con altos índices de refracción. La luz de una fuente de radiación es reflejada por un espejo y golpea un prisma doble. Unas pocas gotas de la muestra se colocan entre este llamado doble prisma de Abbe.
Los rayos de luz incidentes pasan a través del doble prisma y la muestra sólo si sus ángulos de incidencia en la interfaz son menores que el ángulo crítico de reflexión total. Se utiliza un microscopio y un espejo con un mecanismo adecuado para determinar la línea límite claro/oscuro (línea de sombra).
Manejo del refractómetro de Abbe
El operador del refractómetro Abbe ajusta el espejo con la ayuda de un mando giratorio hasta que el límite claro/oscuro se encuentra en la intersección de la retícula del microscopio. Los índices de refracción correspondientes se pueden leer entonces en una escala de Vernier.
Dado que el límite claro/oscuro es muy bajo en contraste, sólo puede determinarse manualmente de forma aproximada. La precisión del refractómetro clásico de Abbe es nD = 0,0002, donde el cuarto decimal se determina promediando un gran número de mediciones individuales. Los resultados dependen de la interpretación del usuario y a menudo difieren entre los usuarios.
Los refractómetros semiautomáticos están equipados con una pantalla digital de los datos de medición y permiten así una lectura más coherente de los datos de medición. Sin embargo, sigue siendo necesario un ajuste manual de este equipo, de modo que los resultados de la medición que se obtengan sigan dependiendo de la interpretación y la habilidad de la persona que se mide.
Para más información Classic Kit: Abbes refractometer
Como citar este artículo:
APA: (2019-07-22). Refractómetro de Abbe. Recuperado de https://quimicafacil.net/infografias/material-de-laboratorio/refractometro-de-abbe/
ACS: . Refractómetro de Abbe. https://quimicafacil.net/infografias/material-de-laboratorio/refractometro-de-abbe/. Fecha de consulta 2026-03-10.
IEEE: , "Refractómetro de Abbe," https://quimicafacil.net/infografias/material-de-laboratorio/refractometro-de-abbe/, fecha de consulta 2026-03-10.
Vancouver: . Refractómetro de Abbe. [Internet]. 2019-07-22 [citado 2026-03-10]. Disponible en: https://quimicafacil.net/infografias/material-de-laboratorio/refractometro-de-abbe/.
MLA: . "Refractómetro de Abbe." https://quimicafacil.net/infografias/material-de-laboratorio/refractometro-de-abbe/. 2019-07-22. Web.
Si tiene alguna pregunta o sugerencia, escribe a administracion@quimicafacil.net, o visita Como citar quimicafacil.net