Raoul-Pierre Pictet
Tiempo de lectura estimado: 17 minutos
Raoul-Pierre Pictet (4 de abril de 1846 – 27 de julio de 1929) fue un físico suizo. Trabajo especialmente en la licuefacción de los llamados gases permanentes y bajas temperaturas.
Vida personal de Raoul-Pierre Pictet
Raoult-Pierre Pictet nació el 4 de agosto de 1846, hijo de Auguste Pictet-de Bock, militar en varios servicios en el extranjero, y miembro de una prominente familia ginebrina que había suministrado ciudadanos distinguidos al Estado. Marc Auguste, colaborador de de Saussure y su sucesor en una cátedra de la antigua Academia de Calvino, fue uno de los fundadores de la Societé Helvétique des Sciences Naturelles. Ernest Pictet fue banquero, presidente del Gran Consejo de Ginebra y representante de su ciudad en el Parlamento nacional; uno de sus hijos, Charles, representó a Ginebra en el Congreso de Viena de 1815 y fue uno de los creadores de la Bibliotheque Britannique; otro hijo, Amé (1857- 1937) fue un químico orgánico muy famoso que realizó un extenso trabajo sobre las reacciones pirogénicas, estableció la constitución de la nicotina y desarrolló una síntesis para la misma.
Raoult estudió primero en el College Calvin y luego en la Academia de Ginebra, donde se graduó a los dieciocho años. En 1867 se matriculó en la École Polytechnique de París, algo inusual para un ciudadano no francés. Entre sus profesores estaban Victor Regnault (1810-1878) y Charles-Adolph Würtz (1817- 1884). Durante su estancia en la École Polytechnique encontró tiempo para seguir cursos adicionales en el College de France y en la Sorbona. Tras licenciarse en 1868, publicó sus memorias sobre la visión binocular y la resistencia del aire. Sus trabajos sobre la visión binocular fueron tan importantes que la Académie de Saint Pétersbourg se ofreció a publicarlos en una memoria completa.
Etapa docente
A los veinticinco años entró al servicio del Virrey de Egipto y se le encargó la creación de un curso de física experimental en la Escuela Superior de El Cairo. Durante los tres años que pasó en Egipto se dedicó a estudiar la termodinámica y fenómenos como la acción solar, el polvo, los torbellinos y remolinos, y la temperatura y las crecidas del Nilo.
Se interesó especialmente por los reptiles venenosos de las regiones del Nilo, con vistas a combatir su veneno en el sistema humano. Recogió serpientes y estudió su veneno en su acción sobre el sistema animal. También tuvo tiempo para construir y dirigir una fábrica de hielo e inventar un proceso para congelar grandes superficies de hielo para el patinaje, que más tarde se aplicó en las pistas de patinaje, construidas en Londres, Manchester y otros lugares.
Experimentando a bajas temperaturas
En 1874 Raoul-Pierre Pictet regresó a Ginebra y se dedicó a experimentar con la física de las bajas temperaturas, con la vista puesta en la lucrativa industria de la refrigeración, que estaba creciendo rápidamente. Comenzó a estudiar la posibilidad de utilizar el dióxido de azufre como posible refrigerante y acabó registrando una patente al respecto. El sistema de refrigeración por compresión que desarrolló, con dióxido de azufre como medio refrigerante, funcionaba a una presión mucho más baja que los sistemas de la competencia; sin embargo, el contacto con el agua a menudo convertía el refrigerante en ácido sulfuroso corrosivo. El sistema, protegido por varias patentes, se comercializó con mucho éxito.
Posteriormente, comenzó a trabajar en la posibilidad de licuar los gases permanentes. Basándose en los trabajos de Faraday, Andrews y Clausius, y en su amplia experiencia en el tema de la refrigeración, consiguió finalmente licuar el oxígeno. Su instalación consistía esencialmente en cuatro compresores que desempeñaban el papel de una bomba de aspiración y compresión, y un largo tubo de Faraday. En el tubo de Faraday el oxígeno se generaba mediante una reacción química, y se comprimía y licuaba sin ayuda de dispositivos mecánicos, sólo por la acumulación de los productos de la reacción química.
En 1877 aceptó una cátedra de física y matemáticas en la Universidad de Ginebra y permaneció allí durante siete años. En 1886 abandonó la vida académica para establecer un laboratorio de investigación industrial de bajas temperaturas en Berlín y comercializar sus inventos. Su sistema se basaba en un refrigerante patentado, el líquido Pictet (dióxido de azufre más dióxido de carbono), que le hizo entrar en controversia porque afirmó que estaba exento de la segunda ley de la termodinámica.
La carrera por el oxígeno liquido
En diciembre de 1877, Raoul-Pierre Pictet y Louis Paul Cailletet (1831-1913) comunicaron simultáneamente a la Académie des Sciences de París que habían conseguido la licuefacción del oxígeno. La importancia de la hazaña no es sólo que se haya conseguido, sino que se ha logrado con métodos completamente diferentes. Cailletet había empleado una combinación de compresión, enfriamiento y expansión del gas, mientras que Pictet había empleado el método de la cascada, en el que se disponían en serie tres medios de enfriamiento diferentes con temperaturas críticas satisfactoriamente más bajas, de modo que el gas licuado en primer lugar actuara como refrigerante en la siguiente etapa de licuefacción. Los tres gases empleados por Pictet eran dióxido de azufre, dióxido de carbono y oxígeno. La cuestión de la prioridad en la consecución de los objetivos ha sido objeto de una agria discusión.
Poco después, Pictet anunció que había utilizado su equipo para licuar y solidificar el hidrógeno.
El trabajo de Raoul-Pierre Pictet en el campo de la baja temperatura fue reconocido por muchas organizaciones: Fue nombrado miembro de la Legión de Honor, en 1878 la Royal Institution le concedió la Medalla Davy, ese mismo año la Exposición Internacional de París le concedió una medalla de oro, las ciudades de Amberes y Roma le concedieron diplomas y medallas de honor, y en 1895 la Société Industrielle du Nord de la France le concedió su Gran Medalla en Lille.
Otros campos de estudio de Pictet
Entró en el campo de la filosofía intelectual y moral con su libro Etude Critique du Materialisme et du Spiritualisme par la Physique Experimentale, en el que investigó la relación entre la energía material y las operaciones mentales; se considera una protesta científica contra las doctrinas que conducen a la depresión o la desesperación. También fue un poeta aficionado, como puede verse en el folleto que dedicó a su amigo el poeta Édouard Tavan, con motivo de su septuagésimo cumpleaños.
Contribución científica de Raoul-Pierre Pictet
Pictet utilizó los conocimientos y tecnologías que había desarrollado para alcanzar temperaturas muy bajas para estudiar su efecto en muchos procesos físicos y químicos, y la licuefacción del oxígeno y otros gases.
Licuefacción del oxígeno
La licuefacción del oxígeno representa un sensacional logro científico que fue alcanzado en 1877 casi simultáneamente por Cailletet y Pictet utilizando técnicas experimentales completamente diferentes. Este logro también estuvo acompañado (y sigue estándolo) de muchas discusiones sobre la prioridad del descubrimiento.
Los resultados de Cailletet y Pictet fueron comunicados a la Academie des Sciences por el secretario Permanente, Jean Baptiste Andre Dumas (1800-1884), durante la sesión celebrada el 24 de diciembre de 1877, y recogidos en Compt. Rendu, 85, 1212-1219, 187716 – En esta sesión se leyó la nota de Cailletet «De la Condensation de l’Oxygene et de l’Oxyde de Carbone» y el telegrama enviado por Pictet y recibido el 22 de diciembre a las 20 horas, informando de la licuefacción del oxígeno con las siguientes palabras «Oxygene liquefie aujord’hui sous 320 atmospheres et-140 de froid par acide sulphureux et carbonique accouples«.
En su nota, Cailletet informó que si el oxígeno o el monóxido de carbono se ponían en su aparato 17 a 300 atm y se enfriaban a -29ºC con dióxido de azufre hirviendo, ambos gases permanecían como tales. Si los gases se liberaban repentinamente, se enfriaban, según la fórmula de Poisson, a una temperatura 200ºC por debajo de la inicial, e inmediatamente se veía una niebla intensa (brouillard intense), causada por la licuefacción y quizás la solidificación del oxígeno o del monóxido de carbono.
Método de Pictet para licuar el oxigeno
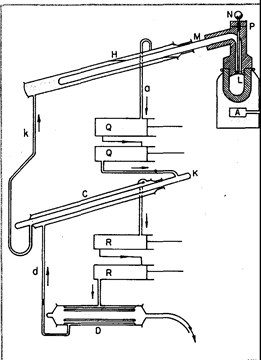
El telegrama de Raoul-Pierre Pictet iba seguido de un documento que describía detalladamente el equipo y el procedimiento utilizados para lograr la condensación del oxígeno (Fig. 1): Q y R eran bombas de aspiración de doble efecto. R funcionaba con dióxido de azufre anhidro líquido contenido en el tubo C a -65°C. El SO2 gaseoso generado en C se dirigía al condensador D, que funcionaba con agua refrigerada, donde se licuaba a -25°C y a unas 2,75 atmósferas. El diámetro de la tubería k era lo suficientemente pequeño como para producir la contrapresión necesaria para condensar el SO2. Del mismo modo, las bombas R funcionaban con CO2 líquido contenido en el espacio anular H, mantenido a la presión adecuada para evaporar el líquido a -140°C. El CO2 gaseoso producido se dirigía al condensador k rodeado por un tubo que contenía SO2 líquido a -65°C y 5 atmósferas. El diámetro del tubo d era lo suficientemente pequeño como para producir la contrapresión necesaria para condensar el CO2. El CO2 líquido se remitía a H a través del conector k
L era un matraz de hierro forjado, capaz de soportar una presión de 500 atmósferas, utilizado para generar oxígeno puro calentando clorato de potasio con una fuente de calor (basado en el concepto de Faraday). La cantidad de sal añadida al matraz determinaba la presión de oxígeno alcanzada. El gas producido se acumulaba en el tubo interno de H, mantenido a -140°C, y tras varias horas de funcionamiento alcanzaba una presión de 320 atmósferas. Al abrir el grifo en N se produjo una fuerte expansión del oxígeno comprimido y frío y una gran parte de éste se licuó y llenó el tubo M.
Por sus investigaciones sobre la licuefacción del oxigeno, Cailletet y Pictet recibieron la Medalla Davy de la Royal Society de Londres (noviembre de 1878) y el Prix Lacaze de la Académie des Sciences (1883). Los miembros del comité de selección fueron Berthelot, Auguste Cahours (1813-1891), Michel Eugéne Chevreul (1786-1889, Henri Debray (1827-1888), Jean Baptiste André Dumas (1800-1884), Edmond Frémy (1814-1894), Charles Friedel (1832-1899), Louis Pasteur (1822-1895) y Charles-Adolphe Würtz (1817-1884).
Aunque las actas de la sesión de la Académie des Sciences indican que Cailletet informó de la licuefacción del oxígeno antes que Pictet, se ha discutido mucho sobre si presentan los hechos tal como ocurrieron realmente.
Congelación de soluciones acuosas
Raoul-Pierre Pictet estudió la congelación de soluciones acuosas de ácido sulfúrico y de etanol con el doble objetivo de determinar la temperatura de inicio de la cristalización y la posibilidad de que se formaran hidratos a bajas temperaturas. Su primera memoria estuvo dedicada al ácido sulfúrico. Su técnica experimental era muy inteligente y estaba diseñada para reducir los errores al mínimo. Realizó cuatro series diferentes de ejecuciones, una partiendo del ácido puro y añadiendo cantidades de agua en proporciones molares definidas; otra añadiendo agua al ácido para conseguir concentraciones en peso definidas, y dos series más en las que empezó con agua pura y añadió ácido de la misma manera que en las dos series anteriores. A continuación, cada solución se enfriaba hasta que se solidificaba aproximadamente la mitad, y entonces se determinaba la composición de ambas fases. Pictet explicó que no utilizó una dilución continua de la solución original para evitar errores experimentales como el traslado de un recipiente a otro y el contacto con el aire húmedo.
Congelación de sustancias orgánicas
Otro trabajo experimental estaba relacionado con la determinación de los puntos de congelación de las sustancias orgánicas puras y con la búsqueda de una regularidad entre este parámetro y su estructura. Las sustancias seleccionadas para este estudio se diferenciaban por la introducción de un grupo CH3 o la sustitución del hidrógeno por cloro. Eran: Cloruro de bencilo, C6H5CH2Cl; cloruro de bencilo, C6H4CHCl2; benzotricloruro, C6H5CCl3; benzaldehído, C6H5CHO; piridina, C5H5N; piperidina, C5H11N; quinoleína, aldehído cinámico, ácido propiónico, o-xileno, ácido isobutírico, tolueno, ácido láctico, mesitileno, metilanilina y m-xileno. Algunos de estos compuestos (ácido isobutírico, tolueno, ácido láctico, metilanilina y m-xileno) no cristalizaron ni siquiera cuando se enfriaron a -100°C
Raoul-Pierre Pictet concluyó lo siguiente:
- Existe una ley general que describe la influencia de un grupo determinado en una molécula aromática: la introducción de un grupo CH3 siempre disminuye el punto de congelación. Por ejemplo, el benceno se congela a +4ºC; la introducción de un grupo CH3 disminuye la temperatura por debajo de -1 00ºC. La anilina se congela a -8ºC; la introducción de un grupo metilo (metilanilina) reduce la temperatura por debajo de-l00ºC.
- La sustitución del hidrógeno en un grupo metilo por cloro aumenta el punto de congelación. La sustitución de los tres átomos de hidrógeno por cloro detiene este aumento. Por ejemplo, el tolueno cristaliza por debajo de -100ºC, el cloruro de bencilo a -47,9ºC; el clorobenzol a- 17ºC; y el cloruro de bencilo también a -17ºC
- Los resultados validaron la ley de Bayer según la cual, en cuerpos homólogos con estructuras similares, el punto de congelación aumenta o disminuye según el número de carbonos sea par o impar. Los compuestos que tienen un número de carbonos deteriorado presentan la menor temperatura de cristalización. Por ejemplo, el ácido propiónico cristaliza a -24 ºC, mientras que el ácido acético lo hace a +16,5ºC, y el ácido butírico a -19ºC.
- Para una serie determinada, una molécula más simétrica que su vecina en la serie cristaliza fácilmente a una temperatura relativamente alta. Así, el ácido butírico cristaliza a -19ºC, y el ácido isobutírico a temperaturas inferiores a -100ºC. Del mismo modo, el ácido hexanoico cristaliza a -18ºC y el ácido dietilbutírico lo hace a temperaturas inferiores a -100ºC.
Los tres isómeros o, m y p-xilenos siguieron la misma ley.
Nuevos fluidos refrigerantes
Raoul-Pierre Pictet demostró que, en los motores frigoríficos, para una diferencia de temperatura dada entre el condensador y el refrigerante y un efecto de refrigeración determinado, el caudal másico de la bomba de compresión era constante e independiente de la naturaleza del refrigerante. Estos resultados le sugirieron una nueva posibilidad teórica, que, en lugar de utilizar un líquido fijo volátil, utilizar un líquido volátil capaz de descomponerse en dos o más líquidos volátiles, por el simple proceso de bajar la temperatura. En otras palabras, si fuera posible encontrar dos o más líquidos volátiles que se asociaran a altas temperaturas y se disociaran al bajar la temperatura, entonces la curva de presión de vapor de la mezcla sería totalmente diferente a la de los componentes puros. Según Pictet, la asociación del oxígeno con una molécula de un líquido volátil reduce su volatilidad y, por tanto, aumenta su punto de ebullición. La fijación del oxígeno por el líquido podía ser física o química, por disolución o por combinación.
Influencia en la fosforescencia
El objetivo de este trabajo era estudiar la acción específica de un gran descenso de la temperatura sobre el brillo de los cuerpos fosforescentes. Para ello, Pictet llenó un vaso con polvo de una sustancia fosforescente como el sulfuro de calcio, el sulfuro de bario y el sulfuro de estroncio, lo expuso a la luz del sol y luego a la oscuridad, y midió el tiempo transcurrido entre el brillo máximo y el mínimo.
Después, se expuso de nuevo el tubo a la luz solar y se introdujo de repente en un cilindro de vidrio de doble pared lleno de monóxido de nitrógeno a -140°C. Después de que el tubo se enfriara a unos -l00°C, se trasladó a un entorno oscuro. Pictet observó que, en estas condiciones, el material no emitía luz, pero a medida que el tubo empezaba a calentarse, el material volvía a adquirir su brillo normal, sin la ayuda de la luz externa y sin haber recibido ninguna influencia significativa de la luz difusa. Estos resultados fueron comunes a todas las sustancias estudiadas.
La siguiente etapa consistió en determinar el límite de temperatura para la extinción del brillo visible. El tubo estaba provisto de un termómetro, se exponía a la acción de la luz solar y luego se introducía en un baño refrigerante a -75°C situado en una cámara oscura. Pictet observó que la emitancia de la luz cesaba cuando la superficie del polvo alcanzaba una temperatura entre -60 y -70°C. Manteniendo los tubos en frío durante una media hora, y retirando el baño para dejar que se calentaran espontáneamente por radiación y en la oscuridad, el brillo y su intensidad volvían al valor original.
Pictet llegó a la conclusión de que la producción de fosforescencia luminiscente requería un cierto movimiento de las partículas que constituían los cuerpos. El enfriamiento a una temperatura suficientemente baja anulaba los movimientos calóricos oscilantes, impedía la generación de ondas luminosas y la fosforescencia desaparecía.
Regla de Pictet-Trouton
Los químicos, en particular los fisicoquímicos, conocen a Frederick Thomas Trouton (1863- 1922) a través de la llamada regla de Trouton que relaciona la entalpía de vaporización con la temperatura de cambio de fase. Trouton presentó sus ideas sobre el tema en los dos trabajos más breves que escribió, y cuando aún era estudiante universitario en el University College.
Estas publicaciones no contenían material experimental ni consideraciones teóricas. En el primero informaba de su hallazgo de que la relación entre el calor latente de vaporización (gasificación) dividido por el producto del volumen relativo del gas y el calor específico del cuerpo era aproximadamente 0,8 para los 24 compuestos para los que lo había calculado. El segundo artículo se abría con la afirmación alternativa de que al comparar las «cantidades de calor necesarias para evaporar a presión constante cantidades de diferentes líquidos tomadas en la relación de sus pesos moleculares, se encuentra que la cantidad de calor requerida por cualquier cuerpo es aproximadamente proporcional a su temperatura absoluta en el punto de ebullición» (hoy en día, regla de Trouton). Ilustró esta afirmación comparando el valor de esta cantidad para compuestos de la misma familia química, como los alcoholes (incluida el agua), los ácidos grasos, los yoduros orgánicos y los cloruros. En el caso de los ácidos grasos, consideró que sus densidades de vapor eran anormales.
La regla de Trouton se expresa en términos modernos de la siguiente manera
Un hecho interesante e inexplicable es que en sus dos publicaciones Trouton no hizo referencia alguna a una expresión muy similar desarrollada teóricamente por Raoul-Pierre Pictet ocho años antes. Pictet utilizó un ciclo de Carnot que opera dentro de la cúpula de saturación de líquido-vapor para demostrar que la relación αλ(274 + t) es una constante para todos los líquidos. En la ecuación de Pictet a es el peso atómico (los valores de los pesos moleculares utilizados por Pictet son la mitad de los actuales) y λ el calor latente interno (el calor necesario para separar dos moléculas).
Pictet observó que el calor latente externo (el calor latente común) era sensiblemente proporcional a α, por lo que su relación era válida tanto para el calor de vaporización externo como para el interno. También informó de que el valor del calor de vaporización por unidad de peso atómico para doce sustancias (agua, cloroformo, mercurio, acetona, benceno, etc.) variaba entre 10,17 y 12,35, lo que demostraba que todos los líquidos tenían esencialmente la misma cohesión y hacía suponer que sus relaciones permitirían calcular el diámetro real de los átomos con una precisión de una fracción de milímetro (!). Además, Pictet concluyó que los calores latentes de todos los líquidos debían ser múltiplos de sus calores específicos.
El análisis del ciclo de Carnot dentro de dos temperaturas muy clases llevó a Pictet a derivar la ecuación de Clausius Claperyon, tal y como la conocemos hoy en día d ln P/dT = λ/RT2. Por lo tanto, la comparación de sus dos relaciones le sugirió que la derivada d ln P/ dT debería ser constante para todos los líquidos a la misma temperatura y presión.
Para más información Raoul-Pierre Pictet-The liquefaction of oxygen and achievement of low temperatures