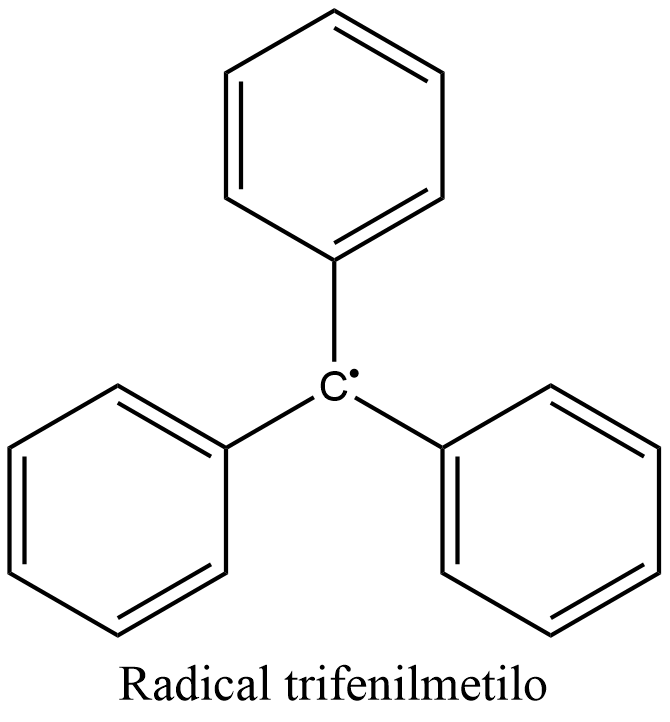
Radical trifenilmetilo
Tiempo de lectura estimado: 3 minutos
El radical trifenilmetilo (a menudo abreviado como radical tritílico) es un radical persistente y el primer radical jamás descrito en la química orgánica.
Historia
El radical fue descubierto por Moses Gomberg en 1900 en la Universidad de Michigan, quien trató de preparar hexafeniletano a partir de cloruro de trifenilmetilo y zinc en benceno en una reacción de Wurtz y descubrió que el producto, por su comportamiento frente al yodo y el oxígeno, era mucho más reactivo de lo previsto. La estructura descubierta se utilizó en el desarrollo de la espectroscopia ESR y fue confirmada por ésta.
La estructura quinoide correcta para el dímero fue sugerida ya en 1904, pero esta estructura fue abandonada poco después por la comunidad científica en favor del hexafeniletano. Posteriormente, tuvo que esperar hasta 1968 para su redescubrimiento, cuando los investigadores de la Vrije Universiteit Amsterdam publicaron datos de RMN de protones.
Preparación y propiedades
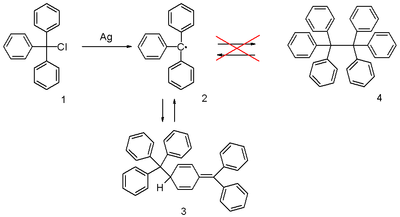
Puede prepararse mediante la homólisis del cloruro de trifenilmetilo 1 por un metal como la plata o el zinc en el benceno o el éter dietílico. El radical 2 forma un equilibrio químico con el dímero 3 de tipo quinoide (dímero de Gomberg). En el benceno la concentración del radical es del 2%.
Las soluciones que contienen el radical son amarillas; cuando se eleva la temperatura de la solución, el color amarillo se hace más intenso al desplazarse el equilibrio a favor del radical (de acuerdo con el principio de Le Châtelier).
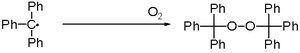
Cuando se expone al aire, el radical se oxida rápidamente al peróxido, y el color de la solución cambia de amarillo a incoloro. De igual manera, el radical reacciona con el yodo al yoduro de trifenilmetilo.
Mientras que el radical tritilico forma un dímero quinoide, los derivados del mismo con el patrón de sustitución apropiado forman dímeros con una estructura de hexafeniletano. Los estudios de rayos X dan una longitud de enlace de 1,67 Å para el hexakis(3,5-di-t-butilfenil)etano. Los cálculos teóricos de un nivel muy alto de teoría indican que la atracción de van der Waals entre los grupos terc-butil crean un mínimo potencial que está ausente en la molécula no sustituida.[2][3] Se ha informado de otros derivados como el dímero quinoide
Para más información Triphenylmethyl chloride | C19H15Cl – PubChem