Tiempo de lectura estimado: 8 minutos
El índigo (del griego antiguo ἰνδικόν indikón, la región de origen, la India Oriental) es un compuesto químico orgánico cristalino de color azul profundo. Es un pigmento orgánico con un alto poder de coloración y difícilmente soluble en agua.
El índigo es el nombre que recibe el grupo de colorantes índigoides, cuya estructura química está estrechamente relacionada con la de este compuesto.

Usos del índigo
El uso principal del índigo es como tinte para el hilo de algodón, que se utiliza principalmente para la producción de tela de vaqueros. En promedio, un par de pantalones vaqueros requiere de 3 a 12 g de este compuesto. Se utilizan pequeñas cantidades para teñir la lana y la seda.
El carmín de índigo, o índigo, es un derivado del índigo que también se utiliza como colorante. Cerca de 20 mil toneladas son producidas anualmente, de nuevo principalmente para blue jeans. También es usado como colorante de alimentos, y está listado en los Estados Unidos como FD&C Blue No. 2.
Fuentes naturales del índigo
A lo largo de la historia, una variedad de plantas ha proporcionado el índigo, pero la mayor parte del índigo natural se obtuvo de las del género Indigofera, que son nativas de los trópicos, en particular del subcontinente indio. La principal especie comercial en Asia fue el verdadero índigo (Indigofera tinctoria, también conocido como I. sumatrana).

Una alternativa común utilizada en los lugares subtropicales relativamente más fríos, como las islas Ryukyu del Japón y Taiwán, es el Strobilanthes cusia. La lenteja de nudo (Polygonum tinctorum) era el tinte azul más importante en Asia oriental hasta la llegada de las especies de Indigofera del sur, que producen más tinte.
En América Central y del Sur, la especie que se cultiva es el añil. En Europa se utilizaba para la tintura azul la lana que contenía el mismo tinte. Varias plantas contienen los precursores de este colorante, pero las bajas concentraciones hacen que sea difícil trabajar con ellas y que el color se contamine más fácilmente con otras sustancias tintóreas, lo que suele dar lugar a un tinte verdoso.
Bioquímica
El precursor del índigo es el indicán, un derivado incoloro y soluble en agua del aminoácido triptófano. El indicán se hidroliza fácilmente para liberar β-D-glucosa e indoxilo. La oxidación por exposición al aire convierte el indoxilo en indigotina, el químico azul insoluble que es el punto final del compuesto.

El indican era obtenido a partir del procesamiento de las hojas de la planta, que contienen hasta 0,2-0,8% de este compuesto. Las hojas se empaparon en agua y se fermentaron para convertir el glicósido indica presente en la planta en el colorante azul indigotina, que se precipita de la solución de la hoja fermentada cuando se mezcla con una base fuerte como la lejía, se presiona en pasteles, se seca y se pulveriza. El polvo se mezclaba entonces con otras sustancias para producir diferentes tonos de azul y púrpura.
Otras fuentes naturales
Las fuentes naturales también incluyen los moluscos. Los caracoles marinos Murex producen una mezcla de índigo y 6,6′-dibromoíndigo (rojo) que juntos producen una gama de matices púrpuras conocidos como púrpura de Tiro. La exposición a la luz durante una parte del proceso de muerte puede convertir el dibromoíndigo en añil, lo que da como resultado tonos azules conocidos como azul real, púrpura jacinto o tekhelet.
Síntesis del índigo
Dada su importancia económica, el índigo ha sido preparado por muchos métodos. La síntesis de Baeyer-Drewson data de 1882. Se trata de una condensación de aldol de o-nitrobenzaldehído con acetona, seguida de una ciclización y una dimerización oxidativa al índigo. Esta ruta es muy útil para obtener índigo y muchos de sus derivados a escala de laboratorio, pero no era práctica para la síntesis a escala industrial.

Johannes Pfleger y Karl Heumann llegaron finalmente a la síntesis para producción industrial en masa. La primera ruta comercialmente práctica se atribuye a Pfleger en 1901. En este proceso, la N-fenilglicina se trata con una mezcla fundida de hidróxido de sodio, hidróxido de potasio y sodamida.
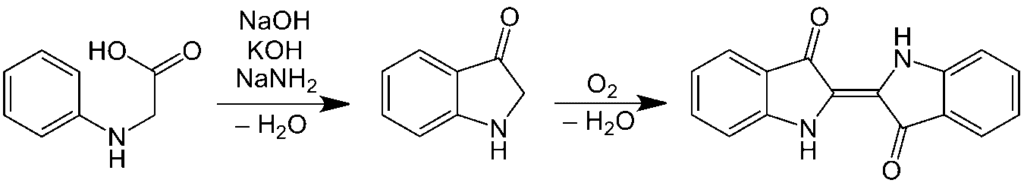
Este fundido altamente sensible produce indoxilo, que posteriormente se oxida en el aire para formar índigo. Las variaciones de este método se siguen utilizando hoy en día. Una ruta alternativa y también viable para el índigo se atribuye a Heumann en 1897. Consiste en calentar la N-(2-carboxifenil) glicina a 200 °C (392 °F) en una atmósfera inerte con hidróxido de sodio.
El proceso es más fácil que el método Pfleger, pero los precursores son más caros. Se genera el ácido indoxil-2-carboxílico. Este material se descarboxila fácilmente para dar indoxilo, que se oxida en el aire para formar la molécula. La preparación del tinte de índigo se practica en las clases de laboratorio de la universidad según la ruta original de Baeyer-Drewsen.
Propiedades químicas y físicas
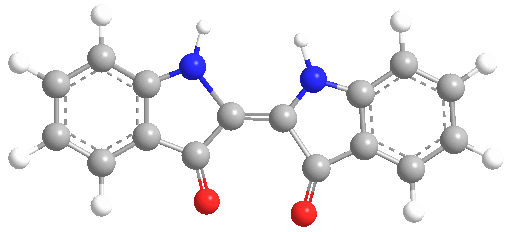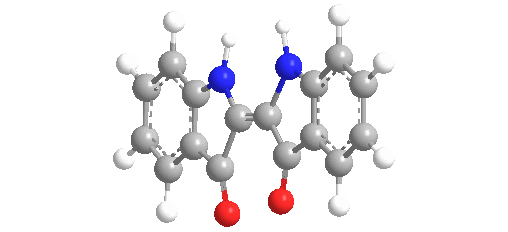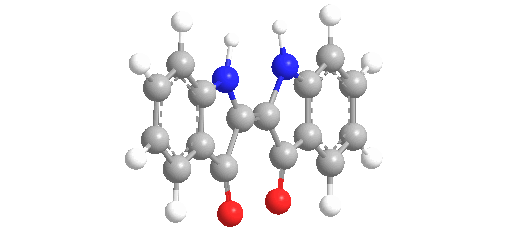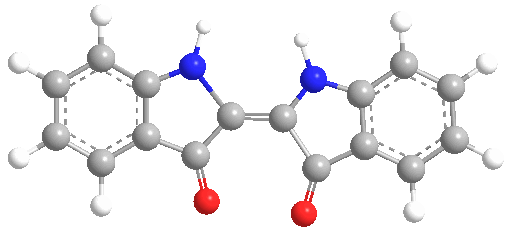
El tinte índigo es un polvo cristalino azul oscuro que se sublima a 390-392 °C (734-738 °F). Es insoluble en agua, alcohol o éter, pero soluble en DMSO, cloroformo, nitrobenceno y ácido sulfúrico concentrado. La fórmula química del índigo es C16H10N2O2.
La molécula absorbe la luz en la parte naranja del espectro (λmax = 613 nm). El compuesto debe su profundo color a la conjugación de los dobles enlaces, es decir, los dobles enlaces dentro de la molécula son adyacentes y la molécula es plana. En el blanco índigo, la conjugación se interrumpe porque la molécula no es plana.
Derivados del índigo
Los anillos de benceno en el índigo pueden ser modificados para dar una variedad de colorantes relacionados. El thioíndigo, donde los dos grupos de NH son reemplazados por átomos de S, es de color rojo intenso.
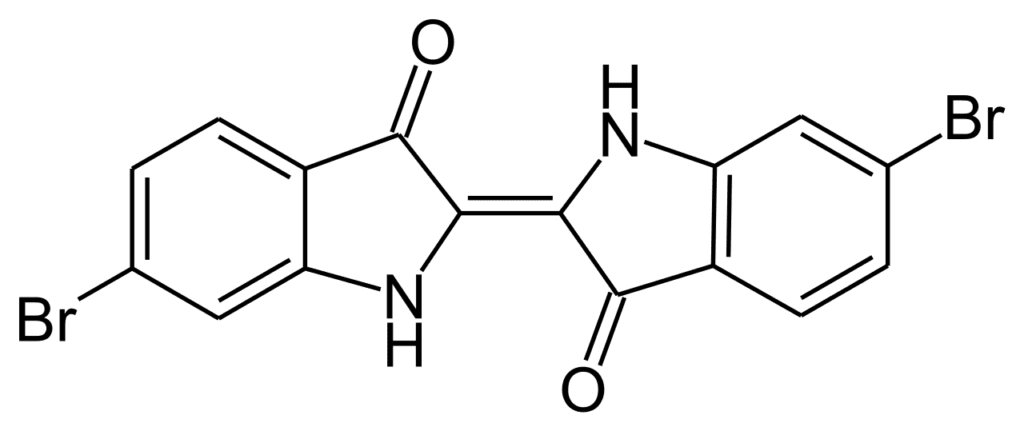
El púrpura tirio es un colorante púrpura apagado que es secretado por un caracol común del Mediterráneo. Fue muy apreciado en la antigüedad. En 1909, se demostró que su estructura era de 6,6′-dibromoíndigo (rojo). El 6-bromoíndigo (púrpura) también es un componente. Nunca se ha producido de forma comercial. Sin embargo, el azul de Ciba relacionado (5,7,5′,7′-tetrabromoindigo) tiene un valor comercial.

El índigo y sus derivados que presentan un enlace de hidrógeno intra e intermolecular tienen una solubilidad muy baja en los solventes orgánicos. Pueden hacerse solubles usando grupos protectores transitorios como el grupo tBOC, que suprime el enlace intermolecular El calentamiento del índigo tBOC da como resultado una eficiente desprotección térmica y la regeneración del pigmento padre enlazado con H.
El tratamiento con ácido sulfúrico convierte el índigo en un derivado verde azulado llamado carmín índigo (índigo sulfonado). Estuvo disponible a mediados del siglo XVIII. Se utiliza como colorante para alimentos, productos farmacéuticos y cosméticos.
Para más información «Indigo Dyeing»
Como citar este artículo:
APA: (2020-11-24). Índigo. Recuperado de https://quimicafacil.net/compuesto-de-la-semana/indigo/
ACS: . Índigo. https://quimicafacil.net/compuesto-de-la-semana/indigo/. Fecha de consulta 2026-02-27.
IEEE: , "Índigo," https://quimicafacil.net/compuesto-de-la-semana/indigo/, fecha de consulta 2026-02-27.
Vancouver: . Índigo. [Internet]. 2020-11-24 [citado 2026-02-27]. Disponible en: https://quimicafacil.net/compuesto-de-la-semana/indigo/.
MLA: . "Índigo." https://quimicafacil.net/compuesto-de-la-semana/indigo/. 2020-11-24. Web.
Si tiene alguna pregunta o sugerencia, escribe a administracion@quimicafacil.net, o visita Como citar quimicafacil.net