Tiempo de lectura estimado: 5 minutos
La síntesis de fenolftaleína es una práctica que permite al estudiante acercarse a la reacciones de condensación, así como a la extracción liquido – liquido.
Características de la fenolftaleína
La fenolftaleína es uno de los indicadores de más uso a nivel laboratorio, aunque sus aplicaciones abarcan más allá del ámbito científico. El uso común de la fenolftaleína es como indicador en las valoraciones ácido-base. También sirve como componente del indicador universal, junto con el rojo de metilo, el azul de bromotimol y el azul de timol.
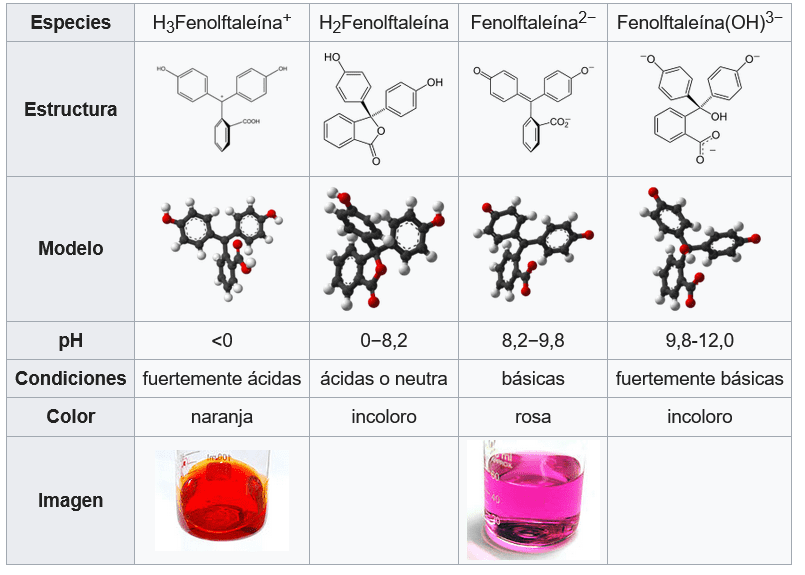
La fenolftaleína adopta cuatro estados diferentes en solución acuosa: En condiciones fuertemente ácidas, existe en forma protonada (HIn+), proporcionando una coloración naranja. Entre las condiciones fuertemente ácidas y ligeramente básicas, la forma de lactona (HIn) es incolora. La forma de fenolato doblemente desprotonado (In2-) (la forma aniónica del fenol) da el color rosado familiar.
En soluciones fuertemente básicas, la fenolftaleína se convierte a su forma In(OH)3-, y su color rosado sufre una reacción de desvanecimiento bastante lenta y se vuelve completamente incolora por encima de 13.0 pH.
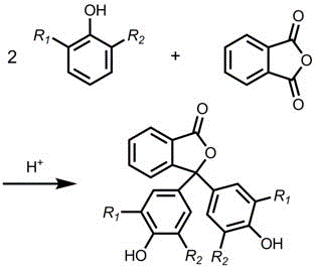
En esta práctica, la síntesis de la fenolftaleína se realiza empleando ácido p-toluenesulfónico como catalizador para mejorar el experimento, junto con un procedimiento de extracción ácido-base del producto fenolftaleína. Además, siguiendo el mismo procedimiento, pero cambiando el fenol por 2,6 dimetilfenol, es posible preparar un análogo de la fenolftaleína.
Materiales
- Balón de fondo redondo de 30 mL
- Baño de aceite
- Soporte universal
- Condensador recto
- Agitador magnético
- Embudo de separación de 50 mL
- 3 Erlenmeyer de 50 mL
- Montaje de filtración al vacío
Reactivos
- Fenol
- anhídrido ftálico
- ácido p-toluenosulfónico monohidratado
- Diclorometano
- Solución de hidróxido de sodio 2M
- Solución de ácido clorhídrico 2M
Procedimiento
Tiempo necesario: 4 horas
Pasos para la síntesis de fenolftaleína
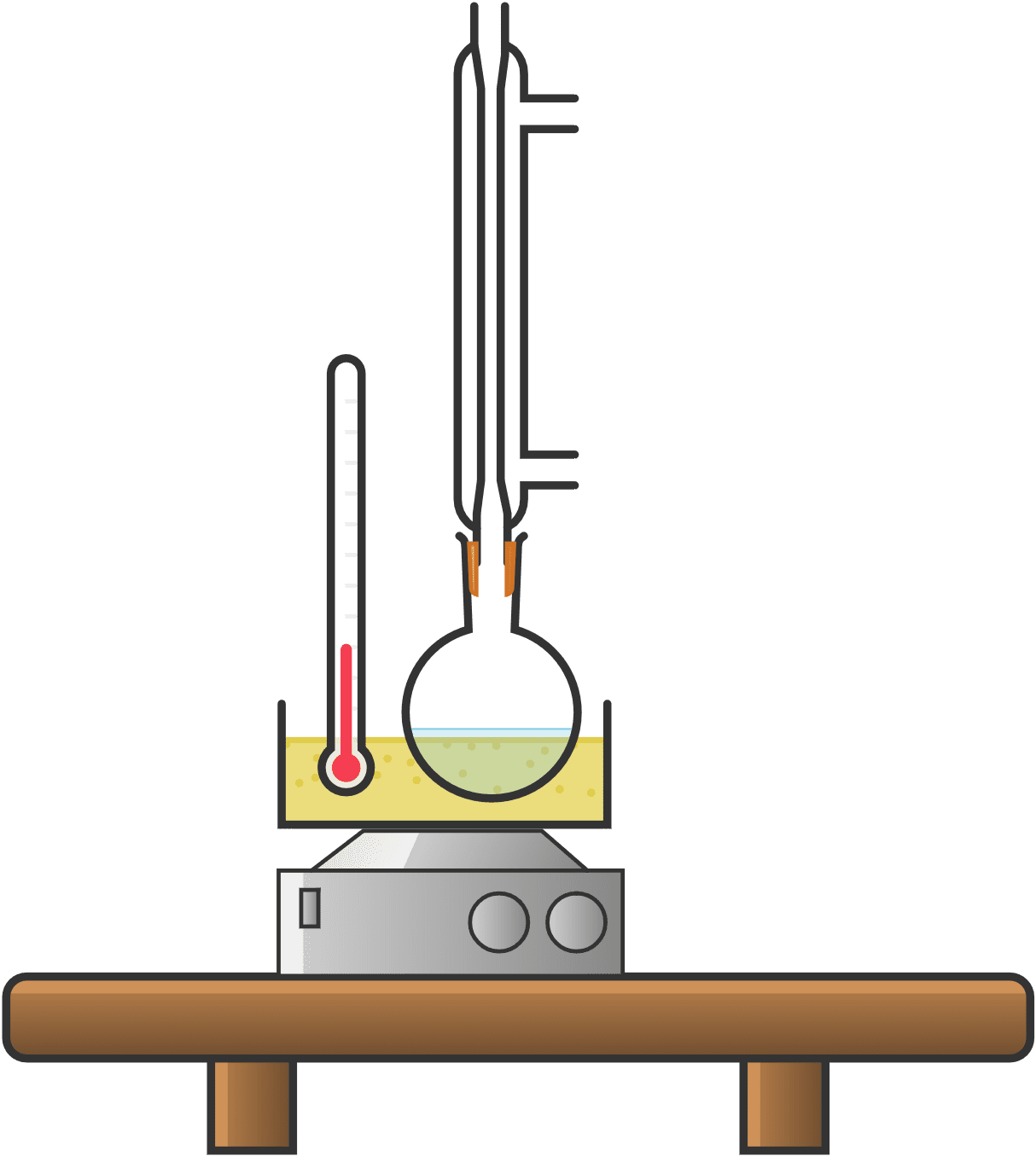
Realizar el siguiente montaje de reacción con reflujo empleando el baño de aceite, el balón de fondo redondo de 30 mL, condensador recto y termómetro.

Colocar una mezcla de fenol (2,0 g: 21 mmol), anhídrido ftálico (1,5 g: 10 mmol) y ácido p-toluenosulfónico monohidratado (190 mg: 1 mmol) en el balón de fondo redondo de 30 ml provisto de una barra agitadora magnética.
La mezcla de reacción se calienta a 150ºC durante 3 horas con agitación continua. Después de enfriarse a temperatura ambiente, se añadieron 10 mL de agua y 10 mL de diclorometano en el balón, y luego la solución resultante se transfirió a un embudo de separación de 50 mL.
La extracción de la fenolftaleína obtenida sigue el esquema que se muestra en la siguiente figura. La capa orgánica inferior se transfiere a un Erlenmeyer de 50 mL. A la capa acuosa restante se extrae posteriormente con 10 mL de diclorometano y la capa orgánica separada se transfiere a el mismo Erlenmeyer.
AnuncioLa capa orgánica combinada que se obtiene se devuelve al embudo de separación vacío y se alcaliniza mediante la adición de 5 mL de solución de hidróxido de sodio 2M. Después diluir el extracto con 10 mL de agua y separar la capa orgánica inferior
Retirar la capa acuosa superior de la parte superior del embudo de separación y transferir a otro Erlenmeyer de 50 mL.
La solución acuosa se acidifica con 5 mL de solución de ácido clorhídrico 2M para aislar la fenolftaleína como fibras musgosas blancas, las cuales se separan por filtración al vacío. Se espera un rendimiento aproximado de 735 mg (22%).

Después del experimento
Pesar el producto obtenido y estimar su rendimiento real en comparación al rendimiento teórico reportado en la práctica.
Comprobar el punto de fusión del producto obtenido y compararlo con el reportado en la literatura.
Recomendaciones de seguridad
En todo momento se deben utilizar los elementos de seguridad básicos en el laboratorio de química (bata de laboratorio, guantes, gafas de seguridad y demás que sean exigidos por las normas internas, locales o nacionales. Los residuos generados por la práctica deben ser dispuestos de manera adecuada según las normas de laboratorio y las normas locales y nacionales respectivas.
Para más información Phenolphthalein as Organic Teaching Materials