Estimated reading time: 8 minutos
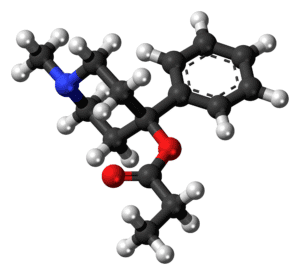
La MPPP, cuyo nombre sistemático es 1-metil-4-fenil-4-propionoxipiperidina, también conocida como desmetilprodina, es un opioide sintético con efectos analgésicos similares a los de la morfina o la petidina. Químicamente, es un análogo y un isómero estructural del conocido analgésico petidina (meperidina).
Aunque fue sintetizada por primera vez en la década de 1940 durante la investigación farmacéutica legítima, la MPPP es tristemente célebre no por su valor terapéutico, sino por su papel central en uno de los episodios más trágicos y, a la vez, científicamente reveladores de la historia de las drogas de diseño.
Un error en su síntesis clandestina en la década de 1970 y 1980 condujo a la formación de una impureza devastadoramente tóxica, el MPTP. La ingestión de esta sustancia provocó en un grupo de jóvenes una forma severa e irreversible de parkinsonismo, dejándolos en un estado «congelado».
Esta tragedia humana, sin embargo, abrió una ventana inesperada hacia la comprensión de la enfermedad de Parkinson, proporcionando a los científicos el primer modelo animal perfecto de la enfermedad y revolucionando la investigación sobre sus causas y posibles tratamientos.
Historia y Síntesis Original
La MPPP fue sintetizada y reportada por primera vez en 1947 por los químicos Albert Ziering y John Lee, quienes trabajaban para la compañía farmacéutica Hofmann-La Roche. En esa época, la investigación se centraba en encontrar nuevos analgésicos opioides que pudieran replicar los potentes efectos de la morfina, pero con un menor potencial de adicción y menos efectos secundarios.
La MPPP es un isómero de la petidina (meperidina), el primer opioide totalmente sintético, y se la conoce a veces como «petidina invertida» porque el grupo éster en su estructura está en una orientación opuesta.
La síntesis original es un proceso de dos pasos:
- Adición Nucleofílica: Se hace reaccionar 1-metil-4-piperidona con fenillitio, un reactivo de organolitio. El anión fenilo, altamente nucleofílico, ataca al carbono carbonílico de la piperidona, formando un alcohol terciario intermediario (1-metil-4-fenilpiperidin-4-ol o PMP-OH).
- Esterificación: El alcohol intermediario se esterifica haciéndolo reaccionar con anhídrido propiónico. Esto reemplaza el grupo hidroxilo (-OH) con un grupo propionato (-OOCCH₂CH₃), dando como producto final la MPPP.
En las pruebas farmacológicas iniciales en ratas, la MPPP demostró tener actividad analgésica pero no ofreció ninguna ventaja sobre los analgésicos ya existentes, por lo que nunca fue comercializada y quedó relegada a la literatura química.
$ text{1-metil-4-piperidona} + text{Fenillitio} rightarrow text{PMP-OH} xrightarrow{text{Anhídrido Propiónico}} text{MPPP} $
El Desastre de las Drogas de Diseño: El MPTP
El concepto de «droga de diseño» se refiere a una sustancia creada modificando ligeramente la estructura de una droga controlada para eludir las leyes existentes, manteniendo o incluso potenciando sus efectos. La historia de la MPPP se convirtió en el ejemplo más terrible de los peligros de esta práctica.
El Caso de Barry Kidston (1976)
En 1976, Barry Kidston, un estudiante de posgrado en química de 23 años en Maryland y consumidor de drogas buscó en la literatura científica un opioide que no estuviera en las listas de sustancias controladas. Encontró el artículo de 1947 sobre la MPPP y decidió sintetizarla para su propio uso. Sus primeros lotes fueron exitosos y le proporcionaron el efecto eufórico que buscaba.
Sin embargo, en un intento posterior, parece que tomó atajos en el procedimiento, probablemente aplicando un exceso de calor o permitiendo que las condiciones se volvieran ácidas durante la esterificación. Estas condiciones favorecen una reacción secundaria de eliminación (deshidratación) del alcohol intermediario, en lugar de la esterificación deseada. El resultado fue la formación de un subproducto oleoso: 1-metil-4-fenil-1,2,3,6-tetrahidropiridina, o MPTP.
Pocos días después de inyectarse este lote contaminado, Kidston desarrolló síntomas neurológicos graves: rigidez muscular extrema, temblores, lentitud de movimientos y mutismo. Fue diagnosticado con catatonia e ingresado en una unidad psiquiátrica. Un neurólogo finalmente reconoció los síntomas como un caso agudo de enfermedad de Parkinson, algo prácticamente inaudito en una persona tan joven.
Aunque fue tratado con Levodopa (L-DOPA), el fármaco estándar para el Parkinson, y experimentó una mejora parcial, nunca se recuperó por completo y continuó abusando de las drogas hasta su muerte por sobredosis en 1978. El análisis post-mortem de su cerebro reveló una destrucción masiva de las neuronas productoras de dopamina en una región llamada sustancia negra, la misma patología que define a la enfermedad de Parkinson.
Los «Adictos Congelados» de California (1982)
El caso de Kidston fue publicado en una revista de psiquiatría en 1979 pero pasó en gran medida desapercibido. La historia resurgió de forma dramática en 1982, cuando el Dr. J. William Langston, un neurólogo del Santa Clara Valley Medical Center en California se encontró con una serie de casos desconcertantes. En pocas semanas, varios jóvenes consumidores de heroína fueron ingresados en hospitales locales en un estado «congelado», incapaces de moverse o hablar, pero plenamente conscientes.
Langston y su equipo, en un brillante trabajo de investigación médica, conectaron los casos y descubrieron que todas las víctimas habían consumido un «nuevo tipo de heroína sintética» procedente del mismo productor clandestino. Alguien en el equipo recordó el oscuro caso de Barry Kidston. Al analizar muestras de la droga callejera, confirmaron sus sospechas: era un lote de MPPP mal sintetizado que consistía casi en su totalidad en la impureza MPTP.
Neurotoxicología: El Mecanismo de Acción del MPTP
La tragedia de los «adictos congelados» desencadenó una intensa investigación que desveló el preciso y devastador mecanismo por el cual el MPTP destruye las neuronas dopaminérgicas.
- Cruce de la Barrera Hematoencefálica: El MPTP es una molécula lipofílica (soluble en grasas), lo que le permite atravesar fácilmente la barrera hematoencefálica y entrar en el cerebro.
- Conversión a MPP⁺: Una vez en el cerebro, el MPTP es metabolizado por la enzima monoamino oxidasa B (MAO-B), presente en las células gliales. Esta enzima oxida el MPTP, convirtiéndolo en el ion 1-metil-4-fenilpiridinio (MPP⁺). El MPP⁺ es la verdadera molécula neurotóxica.
- Captación Selectiva por Neuronas Dopaminérgicas: Aquí radica la especificidad de su toxicidad. El ion MPP⁺ tiene una estructura química muy similar a la de la dopamina. Como resultado, es «confundido» con la dopamina por el transportador de dopamina (DAT), una proteína especializada que se encuentra en la membrana de las neuronas dopaminérgicas y cuya función es recapturar la dopamina del espacio sináptico. El DAT bombea activamente el MPP⁺ hacia el interior de estas neuronas, concentrando el veneno precisamente en las células que va a destruir.
- Toxicidad Mitocondrial: Una vez dentro de la neurona, el MPP⁺ se acumula en las mitocondrias, las centrales energéticas de la célula. Allí, ejerce su efecto letal al inhibir específicamente el Complejo I de la cadena de transporte de electrones. Este bloqueo tiene dos consecuencias catastróficas:
- Colapso Energético: La producción de ATP se detiene, privando a la neurona de la energía necesaria para sobrevivir.
- Estrés Oxidativo Masivo: La inhibición del Complejo I provoca una «fuga» de electrones que reaccionan con el oxígeno para formar radicales libres y especies reactivas de oxígeno, causando un daño celular masivo.
La combinación de la falta de energía y el daño oxidativo conduce a la muerte rápida y selectiva de las neuronas dopaminérgicas de la sustancia negra, replicando la patología central de la enfermedad de Parkinson.
El Legado Científico: Una Revolución en la Investigación del Parkinson
El descubrimiento del MPTP, a pesar de su trágico origen, fue uno de los avances más importantes en la historia de la neurología.
El Modelo Animal Perfecto
Antes del MPTP, no existía un buen modelo animal para la enfermedad de Parkinson. Los investigadores luchaban por replicar la pérdida selectiva de neuronas dopaminérgicas en animales. Se descubrió que, mientras que las ratas y los ratones son resistentes al MPTP, los primates (como los monos) son susceptibles y desarrollan síntomas y patología casi idénticos a los de la enfermedad de Parkinson humana. Esto proporcionó a la ciencia, por primera vez, un modelo fiable para:
- Estudiar la progresión de la enfermedad.
- Probar la eficacia de nuevos fármacos neuroprotectores.
- Desarrollar y perfeccionar terapias sintomáticas como la L-DOPA.
- Experimentar con tratamientos revolucionarios como los trasplantes de tejido fetal (que se realizaron en algunas de las víctimas originales del MPTP) y la estimulación cerebral profunda.
Implicaciones para la Causa de la Enfermedad de Parkinson
El MPTP demostró de manera concluyente que una toxina ambiental podía causar parkinsonismo. Esto dio un impulso masivo a la hipótesis de que la exposición a ciertas sustancias químicas en el medio ambiente podría ser un factor de riesgo para el desarrollo de la enfermedad de Parkinson idiopática (de causa desconocida).
La atención se centró rápidamente en la similitud estructural entre el ion tóxico MPP⁺ y el herbicida paraquat. Numerosos estudios epidemiológicos han explorado desde entonces esta conexión, sugiriendo que la exposición crónica a ciertos pesticidas y herbicidas podría aumentar el riesgo de desarrollar Parkinson, aunque la relación causal exacta sigue siendo un área de intensa investigación.
En conclusión, la historia de la MPPP y el MPTP es una poderosa lección sobre los peligros imprevistos de la química clandestina y la importancia de la pureza en las síntesis. La tragedia de un puñado de individuos catalizó décadas de avances científicos, transformando nuestra comprensión de una de las enfermedades neurodegenerativas más comunes y ofreciendo nuevas esperanzas para su tratamiento.