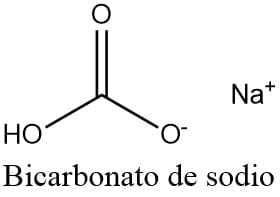
Bicarbonato de sodio
Actualizado en septiembre 15, 2021
Tiempo de lectura estimado: 3 minutos
El bicarbonato de sodio, también llamado hidrogenocarbonato de sodio, carbonato ácido de sodio o polvo para hornear, es una sal del ácido carbónico de apariencia cristalina blanca, generalmente manejado en forma de polvo blanco. Tiene un sabor ligeramente salino y alcalino.
Propiedades del bicarbonato
Químicamente, es una sustancia anfótera que al ser disuelta en agua genera soluciones ligeramente alcalinas debido a la formación de ácido carbónico y la liberación de un ion hidróxido. En presencia de ácidos orgánicos reacciona para dar la sal sódica correspondiente del ácido y liberando dióxido de carbono. Con sustancias básicas produce carbonatos y libera una molécula de agua.
A temperaturas mayores de 200°C el bicarbonato se descompone en carbonato de sodio, agua y dióxido de carbono. Si se prosigue el calentamiento hasta 850°C se obtiene oxido de sodio y liberación de dióxido de carbono. Estas reacciones son la base del uso del bicarbonato de sodio como agente supresor de fuego en extintores de tipo BC de polvo químico seco.
Historia y usos
El químico francés Nicolas Leblanc sintetizo el bicarbonato de sodio en 1791, llamándolo ceniza sódica (soda ash). El uso de esta sal en la industria de alimentos se debe a que, en presencia de un ácido orgánico y/o calor, reacciona liberando dióxido de carbono, que genera finas burbujas en la masa que al ser cocinada se expanden y dan una textura suave y uniforme al producto.
Actualmente, el polvo para hornear contiene cerca de 30% de bicarbonato de sodio y el porcentaje restante son ácidos orgánicos débiles en polvo (fosfato acido de calcio, fosfato sódico de aluminio, bitartrato de potasio) que promueven la generación de dióxido. Anteriormente se empleaba como fuente de dióxido de carbono en bebidas carbonatadas.
Otros usos del bicarbonato de sodio incluyen el control de crecimiento de moho, estabilizador y ajustador de pH en bebidas, pirotecnia, desinfectante suave y antiácido en caso de ingesta accidental de ácidos entre otros.
Como dato curioso, Groucho Marx incluía mucho el bicarbonato de sodio en sus líneas en las películas de los hermanos Marx, en la película Duck Soup de 1933, Groucho interpreta al líder de una nación en guerra, y recibe un mensaje del frente alertándolo de un ataque con gas, respondiéndole a su ayudante que le diga a su general que “tome una cucharada de bicarbonato de sodio y medio vaso de agua”
Para más información Sodium bicarbonate | NaHCO3 – PubChem
Como citar este artículo:
APA: (2019-10-08). Bicarbonato de sodio. Recuperado de https://quimicafacil.net/compuesto-de-la-semana/bicarbonato-de-sodio/
ACS: . Bicarbonato de sodio. https://quimicafacil.net/compuesto-de-la-semana/bicarbonato-de-sodio/. Fecha de consulta 2024-05-11.
IEEE: , "Bicarbonato de sodio," https://quimicafacil.net/compuesto-de-la-semana/bicarbonato-de-sodio/, fecha de consulta 2024-05-11.
Vancouver: . Bicarbonato de sodio. [Internet]. 2019-10-08 [citado 2024-05-11]. Disponible en: https://quimicafacil.net/compuesto-de-la-semana/bicarbonato-de-sodio/.
MLA: . "Bicarbonato de sodio." https://quimicafacil.net/compuesto-de-la-semana/bicarbonato-de-sodio/. 2019-10-08. Web.
Si tiene alguna pregunta o sugerencia, escribe a administracion@quimicafacil.net, o visita Como citar quimicafacil.net