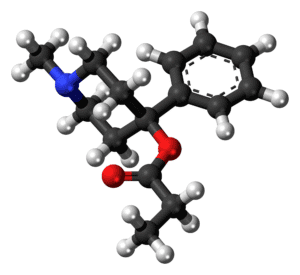
Ferroceno
Tiempo de lectura estimado: 8 minutos
El ferroceno es un compuesto organometálico con la fórmula Fe(C5H5)2. La molécula consiste en dos anillos de ciclopentadienilo unidos en lados opuestos de un átomo de hierro central. Es un sólido anaranjado con un olor parecido al alcanfor, que se sublima por encima de la temperatura ambiente, y es soluble en la mayoría de los disolventes orgánicos.
Es notable por su estabilidad: no se ve afectado por el aire, el agua, las bases fuertes, y puede ser calentado hasta 400 °C sin descomponerse. En condiciones de oxidación puede reaccionar reversiblemente con ácidos fuertes para formar el catión de ferroceno Fe(C5H5)2+.
El rápido crecimiento de la química organometálica se atribuye a menudo a la excitación surgida del descubrimiento del ferroceno y sus numerosos análogos (metalocenos).
Historia del ferroceno
El ferroceno fue descubierto por accidente. La primera síntesis conocida puede haber sido hecha a finales de los años 40 por investigadores desconocidos de la Union Carbide, quienes trataron de pasar vapor caliente de ciclopentadieno a través de un tubo de hierro. El vapor reaccionó con la pared del tubo, creando un «lodo amarillo» que obstruyó el tubo. Años más tarde, una muestra del lodo que se había guardado fue recuperada y analizada por E. Brimm, poco después de leer el artículo de Kealy y Pauson, y encontró que consistía en ferroceno.
La segunda vez fue alrededor de 1950, cuando S. Miller, J. Tebboth y J. Tremaine, investigadores de British Oxygen, intentaban sintetizar aminas a partir de hidrocarburos y nitrógeno en una modificación del proceso de Haber. Cuando intentaron hacer reaccionar el ciclopentadieno con nitrógeno a 300°C, a presión atmosférica, ellos se decepcionaron cuando el hidrocarburo reaccionó con alguna fuente de hierro, sintetizando el ferroceno.

Aunque ellos también observaron su notable estabilidad, dejaron la observación a un lado y no la publicaron hasta después de que Pauson informara de sus hallazgos. De hecho, Kealy y Pauson recibieron una muestra de Miller y otros, quienes confirmaron que los productos eran el mismo compuesto.
En 1951, Peter L. Pauson y Thomas J. Kealy de la Universidad de Duquesne intentaron preparar la fulvalina ((C5H4)2) por dimerización oxidativa del ciclopentadieno (C5H6). Para ello, reaccionaron el compuesto de Grignard bromuro de ciclopentadienilmagnesio en éter dietílico con cloruro férrico como oxidante, pero en lugar del fulvaleno esperado, obtuvieron un polvo naranja claro de «notable estabilidad», con la fórmula C10H10Fe.
Determinación de la estructura
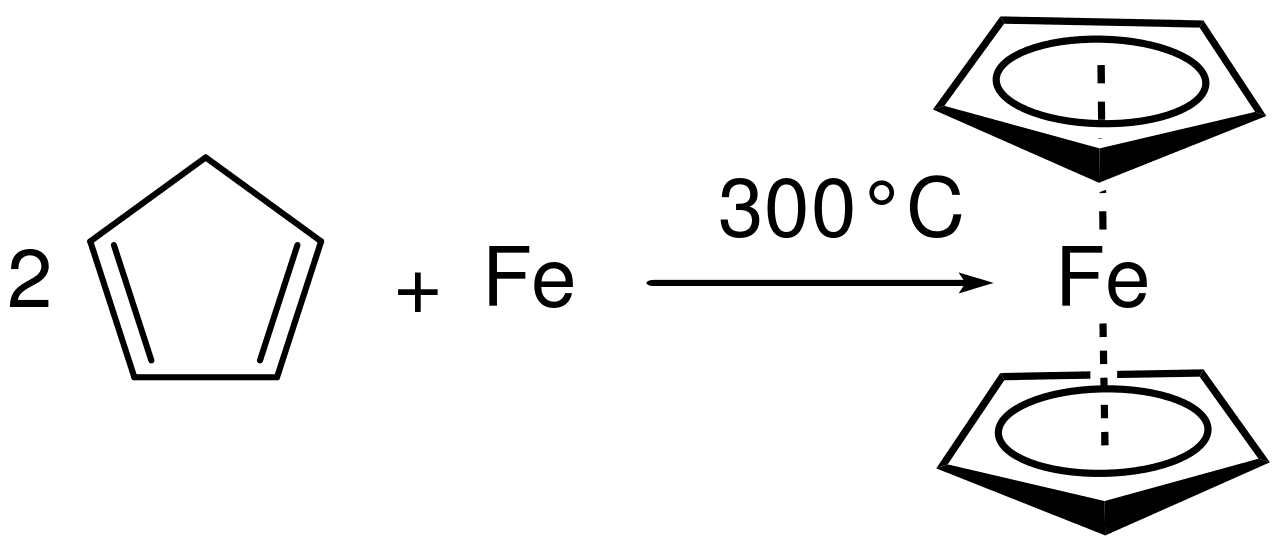
Pauson y Kealy conjeturaron que el compuesto tenía dos grupos de ciclopentadienilo, cada uno con un solo enlace covalente desde el átomo de carbono saturado hasta el átomo de hierro. Sin embargo, esa estructura era inconsistente con los modelos de enlace existentes en ese momento y no explicaba la inesperada estabilidad del compuesto, y los químicos se esforzaron por encontrar la estructura correcta.
La estructura fue deducida y reportada independientemente por tres grupos en 1952:
- Woodward y Wilkinson del Imperial College London lo dedujeron observando que el ferroceno sufría reacciones típicas de compuestos aromáticos como el benceno.
- E. Fischer, de la Universidad Técnica de Múnich, dedujo la estructura (a la que llamó «doble cono») y también comenzó a sintetizar otros metalocenos como el níqueloceno y el cobaltoceno.
- P. F. Eiland y R. Pepinsky confirmaron la estructura mediante cristalografía de rayos X y posteriormente mediante RMN.
La estructura de «sándwich» del ferroceno era sorprendentemente novedosa, y requería una nueva teoría para explicarla. La aplicación de la teoría de la órbita molecular con la suposición de un centro de Fe2+ entre dos aniones ciclopentadienos C5H5– dio como resultado el exitoso modelo Dewar-Chatt-Duncanson, permitiendo la correcta predicción de la geometría de la molécula, así como explicando su notable estabilidad.
Síntesis del ferroceno
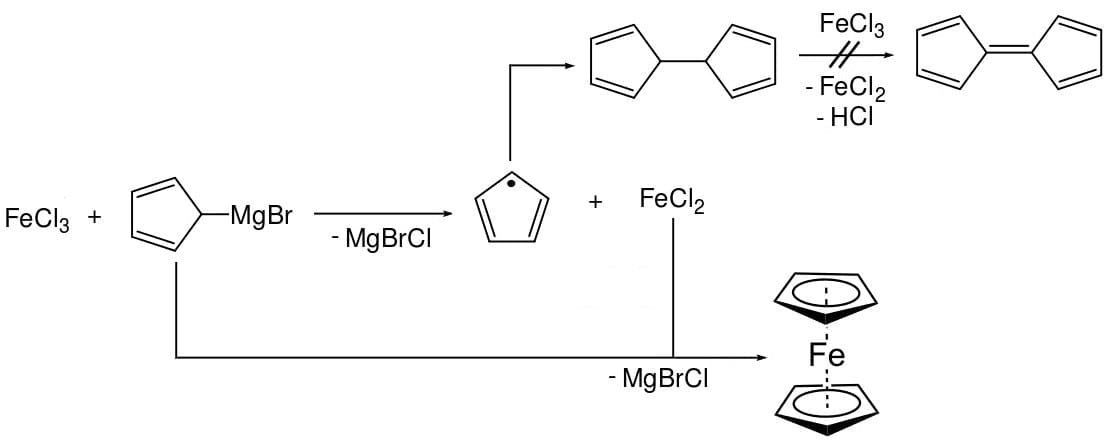
Las primeras síntesis reportadas de ferroceno fueron casi simultáneas. Pauson y Kealy sintetizaron el ferroceno utilizando cloruro de hierro (III) y un reactivo de Grignard, bromuro de ciclopentadienilmagnesio.
El cloruro de hierro (III) se suspende en éter dietílico anhidro y se agrega al reactivo de Grignard. Se produce una reacción redox que forma el radical ciclopentadienilo y los iones de hierro (II). El dihidrofulvaleno se produce por recombinación radical-radical mientras que el hierro (II) reacciona con el reactivo de Grignard para formar ferroceno. La oxidación de dihidrofulvaleno a fulvaleno con hierro (III), el resultado buscado por Kealy y Pauson, no ocurre.
Síntesis vía ciclopentadieno alcalino
Los métodos preparatorios más eficientes son generalmente una modificación de la secuencia de transmutación original que utiliza ya sea ciclopentadieno de sodio disponible comercialmente o ciclopentadieno recién desprotonado con hidróxido de potasio y reaccionado con cloruro de hierro (II) anhidro en solventes etéreos.
Se conocen las siguientes modificaciones modernas del enfoque original de Pauson y Kealy de Grignard:
Usando ciclopentadieno de sodio

Usando ciclopentadieno recién protonado

Usando una sal de hierro (II) con un reactivo de Grignard

Incluso algunas bases amínicas (como la dietilamina) pueden utilizarse para la desprotonación, aunque la reacción procede más lentamente que cuando se utilizan bases más fuertes:

La transmetalación directa también puede ser utilizada para preparar el ferroceno de otros metallocenos, como el manganoceno:

Propiedades
El ferroceno es un sólido anaranjado estable en el aire con un olor parecido al alcanfor. Como se espera de una especie simétrica y sin carga, el ferroceno es soluble en solventes orgánicos normales, como el benceno, pero es insoluble en el agua. Es estable a temperaturas tan altas como 400 °C.
El ferroceno se sublima fácilmente, especialmente cuando se calienta en el vacío. Su presión de vapor es de aproximadamente 1 Pa a 25 °C, 10 Pa a 50 °C, 100 Pa a 80 °C, 1000 Pa a 116 °C, y 10.000 Pa (casi 0,1 atm) a 162 °C.

Impacto del ferroceno
El ferroceno no fue el primer compuesto organometálico conocido. La sal de Zeise K[PtCl3(C2H4)]-H2O fue reportada en 1831, el descubrimiento de Ni(CO)4 por parte de Mond ocurrió en 1888, y los compuestos organolitio fueron desarrollados en los años 30.
Sin embargo, se puede argumentar que fue el descubrimiento del ferroceno lo que inició la química organometálica como un área separada de la química. También condujo a una explosión de interés en los compuestos de metales de bloque d con hidrocarburos.
El descubrimiento se consideró tan significativo que Wilkinson y Fischer compartieron el Premio Nobel de Química de 1973 «por su trabajo pionero, realizado de forma independiente, en la química de los compuestos organometálicos, los llamados compuestos sándwich».
Para más información Ferrocene | chemical compound | Britannica