Tiempo de lectura estimado: 5 minutos
El carbono es uno de los elementos más abundantes en la corteza terrestre y en el universo. Es un elemento con características únicas gracias a sus propiedades químicas y físicas.
Carbono inorgánico
La mayoría de los compuestos de este elemento corresponden a compuestos orgánicos, pero los compuestos inorgánicos de carbón son de interés debido a su papel en procesos biológicos y geoquímicos en la biosfera.
El carbono es el elemento de numero atómico 6 y masa atómica 12.01, de carácter no metálico y tetravalente. Como parte del grupo IV-A, posee 4 electrones de valencia que puede emplear para establecer 4 enlaces con otros elementos.
Óxidos del carbono
El compuesto inorgánico mas importante del carbono es el dióxido de carbono, componente minoritario de la atmósfera terrestre, exhalado por animales y utilizado por las plantas en el proceso de fotosíntesis. Este compuesto al ser disuelto en agua genera ácido carbónico, que es inestable y fácilmente regresa a su estado de óxido. En estado sólido, puede asociarse a metales para formar los respectivos carbonatos, que son la principal fuente de carbono inorgánico en el planeta.
Otros óxidos de interés son el monóxido de carbono, producto de la combustión incompleta de materia orgánica, y el sub oxido de carbono (dióxido de tricarbono), un compuesto raro obtenido por el calentamiento de una mezcla seca de pentóxido de fósforo y ácido malónico.
Con metales este elemento forma carburos y acetiluros, compuestos con carácter ácido. También puede enlazarse con silicio, generando carburo de silicio, un compuesto con propiedades mecánicas similares a las del diamante.
Materiales
- 2 tubos de ensayo
- Gradilla
- Mechero bunsen
- Columna de cromatografía con llave
- Pinza para balón
- Soporte universal
- 2 vasos de precipitados de 100 mL
- Erlenmeyer con desprendimiento lateral
- 4 probetas de 100 mL
- Corcho o tapón de caucho
- Manguera de caucho
- Tina neumática o bandeja profunda
- 2 vidrios de reloj
- Lana de vidrio o algodón desengrasado
Reactivos
- Carbón vegetal
- Carbón activado
- Ácido sulfúrico concentrado
- Solución de hidróxido de sodio 6 N
- Acido clorhídrico 6 N
- Magnesio en tiras
- Carbonato de calcio
Procedimiento
Tiempo necesario: 40 minutos
Química inorgánica del carbono
Tomar dos tubos de ensayo y colocar en cada uno un trozo pequeño de carbón vegetal. En uno de ellos añadir 1 mL de ácido sulfúrico concentrado, anotar las observaciones. En el otro tubo de ensayo, añadir 1 mL de hidróxido de sodio y anotar las observaciones.
Preparar la columna de cromatografía con 1 cm de lana de vidrio o algodón desengrasado*, 1 cm de carbón activado y 1 cm de lana de vidrio o algodón desengrasado. Filtrar lentamente una solución de un colorante orgánico. Anotar las observaciones.
* La columna de cromatografía puede ser reemplazada por una jeringa sin embolo
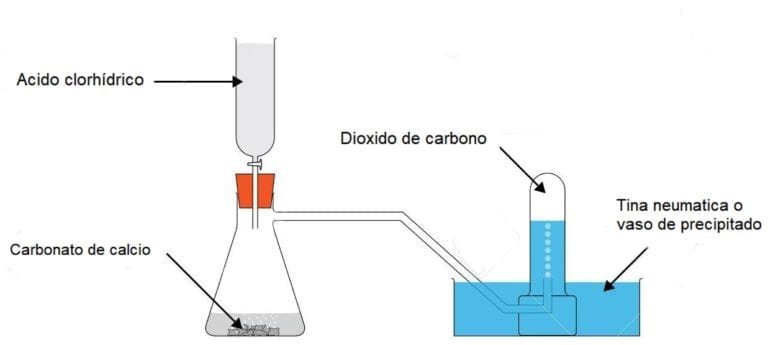
Realizar el montaje sugerido de generación de dióxido de carbono como se muestra a continuación. También se puede emplear un aparato de Kipp o un montaje similar. La bureta puede ser reemplazada por un tubo de adición o una jeringa con aguja para adicionar el ácido de manera controlada. Recoger dos probetas con el gas y taparlas con vidrios de reloj.
 Anuncio
AnuncioTomar una de las probetas vacías y colocar una vela encendida de tal manera que quede en su interior. Verter el dióxido de carbono de una de las probetas en la bureta con la vela y observa. Anotar las observaciones.
Encender una tira de magnesio de 10 cm y arrojarla en la otra probeta con el gas sintetizado. Observar y anotar.
*el algodón puede desengrasarse lavándolo de manera sucesiva con éter de petróleo.
Después del experimento
Anotar las observaciones, escribir las posibles reacciones que se observaron en cada experimento y analizar los cambios sufridos por el carbono.
Investigar que es el carbón activado y la propiedad que le permite adsorber otros compuestos y purificar. ¿Cómo se produce el carbón activado? Investigar las diferencias entre carbón vegetal y carbón mineral, así como sus propiedades y usos.
Recomendaciones de seguridad
En todo momento se deben utilizar los elementos de seguridad básicos en el laboratorio de química (bata de laboratorio, guantes, gafas de seguridad y demás que sean exigidos por las normas internas, locales o nacionales. Los residuos generados por la práctica deben ser dispuestos de manera adecuada según las normas de laboratorio y las normas locales y nacionales respectivas.
Para más información Inorganic Carbon
Como citar este artículo:
APA: (2019-05-01). Química inorgánica del carbono. Recuperado de https://quimicafacil.net/manual-de-laboratorio/quimica-inorganica-del-carbono/
ACS: . Química inorgánica del carbono. https://quimicafacil.net/manual-de-laboratorio/quimica-inorganica-del-carbono/. Fecha de consulta 2026-02-17.
IEEE: , "Química inorgánica del carbono," https://quimicafacil.net/manual-de-laboratorio/quimica-inorganica-del-carbono/, fecha de consulta 2026-02-17.
Vancouver: . Química inorgánica del carbono. [Internet]. 2019-05-01 [citado 2026-02-17]. Disponible en: https://quimicafacil.net/manual-de-laboratorio/quimica-inorganica-del-carbono/.
MLA: . "Química inorgánica del carbono." https://quimicafacil.net/manual-de-laboratorio/quimica-inorganica-del-carbono/. 2019-05-01. Web.
Si tiene alguna pregunta o sugerencia, escribe a administracion@quimicafacil.net, o visita Como citar quimicafacil.net