Electrolisis del ácido sulfúrico
Tiempo de lectura estimado: 5 minutos
El descubrimiento del fenómeno de la electrolisis sucedió de manera accidental en 1800 cuando el químico ingles William Nicholson cuando trabajaba con baterías químicas. Pero fue el químico y científico Michael Faraday quien introdujo el termino electrolisis y desarrollo las primeras descripciones sobre los fenómenos que involucra la aplicación de una corriente eléctrica en una solución o compuesto.
La electrolisis se constituyó rápidamente en una herramienta fundamental para el estudio y aislamiento de nuevos compuestos que, hasta ese momento, habían sido esquivos para los químicos de la época. El químico ingles Sir Humpry Davy aisló sucesivamente los elementos potasio, sodio, bario, calcio y magnesio a partir de sus sales fundidas, igualmente William Thomas Brande aisló el litio en 1821 y el galio fue descubierto por Paul Émile Lecoq de Boisbaudran, todo gracias al desarrollo de la electroquímica.
Electrolisis de ácido sulfúrico
Una reacción redox es capaz de generar energía (corriente eléctrica) cuando se liberan electrones, pero, siguiendo los principios del equilibrio químico, si se aplica un estímulo externo al sistema, es posible revertir el curso natural de la reacción.
Por ejemplo, si se disponen dos semiceldas estándar de Cu2+/Cu y Zn2+/Zn, estas generaran una diferencia de potencial de 1.1V, que puede ser medida con un amperímetro. Si a este mismo conjunto se le aplica una corriente externa ligeramente superior a los 1.1V, se invierte la reacción observada.
Desde el punto de vista termodinámico, no vulnera las leyes fundamentales de la termodinámica, dado que la reacción se invierte debido a la aplicación externa de energía eléctrica. En este caso, se convierte energía eléctrica, suministrada por un generador de corriente, en energía química, dado que se generan productos cuya energía química es superior a la de los reactivos.
Las leyes de Faraday son dos principios rigen los fenómenos de electrólisis, y se emplean para describir los procesos de conversión de energía eléctrica en energía química. A saber:
- La masa de una sustancia liberada es directamente proporcional a la cantidad de electricidad (o bien, a la intensidad de corriente, I, y al tiempo que circula, t)
- Las masas de diferentes sustancias, liberadas por la misma cantidad de electricidad, son directamente proporcionales a los pesos equivalentes de las mismas.
Materiales
- 2 vasos de precipitado de 100 mL
- 2 vasos de precipitado de 1000 mL
- 1 bureta de 50 mL
- Soporte universal
- Pinza para bureta
- trozo de hilo de cobre de 25 cm
- Frasco lavador
- Erlenmeyer de 500 mL
- Cable eléctrico de cobre
- Trozo de cobre de 12 gramos aproximadamente
- Fuente de corriente directa de 12 V a 4 A con sus respectivos cables y pinzas
- Balanza analítica
Reactivos
- 500 mL de solución 0.1 M de ácido sulfúrico
Procedimiento
Tiempo necesario: 50 minutos.
Electrolisis de ácido sulfúrico
-
Verter la solución de ácido sulfúrico 0.1 M en el vaso de 1000 mL e invertir una bureta dentro de la solución, introducir un trozo de cable de cobre con unos 8 cm de metal expuesto por la boca de la bureta invertida, el cable debe quedar totalmente cubierto por la solución
-
Tomar el trozo de cobre de 12 g aproximadamente y medir su masa con una exactitud de 3 cifras decimales al menos y sumergirlo en la disolución de ácido sulfúrico.
-
El trozo de cable será el cátodo del montaje mientras que el trozo de cobre será el ánodo. Conectar el borne positivo al ánodo y el borne negativo al cátodo con la fuente de corriente apagada. Las pinzas que trasmiten la corriente no deben tocar la solución, por lo tanto, una parte de la pieza de cobre debe sobresalir de la solución al igual que el otro extremo del alambre de cobre.
-
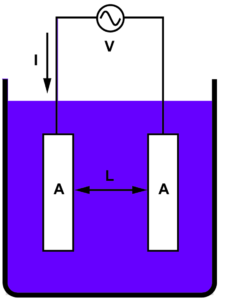
Cuidadosamente retirar el aire contenido en la bureta a través de su punta con la llave abierta para elevar la solución de ácido sulfúrico a través de esta. Para realizar este procedimiento, se aconseja emplear una línea de vacío conectada a una trampa para líquidos. El montaje experimental debe quedar como se muestra en la figura que se muestra abajo
-
Encender la fuente de poder y anotar la hora de inicio. Se observará el desprendimiento de burbujas en el cátodo, gas que será recogido en el interior de la bureta. Igualmente, la solución tomara un color azul celeste.
-
Pasados entre 5 y 10 minutos, la bureta estará lleno de gas. Apagar la fuente de corriente y anotar el volumen exacto de gas producido, al igual que la presión atmosférica y la temperatura del sitio del ensayo.
-
Corregir el volumen de gas teniendo en cuenta la presión de vapor de agua y la presión ambiental. Desconectar el trozo de cobre de la corriente, enjuagarlo con acetona y dejarlo secar por unos minutos. Pesar el trozo de cobre y anotar su masa.
Después del experimento
Determinar la masa perdida por parte del ánodo según la medición de la masa del trozo de cobre antes y después del experimento de electrolisis. Formular las semirreacciones que han tenido lugar en el experimento al igual que la reacción global. Con la ayuda de las leyes de Faraday, determinar la intensidad media de la corriente en el experimento.
Recomendaciones de seguridad
Tener cuidado en el manejo de la solución de acido sulfúrico 0.1 M y la realización del montaje. Evitar aspirar los vapores provenientes de la solución de ácido.
Se debe leer el manual de operación del amperímetro o multímetro a emplear, o recibir instrucción sobre su correcto manejo por parte de personal experto.
En todo momento se deben utilizar los elementos de seguridad básicos en el laboratorio de química (bata de laboratorio, guantes, gafas de seguridad y demás que sean exigidos por las normas internas, locales o nacionales. Los residuos generados por la práctica deben ser dispuestos de manera adecuada según las normas de laboratorio y las normas locales y nacionales respectivas.
Mayor información
Electrolysis of dilute sulfuric acid
Clasificación
Nivel: Universitario
Tipo: Practica de enseñanza
Riesgo: medio