Tiempo de lectura estimado: 7 minutos
La estequiometría es el cálculo de los reactivos y productos en las reacciones químicas y se puede aplicar tanto en soluciones como en gases. Se fundamenta en la ley de conservación de las masas que establece que la masa total de los reactivos es igual a la masa total de los productos, relacionadas a través de números enteros positivos, llamados coeficientes estequiométricos.
Igualmente, la estequiometría permite calcular la masa de los productos si se conoce la masa total de los reactivos. Si se conocen las masas de los productos es posible calcular la masa inicial de los reactivos y así sucesivamente.
La cuantificación de las especies químicas que intervienen en una reacción se puede realizar de distintas maneras, desde pesar la masa de ellos, hasta avanzadas técnicas analíticas como espectrometría.
La estequiometría y las soluciones
El termino estequiometria fue empleado por primera vez por el químico alemán Jeremias Benjamin Richter en 1792 en el primer volumen de Richter’s Stoichiometry or the Art of Measuring the Chemical Elements. El termino se deriva que las palabras griegas stoicheion que significa elemento y metron, que significa medida.
Una cantidad estequiométrica, o relación estequiométrica de un reactivo es la cantidad optima que, asumiendo que la reacción es completa, hace que todo el reactivo sea consumido, que no haya deficiencia de reactivo y no exista exceso de este.
El manejo de gases tanto en investigación como en la industria es de importancia fundamental. Las reacciones que involucran gases tanto en sus reactivos como en sus productos plantean un desafío adicional en el momento de realizar cálculos sobre la cantidad de producto obtenido o de reactivo necesario para llevar a cabo una reacción completa.
Una primera aproximación que se puede realizar para la estimación de la cantidad de masa de un gas es emplear la ley de los gases ideales, que, dependiendo de las condiciones, nos brindará la cantidad en moles de un gas presente bajo las condiciones dadas.
Cuando factores como la presión, la temperatura, el volumen o la masa con la que se está trabajando generan fuertes desviaciones del modelo ideal, es necesario realizar ajustes al modelo de gas ideal introduciendo elementos como el factor acéntrico.
Cuando la desviación es mayor, existen modelos de gases reales que permiten estimar las propiedades de los gases en condiciones como las que se pueden encontrar en una planta de procesamiento químico.
Materiales
- Probeta de 250mL
- Tubo con desprendimiento lateral y manguera
- Tapón de caucho
- Pipeta 5mL
- Vaso de precipitados de 100mL
- Vaso de precipitados de 1L
- Espátula
- Jeringa de 50 mL con aguja hipodérmica
Reactivos
- Carbonato de calcio (CaCO3)
- Acido Clorhídrico 1 M
Procedimiento – Estequiometría que implica gases y soluciones
Tiempo necesario: 50 minutos.
Estequiometría de reacción en soluciones y gases
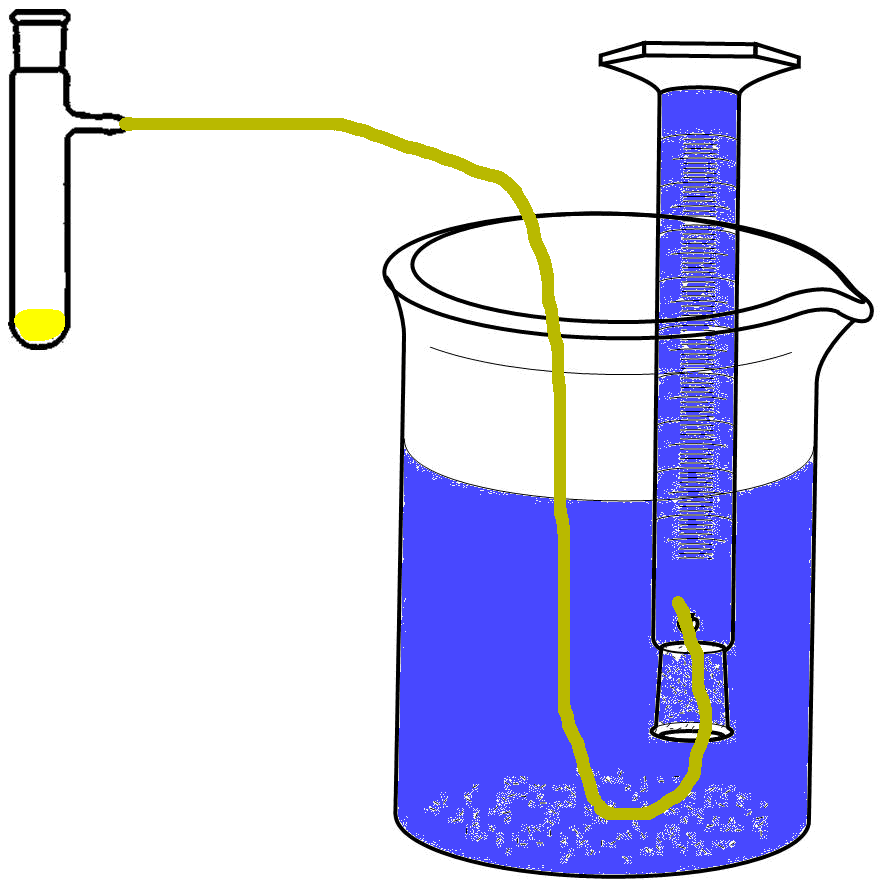
Realizar el montaje que se muestra en la figura. Para llenar la probeta de 250 mL invertida; llenarla a ras y tapando la boca de la probeta, voltearla cuidadosamente en el vaso de precipitados de 1 L previamente lleno con 500 mL de agua. Si queda aire en la probeta invertida se debe anotar dicho valor para restarlo del volumen de gas generado.

Conectar la manguera al desprendimiento lateral del tubo de ensayo y el otro extremo introducirlo en la boca de la probeta ya sumergida en el líquido. Posteriormente pesar 0.1 g de carbonato de calcio y depositarlo en el tubo de ensayo. Tapar herméticamente con el tapón de caucho.
En el vaso de precipitados de 100 mL, servir una cantidad de ácido clorhídrico 1 M. Marcar el vaso.
Con ayuda de la jeringa con aguja, tomar 20 mL de ácido cuidadosamente y verter el ácido dentro del tubo de ensayo con desprendimiento a través del tapón de goma de manera lenta y constante*.
AnuncioCuando el ácido entre en contacto con el carbonato, se observará la generación de un gas que, a través del tubo de goma, será recolectado en la probeta invertida.
Adicionar ácido hasta que no se observe más reacción. Cuando la generación de gas cese, medir el volumen obtenido en la probeta invertida y anotar dicho valor. También se debe registrar la temperatura ambiente y la presión atmosférica del sitio donde se realiza el experimento.
Repetir el experimento con 0.2 g de carbonato de calcio, para esto se debe limpiar el tubo de ensayo con desprendimiento lateral y llenar nuevamente la probeta para realizar una nueva lectura. Repetir 3 veces mas aumentando en cada ensayo 0.1 g de carbonato de calcio.
*este procedimiento debe ser realizado por el instructor a cargo de la practica en caso de que los estudiantes no tengan la suficiente habilidad o edad. La velocidad de adición de ácido debe ser lenta para evitar un aumento de presión excesivo en el tubo de ensayo y un aumento brusco en la temperatura del tubo de ensayo. Se puede agitar suavemente para mejorar el contacto entre el carbonato y el ácido.
Anuncio
Procedimiento alterno
Un procedimiento alterno al anterior descrito consiste en pesar el carbonato de calcio en un pequeño trozo de papel de filtro y hacer una pequeña bolsa con el papel y el carbonato en su interior, colocar 20 mL de ácido clorhídrico en el tubo de ensayo con desprendimiento lateral ligeramente inclinado. Colocar el papel de filtro en la boca del tubo y tapar empleando el tapón de caucho.
Cuando el conjunto este sellado, poner verticalmente para que la bolsa de papel con el carbonato caiga sobre el ácido, iniciando la reacción. Este procedimiento tiene el inconveniente que, si la cantidad de carbonato de calcio es mayor a la estequiométrica, se convertirá en el reactivo limite, limitando la generación de gas. Se pueden realizar previamente los cálculos estequiométricos sobre la cantidad de ácido necesaria para reaccionar con la totalidad del carbonato de calcio.
Después del experimento
Escribir la reacción entre el carbonato de calcio y el ácido clorhídrico, balancear la ecuación. Tomando como reactivo limite el carbonato de calcio, realizar los cálculos estequiométricos sobre la cantidad teórica de gas generado.
Estimar la cantidad de masa de gas recolectado en la probeta empleando la ecuación de los gases ideales
Teniendo en cuenta la temperatura ambiente del laboratorio al momento de realizar la práctica, la presión atmosférica el lugar y el volumen de gas recolectado
Completar la siguiente tabla con los datos obtenidos en la práctica y resultantes de los cálculos estequiométricos realizados.

¿Qué factores se pueden tener en cuenta para explicar la diferencia entre el valor teórico y el valor real del gas recolectado en el experimento?
Recomendaciones de seguridad
Es necesario tener precaución en el momento de la inyección del ácido en el tubo de ensayo con desprendimiento lateral, evitar pincharse con la aguja. Se debe tener cuidado que la manguera que transporta el gas hacia la probeta no se encuentre obstruido, lo que podría generar una sobre presión en el sistema.
En todo momento se deben utilizar los elementos de seguridad básicos en el laboratorio de química (bata de laboratorio, guantes, gafas de seguridad y demás que sean exigidos por las normas internas, locales o nacionales. Los residuos generados por la práctica deben ser dispuestos de manera adecuada según las normas de laboratorio y las normas locales y nacionales respectivas.
Para más información Calcium carbonate and hydrochloric acid and their interaction
Clasificación
Nivel: Universitario
Tipo: Practica de enseñanza
Riesgo: medio