Estimated reading time: 8 minutos
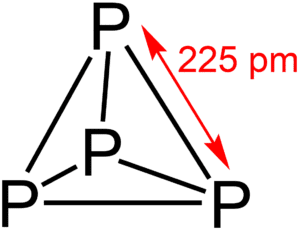
El fósforo blanco, también conocido como fósforo amarillo por sus impurezas, es el alótropo más común, volátil y reactivo del elemento químico fósforo. Su fórmula molecular es , y su estructura consiste en cuatro átomos de fósforo dispuestos en los vértices de un tetraedro regular.
Este compuesto es tristemente célebre por su extrema reactividad, siendo pirofórico (se inflama espontáneamente al contacto con el aire) y altamente tóxico.
Descubierto en el siglo XVII por un alquimista en una búsqueda de la piedra filosofal, el fósforo blanco ha tenido una historia dual fascinante. Por un lado, ha sido un pilar en la industria química para la producción de ácido fosfórico de alta pureza, un compuesto esencial en alimentos, bebidas y fertilizantes.
Por otro, su naturaleza peligrosa lo llevó a ser el causante de una terrible enfermedad laboral conocida como «fosforonecrosis» en la industria de las cerillas y a ser utilizado como un controvertido agente incendiario y de ocultación en la guerra moderna. Su misterioso brillo en la oscuridad, un fenómeno de quimioluminiscencia, le dio su nombre, derivado del griego phosphoros, que significa «portador de luz».
Historia
El Descubrimiento Alquímico de Hennig Brand
El fósforo blanco fue descubierto en 1669 en Hamburgo por el alquimista alemán Hennig Brand. Como muchos alquimistas de su tiempo, Brand estaba obsesionado con la búsqueda de la piedra filosofal, una sustancia mítica capaz de transmutar metales base en oro. En su razonamiento, pensó que la orina humana, por su color dorado y su origen en el cuerpo, podría contener la «esencia vital» o el «espíritu» necesario para este proceso.
Su procedimiento era tan laborioso como maloliente. Dejó reposar grandes cantidades de orina durante semanas hasta que se pudriera, para luego calentarla en una retorta a altas temperaturas. Al final del proceso, los fosfatos presentes en la orina (como el fosfato de sodio y amonio) fueron reducidos por el carbono (procedente de la materia orgánica), produciendo un vapor que, al condensarse en agua, formaba una sustancia cerosa y pálida que brillaba en la oscuridad.
Había aislado el fósforo elemental. Se dice que su segunda esposa, una mujer adinerada, financió sus experimentos, mostrando una admirable devoción conyugal a pesar de los olores nauseabundos que emanaban de su laboratorio. Este dramático momento fue inmortalizado en la famosa pintura de Joseph Wright de Derby, El Alquimista descubriendo el Fósforo.
La Era de las Cerillas y la «Fosforonecrosis»
En el siglo XIX, la alta inflamabilidad del fósforo blanco lo convirtió en el ingrediente clave para la fabricación de las primeras cerillas de fricción, conocidas como «Lucifers». Estas cerillas contenían una mezcla de fósforo blanco, un agente oxidante como el clorato de potasio, y un aglutinante. Eran efectivas, pero peligrosamente inestables, a menudo encendiéndose por sí solas en los bolsillos de sus dueños.
El mayor problema, sin embargo, era el impacto en la salud de los trabajadores de las fábricas de cerillas, en su mayoría mujeres y niñas. La exposición prolongada a los vapores de fósforo blanco causaba una devastadora enfermedad laboral conocida como osteonecrosis del maxilar o, más comúnmente, «fosforonecrosis» (phossy jaw). La enfermedad comenzaba con dolores de muelas y abscesos, progresando hacia la destrucción del hueso de la mandíbula, causando desfiguración severa y, en muchos casos, la muerte.
La situación culminó en la histórica huelga de las cerilleras de Londres de 1888, un evento fundamental en la historia del movimiento obrero y la salud industrial. La protesta contra las condiciones de trabajo inhumanas llevó a una mayor conciencia pública y, finalmente, a la prohibición del uso de fósforo blanco en las cerillas a través de la Convención de Berna de 1906. Las cerillas modernas de seguridad utilizan fósforo rojo, un alótropo mucho más seguro, en la superficie de fricción de la caja, no en la cabeza de la cerilla.
Estructura, Alotropía y Propiedades
El fósforo, como otros elementos del grupo 15, existe en varias formas alotrópicas, siendo el fósforo blanco la más reactiva.
Estructura Molecular del P₄ y Tensión de Anillo
La molécula de fósforo blanco, , tiene una estructura tetraédrica. Los cuatro átomos de fósforo están unidos entre sí por enlaces covalentes simples. La geometría de un tetraedro regular impone que los ángulos de enlace P-P-P sean de 60°. Este ángulo es extremadamente agudo y se desvía drásticamente del ángulo de enlace ideal de ~109.5° para orbitales híbridos sp³.
Esta desviación crea una inmensa tensión de anillo en la molécula. Los enlaces P-P son, por tanto, débiles y la molécula es energéticamente muy inestable. Esta energía almacenada se libera de forma explosiva durante las reacciones químicas, lo que explica su alta reactividad y naturaleza pirofórica.
Otros Alótropos
- Fósforo Rojo: Es la forma que se obtiene al calentar el fósforo blanco en ausencia de aire. Es una estructura polimérica amorfa, mucho más estable, menos reactiva y no tóxica. Es el que se utiliza en las superficies de rascado de las cajas de cerillas.
- Fósforo Negro: Es el alótropo termodinámicamente más estable y menos reactivo. Posee una estructura en capas similar al grafito y ha ganado interés en la ciencia de materiales para aplicaciones en electrónica (fosforeno).
- Fósforo Violeta y Azul: Son otras formas cristalinas menos comunes.
Propiedades Físicas y Químicas
- Apariencia: Es un sólido ceroso y blando. Cuando es puro es blanco, pero a menudo tiene un tinte amarillento debido a la lenta conversión a fósforo rojo por exposición a la luz.
- Solubilidad: Es insoluble en agua, lo que permite su almacenamiento seguro por inmersión. Sin embargo, es soluble en disolventes no polares como el disulfuro de carbono (
).
- Quimioluminiscencia: El característico brillo verdoso del fósforo blanco en la oscuridad no es fosforescencia, sino quimioluminiscencia. Es el resultado de una reacción de oxidación lenta en la superficie con el oxígeno del aire. Esta reacción produce intermedios electrónicamente excitados ((PO)₂ y HPO) que emiten luz al relajarse a su estado fundamental.
- Piroforicidad: Se inflama espontáneamente en el aire a unos 30 °C, ardiendo con una llama brillante y produciendo un humo denso de pentóxido de fósforo (
).
Producción Industrial y Usos
A pesar de ser una sustancia peligrosa, el fósforo blanco es un producto químico industrial fundamental.
Proceso de Producción
Se produce a gran escala mediante el proceso electrotérmico. En este método, la roca fosfórica (principalmente fosfato de calcio, ) se calienta a temperaturas de 1200-1500 °C en un horno de arco eléctrico junto con coque (carbono) y sílice (arena,
).
- El carbono actúa como agente reductor.
- La sílice actúa como un fundente, reaccionando con el calcio para formar una escoria líquida de silicato de calcio (
), que se elimina fácilmente.
El fosfato se reduce a fósforo elemental, que se volatiliza a esas temperaturas. Los vapores de se recogen y se condensan bajo agua para obtener el fósforo blanco.
Principal Aplicación: Producción de Ácido Fosfórico
La gran mayoría del fósforo blanco producido se utiliza para fabricar ácido fosfórico () de alta pureza a través del «proceso térmico». Este proceso implica dos etapas:
- Combustión: El fósforo blanco se quema en un exceso de aire para producir pentóxido de fósforo (
).
- Hidratación: El pentóxido de fósforo, un sólido blanco muy higroscópico, se hidrata con agua para formar ácido fosfórico puro.
Este ácido fosfórico de grado alimentario es el que se utiliza como acidulante en bebidas gaseosas como la Coca-Cola y la Pepsi, dándoles su característico sabor ácido y picante. También se utiliza en la fabricación de otros productos químicos de fósforo, detergentes y productos farmacéuticos.
Uso Militar
El fósforo blanco tiene dos aplicaciones principales en el ámbito militar, ambas derivadas de su violenta reacción con el aire.
- Agente Incendiario: Las municiones de fósforo blanco dispersan partículas de P₄ que se inflaman al contacto con el aire. Estas partículas ardientes (a más de 800 °C) se adhieren a las superficies, incluida la piel, y son extremadamente difíciles de extinguir, ya que se reavivan si vuelven a exponerse al oxígeno. Causan quemaduras térmicas y químicas muy graves y profundas. Su uso como arma incendiaria contra objetivos civiles o en zonas pobladas está prohibido por el Protocolo III de la Convención sobre Ciertas Armas Convencionales de la ONU.
- Pantalla de Humo: La combustión del fósforo blanco produce una nube instantánea, densa y extensa de partículas de pentóxido de fósforo. Estas partículas absorben rápidamente la humedad del aire para formar un aerosol de gotitas de ácido fosfórico, que es muy eficaz para ocultar movimientos de tropas y vehículos tanto en el espectro visible como en el infrarrojo. El uso de fósforo blanco para crear pantallas de humo se considera legítimo según el derecho internacional, lo que crea un «vacío legal» controvertido que dificulta la persecución de su uso ilegal como arma incendiaria.