Destilación simple – Azeótropos
Tiempo de lectura estimado: 5 minutos
Un azeótropo (o mezcla azeotrópica) es una mezcla de composición especifica entre dos o más compuestos químicos que hierve a temperatura constante, comportándose como si fuese un solo componente
Los compuestos puros se destilan a una temperatura constante, mientras que la mayoría de las soluciones que contienen más de un componente volátil se destilan en un rango de temperaturas.
Hay una excepción a esta afirmación, ya que algunas mezclas de cierta composición también se destilan a una temperatura constante. Estas mezclas se denominan «azeótropos», que presentan un comportamiento no ideal y no siguen la ley de Raoult.
¿Qué es un azeótropo?
Uno de los azeótropos más conocidos es una mezcla que contiene el 95,6% de etanol y un 4,4% de agua. Cuando se destila una mezcla que contiene etanol y agua (por ejemplo, cuando se concentran granos fermentados para producir licor), el 95,6% es el porcentaje más alto posible de etanol en el destilado.
Es imposible destilar etanol 100% puro cuando hay agua en el recipiente de destilación, ya que el etanol y el agua actúan conjuntamente como una sustancia pura. Por esta razón, la mayor parte del etanol utilizado es la versión del 95%, ya que se puede purificar por destilación y es el menos costoso.
También se puede comprar «etanol absoluto» (pureza <99% en etanol), pero es más caro, ya que se requieren otros métodos (por ejemplo, agentes secantes) para eliminar el agua residual antes o después de la destilación.
Los azeótropos se forman cuando una solución se desvía de la ley de Raoult, lo que significa que la presión de vapor producida por una solución azeotrópica no se correlaciona directamente con su fracción molar.
Las desviaciones se producen cuando los componentes se atraen o se repelen entre sí, es decir, si tienen fuerzas significativamente diferentes de las fuerzas intermoleculares (IMF) hacia sí mismas (p. ej. A-A o B-B) como lo hacen con los otros componentes (p. ej. A-B). En otras palabras, una solución se desviará de la ley de Raoult si la entalpía de la mezcla no es cero.
Mezclas azeotropicas
Las mezclas azeotrópicas se presentan en dos formas: una cuyo punto de ebullición es inferior a cualquiera de sus constituyentes (denominada «azeótropo de punto mínimo de ebullición») o aquellas cuyo punto de ebullición es superior a cualquiera de sus constituyentes (denominada » azeótropo de punto máximo de ebullición «).
Por ejemplo, la mezcla de 61% de benceno/39% de metanol es un azeótropo con un punto de ebullición mínimo, ya que su punto de ebullición es de 58°C, que es inferior al punto de ebullición del benceno (80°C) y el metanol (65°C). Los azeótropos de punto mínimo de ebullición son mucho más comunes que los de máximo punto de ebullición.
Los azeótropos de punto de ebullición mínima ocurren cuando las fuerzas intermoleculares del componente son más fuertes entre sí (A-A/B-B) que entre los componentes (A-B). Esto ocurre generalmente con componentes que carecen de afinidad entre sí, por ejemplo, cuando un componente puede interactuar con el hidrógeno, pero el otro no.
En estas situaciones, los componentes interactúan un poco en solución, lo que disminuye la entropía de la solución y la hace más favorable para convertirse en gas. Por lo tanto, estas soluciones tienen una presión de vapor más alta que la prevista por la ley de Raoult, lo que lleva a una temperatura de ebullición más baja.
Los azeótropos de punto máximo de ebullición tienen el efecto contrario, como resultado de las atracciones en la solución que conducen a presiones de vapor más bajas de lo previsto y, por lo tanto, a temperaturas de ebullición más altas.
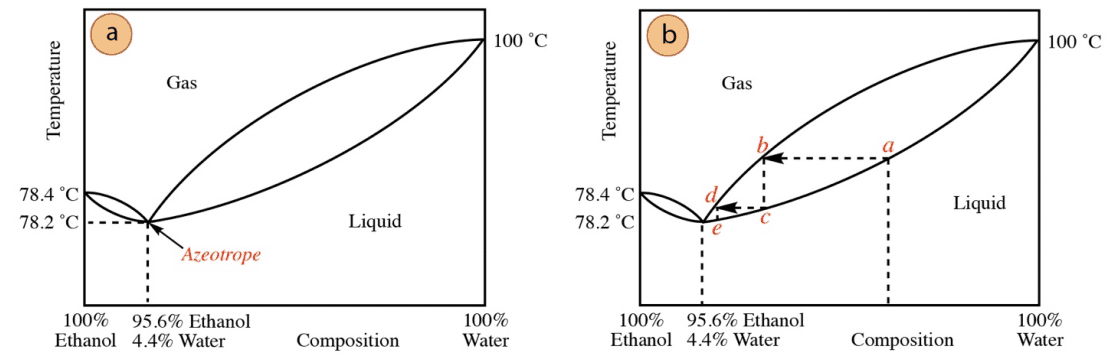
En la siguiente figura se muestra una curva de destilación para una mezcla de etanol y agua (no dibujada a escala para mostrar los detalles). El azeótropo de punto mínimo de ebullición está representado por la intersección de las dos formas de lágrimas, como se indica en la figura, esta curva demuestra por qué no se puede destilar una mezcla de etanol y agua para producir un destilado con una concentración superior al 95,6%. etanol.
Imagine destilar una mezcla de etanol y agua de la composición en la posición a de la figura. Después de cada proceso de vaporización-condensación (de a a b a c, luego de c a d a e en la figura), la concentración de etanol aumenta.
Sin embargo, el material siempre es canalizado hacia el punto más bajo de la curva, la composición azeotrópica. Las concentraciones superiores al 95,6% de etanol sólo se pueden destilar cuando ya no hay agua en el sistema (momento en el que el diagrama de fases de la figura ya no es aplicable).
Dado que el agua forma azeótropos de punto minino de ebullición con muchos compuestos orgánicos, queda claro por qué el agua debe eliminarse siempre cuidadosamente con agentes secantes antes de la destilación: si no se eliminan los rastros de agua, se producirá un destilado con contenido de humedad.
Para más información Simple Distillation