Tiempo de lectura estimado: 13 minutos
La cromatografía en microcolumna es una técnica análoga a la cromatografía en columna empleada para la purificación de extractos pequeños, aunque sigue los mismos principios de la cromatografía
Una columna tradicional es demasiado grande para cantidades muy pequeñas de material (<20mg). En cambio, se puede construir una columna con una pipeta Pasteur desechable, esto se llama cromatografía en microcolumna
Para conseguir una buena separación, es ideal si el componente deseado tiene un Rf alrededor de 0,35 y está separado de otros componentes por al menos 0,2 unidades Rf. Si los puntos a separar están muy cerca (< 0,2 ΔRf), es mejor que el centro de los puntos tenga un Rf de 0,35. Un Rf cercano a 0,35 es ideal porque es lo suficientemente lento como para que se produzca un equilibrio de fase estacionaria-móvil, pero lo suficientemente rápido como para minimizar el ensanchamiento de la banda por difusión.
Procedimiento paso a paso cromatografía en microcolumna
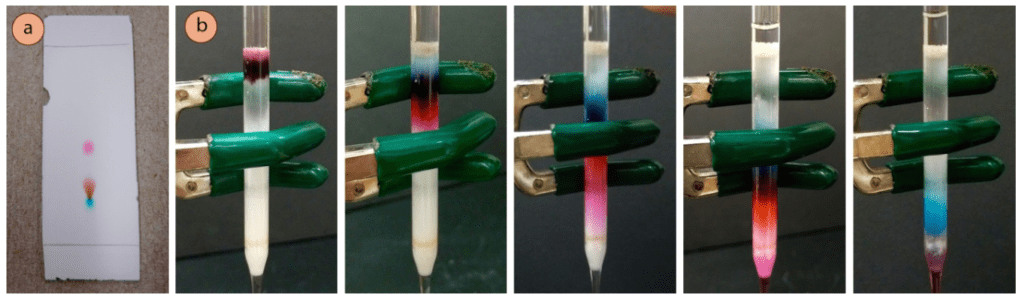
La columna que se muestra en esta sección muestra la purificación de una gota de colorante alimentario púrpura diluido (hecha de 1 gota de colorante rojo, 1 gota de colorante azul y 15 gotas de agua). El tinte se separa lo mejor posible en sus tres componentes: azul, rojo y rosa (como se ve en la placa de TLC de la figura 1a). Se utiliza una columna de gel de sílice de 2,5″ y se eluye con una solución hecha con una relación de volumen de 1:3:1 de NH4OH 6M:1-pentanol:etanol.

- Realice una cromatografía en capa delgada o TLC de la muestra que se va a purificar (Figuras 2 a+b) para determinar el disolvente apropiado para la cromatografía. El componente deseado debe tener un Rf de alrededor de 0,35.
Preparar la columna seca
- Utilice una varilla de metal o un colgador (Figura 2d) para introducir un poco de algodón o lana de vidrio en el extremo estrecho de una pipeta Pasteur de tallo corto. El algodón debe estar moderadamente apretado para que el líquido pueda pasar, pero no el sólido.

- Ponga sílice o alúmina en el extremo ancho de la columna de la pipeta (Figura 3a), luego invierta y levante la columna para que el polvo caiga al fondo. Continúe utilizando este método de extracción para llenar la columna de la pipeta hasta una altura de 2 a 2,5 pulgadas con sílice o alúmina (esta cantidad puede ser alterada dependiendo de la cantidad de muestra).
Alternativamente, extraiga el adsorbente en el extremo ancho de una pipeta nueva y utilícelo como embudo para introducir el adsorbente a través de la punta estrecha y en la columna de la pipeta asegurada a un soporte de anillo con una abrazadera de tres dedos (Figuras 3 a-c).
Nota de seguridad: Como la sílice y la alúmina son polvos finos e irritantes para los pulmones, asegúrese de trabajar en una campana extractora cuando manipule la sílice o la alúmina. También golpee la pipeta después de recogerla para desalojar el adsorbente en el exterior de la pipeta (para que no se derrame cuando esté en posición vertical).
- Sujetar suavemente la columna de la pipeta a un soporte de anillo o enrejado usando una abrazadera de tres dedos (nota: ¡son frágiles!) y golpearla para asegurarse de que el sílice / alúmina se asiente y el borde superior esté horizontal.
- Añada aproximadamente 0.5 cm de arena sobre la capa de sílice y alúmina. Si se utiliza arena muy fina, use otra pipeta para actuar como embudo, como se describe en el paso 3. Para la arena gruesa, utilice una pequeña pala o el extremo ancho de otra pipeta para ayudar en su entrega (Figura 3d). En la Figura 3e se muestra una columna de pipeta completa.
Humedecer la columna
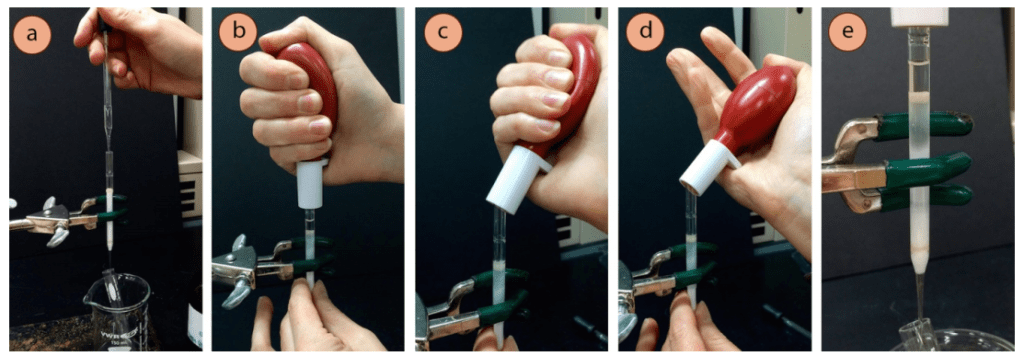
- Coloca un tubo de ensayo apoyado en un pequeño vaso debajo de la columna. Añada un chorro del eluyente apropiado (previamente determinado por la TLC en el Paso 1), suavemente por encima de la capa de arena de la columna de la pipeta (Figura 4a).
- Utilice una bombilla de pipeta (o bombilla de gotero) para aplicar una suave presión de aire y empujar el eluyente a través de la columna (Figura 4b), deteniéndose cuando el nivel de líquido esté en la capa de arena. A lo largo de todo el proceso de elución, mantenga esta sección de la columna blanca mojada con el eluyente.
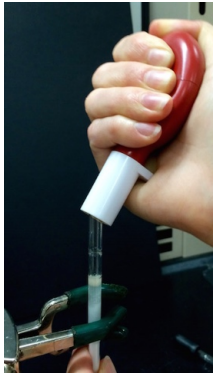
Para aplicar presión de aire con una bombilla de pipeta, cree una fuerte conexión entre la columna y la bombilla, y luego apriete la bombilla. Es importante que cuando se libere la presión, primero se rompa el sello mientras se mantiene la mano apretada (Figura 4c) y DESPUÉS se libere la mano (Figura 4d). Si suelta la mano mientras aún está conectada a la columna, la bombilla creará una succión que puede arrastrar violentamente el líquido dentro de la bombilla y perturbar la columna.
- Añada más eluyente si es necesario, y utilice la presión del bulbo hasta que toda la columna esté saturada de eluyente (Figura 4e), y el nivel de eluyente esté en la capa de arena.

Añada la muestra
- Utilice una pipeta para añadir toda la muestra a la capa de arena. Si la muestra es un líquido, añádala directamente. En caso que sea es un sólido, disuélvalo en la menor cantidad de disolvente posible, preferiblemente el eluyente. Si el sólido no es soluble en el eluyente, use la mínima cantidad de diclorometano. Coloque la punta de la pipeta cerca de la capa de arena y añada la muestra con cuidado, tratando de no salpicar el compuesto en los lados (Figura 5a).
- Enjuague el recipiente original con un poco de disolvente y añada el enjuague a la columna utilizando la misma pipeta (para enjuagar también la pipeta).
- Aplique presión con la bombilla para forzar la muestra justo después de la capa de arena (Figuras 5 b+c).
- Añada más eluyente (aproximadamente 0,5 cm alto) para enjuagar los lados de la columna (Figura 5d). De nuevo, utilice la presión del bulbo para forzar el tinte sobre el adsorbente (Figura 5e), y luego llene la pipeta por encima de la capa de arena lo más alto posible con el eluyente.

Eluye la columna y recoja las fracciones
- Aplique una suave presión de bombilla para empezar a eluir la muestra a través de la columna (Figura 6a), rellenando la pipeta siempre que el nivel de disolvente se acerque a la capa de arena.
- Inmediatamente empiece a recoger el líquido que elude debajo de la columna en un tubo de ensayo vacío. Cambie el tubo de ensayo por uno nuevo periódicamente (Figura 6c), basándose en su juicio o en la orientación de su instructor (tal vez cuando un pequeño tubo de ensayo se llene hasta aproximadamente 1cm alto).
Estos diferentes tubos se llaman «fracciones». El objetivo de una cromatografía en microcolumna es recoger fracciones lo suficientemente pequeñas que la mayoría (o algunas) fracciones contienen material puro.
Si la separación de la mezcla es difícil (si el ΔRf de los componentes es bajo), puede ser mejor recolectar fracciones aún más pequeñas (por ejemplo, 0,5cm alto).
- Mantenga los tubos de ensayo en orden en un estante para tubos de ensayo (Figura 6d).

Encontrar y concentrar el componente deseado
- Para encontrar el componente deseado en las fracciones de tubo de ensayo, es útil comprender la relación entre el Rf y el orden de elución en la cromatografía en columna.
En la cromatografía en microcolumna, la muestra se deposita en la parte superior de la columna y se eluye hacia abajo, mientras que en la cromatografía en capa fina la muestra se deposita en la parte inferior de la placa y se elude hacia arriba. Por lo tanto, una columna puede ser pensada como una placa de TLC al revés.
Un compuesto con un Rf más alto corre «más rápido», lo que significa que terminará más alto en una placa de TLC, y se recogerá primero con una columna.
En la columna de la pipeta que se muestra en esta sección, el componente rosa tenía el Rf más alto en la placa de TLC (Figura 7a), y se recogió primero (Figura 7b). También se recogió una fracción de color púrpura (Figura 7c), debido a la separación incompleta de los componentes rojo y azul.
- Utilice la TLC como se describe en la sección de columnas a macroescala para determinar qué tubos contienen el componente deseado.
- Combine las fracciones puras en un matraz de fondo redondo de tamaño apropiado utilizando un embudo, enjuague cada tubo con una pequeña cantidad de eluyente (u otro disolvente si hay problemas de solubilidad) y añada el enjuague al matraz. Retire el disolvente del evaporador rotativo.
- Para limpiar la columna de la pipeta, utilice la presión de la bombilla para forzar el exceso de líquido fuera de la columna de la pipeta, y deseche la columna semiseca (gel de sílice y todo) en el recipiente de vidrio roto.
Paso a paso – Cromatografía en microcolumna
Resumen cromatografía en microcolumna
Ponga un poco de algodón en el fondo de una pipeta. Use un método de extracción para llenar de sílice o alúmina hasta 2-2.5 pulgadas de altura.

Añade una capa de 0,5 cm de arena
 Anuncio
AnuncioAñade el eluyente a la columna y aplica presión con una bombilla de pipeta para forzar el eluyente a través de la columna para humedecerla completamente.

Recuerde romper el sello antes de soltar la bombilla de la pipeta, o la succión arruinará la columna. Rellene la columna con el eluyente según sea necesario

Ajustar el nivel de eluyente a la capa de arena, y luego agregar delicadamente la muestra. Presione para empujar el eluyente hacia la capa de sílice/alúmina. Enjuague con una porción de eluyente y empuje el disolvente sobre la columna.

Llene la pipeta con el eluyente y aplique presión para eluir la columna. Recoger el líquido en tubos de ensayo. Mantenga siempre húmeda la sección blanca de la columna (rellénela siempre que el nivel de eluyente se acerque a la capa de arena).
 Anuncio
AnuncioCambie los tubos de ensayo periódicamente (quizás cuando tengan 1 cm de altura en pequeños tubos de ensayo) para recoger diferentes fracciones.

Mantén las fracciones organizadas en un estante para tubos de ensayo en el orden en que se eluyen. Usen el TLC para determinar la pureza de las fracciones, y combinen las fracciones apropiadas. Elimine el disolvente con el evaporador rotativo.

Para más información sobre cromatografía en microcolumna 2.3B: Microscale (Pipette) Columns