El misterioso experimento de un siglo
Tiempo de lectura estimado: 5 minutos
Desde hace más de un siglo, un misterioso experimento permanecía sin explicación aparente, una transformación mágica que ahora ha revelado su secreto.
Los científicos pueden finalmente entender la misteriosa transición detrás de un experimento de química de un siglo de antigüedad. Los detalles de esta transformación, en la que la adición de electrones a una solución de amoníaco azul brillante la transforma en un bronce metálico brillante, han eludido por mucho tiempo a los científicos.
El nuevo estudio revela los sutiles detalles de este cambio, y muestra que esta transformación es gradual, más que repentina. «Lo que hemos hecho con éxito es que hemos comprendido bastante bien cómo se comportan estas soluciones en una amplia gama de concentraciones utilizando una técnica de microchorro«, dijo el coautor del estudio Ryan McMullen, un estudiante de doctorado en química de la Universidad de California del Sur. Esta técnica, que consiste en disparar chorros muy finos de la solución a través de un vacío, no se ha utilizado antes en el líquido brillante.
Y el descubrimiento podría abrir nuevos tipos de reacciones en la química orgánica en el futuro, dijo McMullen.
¿Qué es un metal?
Los metales son un grupo diverso. Algunos, como el litio, son lo suficientemente ligeros como para flotar, mientras que otros, como el plomo o el osmio son extremadamente densos. Algunos requieren temperaturas increíblemente altas para fundirse, mientras que otros se funden fácilmente (el mercurio, por ejemplo, se funde a 38,3 grados centígrados bajo cero, o a 37,9 grados Fahrenheit bajo cero). En última instancia, lo que los metales tienen en común es su capacidad de conducir la electricidad en el cero absoluto, el punto en el que el movimiento molecular del calor se detiene.
Pero ¿cómo se transforman en metales algunas sustancias no metálicas? En un nuevo estudio, los investigadores respondieron a esa pregunta añadiendo metales al amoníaco líquido.
Primero, los investigadores condensaron amoníaco, que es un gas a temperatura ambiente, en un líquido enfriándolo a – 27,4 F (- 33 °C). Luego añadieron sodio, litio o potasio, que son todos metales alcalinos. Los experimentos se realizaron en colaboración con científicos de la Academia Checa de Ciencias y el Instituto Fritz-Haber de la Sociedad Max Planck de Berlín, así como con investigadores de Japón y Francia.
El resultado fue una reacción esperada: El amoníaco líquido extrajo electrones del metal. Esos electrones quedaron atrapados entre las moléculas de amoníaco, creando los llamados electrones disueltos que los investigadores esperaban estudiar. En bajas concentraciones, el resultado fue un líquido azul no metálico. Sin embargo, a medida que los electrones disueltos, o atrapados, se apilaban, la solución pasaba a ser de color bronce brillante.
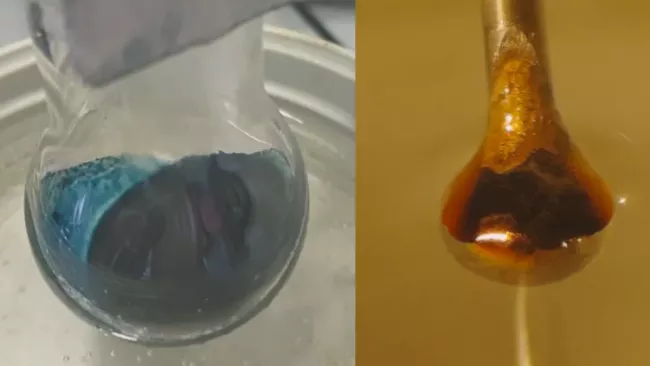
El efecto de la concentración
El siguiente desafío fue investigar cómo se comportaron los electrones disueltos en diferentes concentraciones. Esto implicaba disparar un microchorro de la solución – aproximadamente del ancho de un cabello humano – a través de un haz de rayos X de sincrotrón, que son rayos X de alta energía. Los rayos X excitaban los electrones disueltos, causando que salieran de su jaula líquida de moléculas de amoníaco. Los investigadores pudieron entonces medir cuánta energía se necesitó para liberar los electrones disueltos.
Los investigadores descubrieron que cuanto mayor era la concentración de electrones disueltos, más el patrón de liberación de energía coincidía con lo que se veía en un metal. Esto es lo que significa: Si se grafica la cantidad de energía necesaria para liberar electrones de su jaula de amoníaco líquido, los metales suelen tener lo que se denomina un «borde de Fermi», una transición muy abrupta, dijo McMullen. A concentraciones más bajas de electrones disueltos, este gráfico de liberación de energía se parece más a una colina redondeada. Sólo a mayores concentraciones de electrones surgió este borde de Fermi. El borde refleja cuánta energía tienen los electrones a una temperatura determinada, añadió McMullen.
«Cuando se aumenta la concentración a la gama metálica entonces se ve, este maravilloso patrón emerge que es muy, muy característico de un metal», dijo McMullen.
Los resultados fueron interesantes porque mostraron que el líquido similar al metal creado al combinar metales alcalinos y amoníaco es en realidad un metal a un nivel físico fundamental, dijo.
«Es un metal genuino, no es algo que sólo se parece a uno», dijo McMullen.
Reducción de Birch
Los electrones disueltos de baja concentración se utilizan en un tipo de reacción llamada reacción de Birch (o reducción de Birch), que añade electrones a estructuras moleculares llamadas anillos aromáticos. Este tipo de reacción se utilizó en la fabricación de las primeras píldoras anticonceptivas orales en la década de 1950, dijo McMullen. Al comprender cómo funcionan los electrones disueltos en altas concentraciones, los investigadores pueden encontrar potencialmente nuevos tipos de reacciones químicas, dijo. Por ejemplo, podrían excitar los electrones disueltos con rayos de luz para que se comporten de nuevas maneras.
«Si se hace un poco de cosquillas a los electrones para que se exciten más energéticamente, se puede comenzar a observar algunas reacciones locas que de otra manera nunca ocurrirían«, dijo McMullen.
Los investigadores informaron sobre sus experimentos y hallazgos el 5 de junio en la revista Science
Para más información Experiment shows for the first time in detail how electrolytes become metallic



