Taxol
Estimated reading time: 15 minutos
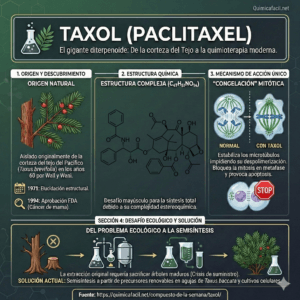
El Paclitaxel (PTX), que se vende bajo el nombre comercial de Taxol entre otros, es un medicamento quimioterapéutico que se utiliza para tratar varios tipos de cáncer, entre ellos el cáncer de ovario, de mama, de pulmón, el sarcoma de Kaposi, el cáncer de cuello de útero y el cáncer de páncreas. Se administra por inyección en una vena. También hay una formulación con albumina.
Los efectos secundarios más comunes incluyen pérdida de cabello, supresión de la médula ósea, entumecimiento, reacciones alérgicas, dolores musculares y diarrea. Otros efectos secundarios serios incluyen problemas cardíacos, aumento del riesgo de infección e inflamación de los pulmones. Existe la preocupación de que el uso durante el embarazo pueda causar defectos de nacimiento. El Paclitaxel pertenece a la familia de los medicamentos taxanos. Funciona interfiriendo en la función normal de los microtúbulos durante la división celular.
El Paclitaxel fue aislado por primera vez en 1971 del tejo del Pacífico (Taxus brevifolia) y aprobado para uso médico en 1993.
Historia
El descubrimiento del paclitaxel comenzó en 1962 como resultado de un programa de detección financiado por el NCI. Varios años después se aisló de la corteza del tejo del Pacífico, Taxus brevifolia, de ahí su nombre «taxol».
El descubrimiento fue hecho por Monroe E. Wall y Mansukh C. Wani en el Research Triangle Institute, Research Triangle Park, Carolina del Norte, en 1971. Estos científicos aislaron el producto natural de la corteza del tejo del Pacífico, determinaron su estructura y lo llamaron «taxol», y organizaron sus primeras pruebas biológicas. El compuesto fue luego desarrollado comercialmente por BMS, a quien se le asignó el nombre genérico de «paclitaxel».
Programa de detección de plantas
En 1955, el NCI de los Estados Unidos estableció el Centro de Servicio Nacional de Quimioterapia para el Cáncer (CCNSC) para que actuara como centro público de detección de la actividad anticancerosa en compuestos presentados por instituciones y empresas externas. Aunque la mayoría de los compuestos examinados eran de origen sintético, un químico, Jonathan Hartwell, que trabajó allí desde 1958 en adelante, tenía experiencia con compuestos derivados de productos naturales y comenzó un programa de detección de compuestos de interés en plantas.
Después de algunos años de arreglos informales, en julio de 1960, el NCI encargó a los botánicos del Departamento de Agricultura de los Estados Unidos (USDA) que recogieran muestras de unas 1.000 especies de plantas al año. El 21 de agosto de 1962, uno de esos botánicos, Arthur S. Barclay, recogió cortezas de un solo tejo del Pacífico en un bosque al norte de la ciudad de Packwood, Washington, como parte de un viaje de cuatro meses para recoger material de más de 200 especies diferentes. El material fue luego procesado por varios subcontratistas especializados del CCNSC, y una de las muestras del árbol resultó ser citotóxica en un ensayo celular el 22 de mayo de 1964.
Por consiguiente, a finales de 1964 o principios de 1965, el laboratorio de fraccionamiento y aislamiento dirigido por Monroe E. Wall en Research Triangle Park, Carolina del Norte, comenzó a trabajar en muestras frescas de Taxus, aislando el ingrediente activo en septiembre de 1966 y anunciando sus hallazgos en una reunión de la Sociedad Química Americana en abril de 1967 en Miami Beach. Wall y su colega Wani publicaron sus resultados, incluyendo la estructura química, en 1971.
Paso a la siguiente etapa de investigación
El NCI siguió encargando trabajos para recoger más corteza de Taxus y aislar cantidades cada vez mayores de taxol. Para 1969, se habían aislado 28 kg (62 lb) de extracto crudo de casi 1.200 kg (2.600 lb) de corteza, aunque finalmente sólo se obtuvieron 10 g (0,35 oz) de material puro, pero durante varios años, el NCI no hizo uso del compuesto. En 1975 se demostró que era activo en otro sistema in vitro; dos años más tarde, un nuevo jefe de departamento revisó los datos y finalmente recomendó que el taxol pasara a la siguiente etapa del proceso de descubrimiento, lo que requería cantidades cada vez mayores de taxol purificado, hasta 600 g (21 oz), y en 1977 se hizo otra solicitud de 3.200 kg (7.000 lb) de corteza.
En 1978, dos investigadores del NCI publicaron un informe que demostraba que el taxol era ligeramente efectivo en ratones leucémicos. En noviembre de 1978, se demostró que el taxol era efectivo en estudios de xenoinjertos. Mientras tanto, el taxol comenzó a ser bien conocido en la biología celular, así como en la comunidad del cáncer, con una publicación a principios de 1979 de Susan B. Horwitz, una farmacóloga molecular de la Facultad de Medicina Albert Einstein, que demostraba que el taxol tenía un mecanismo de acción previamente desconocido que implicaba la estabilización de los microtúbulos.
Junto con los problemas de formulación, este mayor interés de los investigadores hizo que, para 1980, el NCI previera la necesidad de recoger 9.100 kg (20.000 libras) de corteza. Los estudios de toxicología animal se completaron en junio de 1982, y en noviembre el NCI solicitó el IND necesario para iniciar los ensayos clínicos en humanos.
Los primeros ensayos clínicos, el suministro y la transferencia a BMS
Los ensayos clínicos de la fase I comenzaron en abril de 1984, y la decisión de comenzar los ensayos de la fase II se tomó un año más tarde. Estos ensayos más grandes necesitaron más corteza y se encargó la recolección de otras 12.000 libras, lo que permitió que algunos ensayos de la fase II comenzaran a finales de 1986. Pero para entonces se reconoció que la demanda de taxol podría ser sustancial y que se necesitarían más de 60.000 libras de corteza como mínimo. Esta cantidad sin precedentes hizo que las preocupaciones ecológicas sobre el impacto en las poblaciones de tejo se pusieran de manifiesto por primera vez, ya que los políticos y silvicultores locales expresaron su malestar por el programa.
El primer informe público de un ensayo de fase II en mayo de 1988 mostró efectos prometedores en el melanoma y el cáncer de ovario refractario. En ese momento, Gordon Cragg, de la Rama de Productos Naturales del NCI, calculó que la síntesis de suficiente taxol para tratar todos los casos de cáncer de ovario y melanoma en los EE.UU. requeriría la destrucción de 360.000 árboles anualmente. Por primera vez se consideró seriamente el problema del suministro.
Debido a la escala práctica y, en particular, financiera del programa necesario, el NCI decidió buscar la asociación con una empresa farmacéutica, y en agosto de 1989 publicó un Acuerdo de Cooperación en Investigación y Desarrollo (CRADA) que ofrecía sus existencias actuales y el suministro de las actuales existencias de corteza, así como el acceso de propiedad a los datos recogidos hasta el momento, a una empresa dispuesta a comprometerse a proporcionar los fondos para recoger más materia prima, aislar el taxol y financiar una gran proporción de los ensayos clínicos. En palabras de Goodman y Welsh, autores de un importante libro académico sobre el taxol, «El NCI no pensaba en la colaboración, … sino en un traspaso del taxol (y sus problemas)».
Aunque la oferta fue ampliamente publicitada, sólo cuatro empresas respondieron a la CRADA, incluida la empresa estadounidense Bristol-Myers Squibb (BMS), que fue seleccionada como socia en diciembre de 1989. La elección de BMS se volvió controvertida y fue objeto de audiencias en el Congreso en 1991 y 1992. Si bien parece claro que el NCI no tenía otra opción que buscar un socio comercial, también hubo controversia sobre los términos del acuerdo, lo que finalmente condujo a un informe de la Oficina de Contabilidad General en 2003, en el que se concluía que el NIH no había logrado asegurar la rentabilidad del dinero.
En los CRADAs relacionados con el Departamento de Agricultura de los Estados Unidos y el Departamento del Interior, se concedió a Bristol-Myers Squibb la primacía exclusiva en todos los suministros federales de Taxus brevifolia. Este contrato exclusivo llevó a algunas críticas por dar a BMS un «monopolio del cáncer». Dieciocho meses después del CRADA, BMS presentó una solicitud de nuevo medicamento (NDA), que fue aprobada por la FDA a finales de 1992. Aunque no había ninguna patente sobre el compuesto, las disposiciones de la Ley Waxman-Hatch dieron a Bristol-Myers Squibb cinco años de derechos exclusivos de comercialización.
Controversia sobre el nombre taxol
En 1990, BMS solicitó la marca registrada del nombre Taxol como Taxol(R). Esto fue aprobado de forma controvertida en 1992. Al mismo tiempo, paclitaxel reemplazó a taxol como el nombre genérico (DCI) del compuesto. Los críticos, incluida la revista Nature, argumentaron que el nombre taxol se había utilizado durante más de dos décadas y en más de 600 artículos científicos y sugirieron que la marca no debería haber sido concedida y que BMS debería renunciar a sus derechos sobre ella.
BMS argumentó que cambiar el nombre causaría confusión entre los oncólogos y posiblemente pondría en peligro la salud de los pacientes. BMS ha seguido defendiendo sus derechos sobre el nombre en los tribunales. BMS también ha sido criticada por la tergiversación de Goodman y Walsh, que citan un informe de la empresa que dice: «No fue hasta 1971 que … las pruebas … permitieron el aislamiento del paclitaxel, inicialmente descrito como ‘compuesto 17′». Esta cita es, en sentido estricto, exacta: la objeción parece ser que esta engañosa omisión explica que fue el científico que hizo el aislamiento quien nombró al compuesto taxol y no se le hizo ninguna otra referencia durante más de veinte años. Las ventas anuales alcanzaron un máximo en 2000, llegando a 1.600 millones de dólares de los EE.UU.; el paclitaxel está disponible ahora en forma genérica.
Nomenclatura del paclitaxel
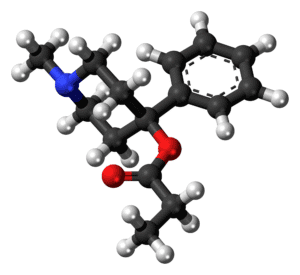
La nomenclatura para el paclitaxel está estructurada en un esqueleto tetracíclico de 17 átomos. Hay un total de 11 estereocentros. El estereoisómero activo es (-)-paclitaxel.


Síntesis y producción del paclitaxel
Procesamiento de la corteza
De 1967 a 1993, casi todo el paclitaxel producido se derivó de la corteza del tejo del Pacífico, Taxus brevifolia, cuya recolección mata al árbol en el proceso. Los procesos utilizados fueron descendientes del método original de aislamiento de Monroe Wall y Mansukh Wani; para 1987, el Instituto Nacional del Cáncer (NCI) de EE.UU. había contratado a Hauser Chemical Research de Boulder, Colorado, para manipular la corteza a la escala necesaria para los ensayos de las fases II y III.
Aunque tanto el tamaño de la población silvestre de tejo del Pacífico como la magnitud de la eventual demanda de paclitaxel eran inciertos, estaba claro que se necesitaría una fuente alternativa y sostenible del producto natural. Los intentos iniciales de ampliar su fuente utilizaban agujas del árbol, o material de otras especies de Taxus afines, incluidas las cultivadas, pero estos intentos se vieron desafiados por los rendimientos relativamente bajos y a menudo muy variables que se obtuvieron. A principios del decenio de 1990, coincidiendo con el aumento de la sensibilidad a la ecología de los bosques del noroeste del Pacífico, se extrajo paclitaxel con éxito a escala clínicamente útil de estas fuentes
Semisíntesis
Al mismo tiempo, los químicos sintéticos de los Estados Unidos y Francia se habían interesado por el paclitaxel, a partir de finales del decenio de 1970. Como se ha señalado, en 1992 se estaban realizando grandes esfuerzos para lograr la síntesis total del paclitaxel, esfuerzos motivados por el deseo de generar nuevos conocimientos químicos en lugar de lograr una producción comercial práctica.
En cambio, el grupo francés de Pierre Potier del Centre national de la recherche scientifique (CNRS) se ocupó de la cuestión del rendimiento global del proceso, demostrando que era factible aislar cantidades relativamente grandes del compuesto 10-deacetilbaccatin del tejo europeo, Taxus baccata, que crecía en el campus del CNRS y cuyas agujas estaban disponibles en gran cantidad. En virtud de su estructura, la 10-deacetilbaccatina se consideraba un material de partida viable para una corta semisíntesis para producir paclitaxel. Para 1988, Poitier y sus colaboradores habían publicado una ruta semisintética desde las agujas del tejo europeo hasta el paclitaxel.
La opinión del NCI, sin embargo, era que incluso esta ruta no era práctica. El grupo de Robert A. Holton también había seguido una ruta práctica de producción semisintética; a finales de 1989, el grupo de Holton había desarrollado una ruta semisintética al paclitaxel con el doble de rendimiento que el proceso de Potier. La Universidad Estatal de Florida, donde Holton trabajó, firmó un acuerdo con Bristol-Myers Squibb (BMS) para licenciar su semisíntesis y futuras patentes.
En 1992, Holton patentó un proceso mejorado con un rendimiento del 80%, y BMS tomó el proceso en sus instalaciones y comenzó a fabricar paclitaxel en Irlanda a partir de 10 deacetilbaccatin aislado de las agujas del tejo europeo. A principios de 1993, BMS anunció que dejaría de depender de la corteza del tejo del Pacífico a finales de 1995, poniendo fin efectivamente a la controversia ecológica sobre su uso. Este anuncio también hizo realidad su compromiso de desarrollar una ruta de suministro alternativa, hecho al NCI en su aplicación del acuerdo de cooperación para la investigación y el desarrollo (CRADA) de 1989.
A partir de 2013, BMS estaba usando el método semisintético utilizando agujas de tejo europeo para producir paclitaxel. Otra compañía que trabajó con BMS hasta 2012, Phyton Biotech, Inc, utiliza la tecnología de fermentación de células vegetales (PCF). Al cultivar una línea específica de células de Taxus en tanques de fermentación, ya no necesitan una fuente continua de material procedente de plantaciones reales de tejo. El paclitaxel es entonces purificado directamente del caldo de suspensión por una resina que permite la concentración a un polvo altamente enriquecido que contiene alrededor de un 40% de paclitaxel. El compuesto es luego purificado por un paso cromatográfico seguido de la cristalización. Comparado con el método de semisíntesis, el PCF elimina la necesidad de muchos productos químicos peligrosos y ahorra una cantidad considerable de energía.
En 1993, se descubrió el paclitaxel como un producto natural en un hongo endofítico recientemente descrito que vive en el tejo. Desde entonces se ha notificado su presencia en varios otros hongos endofitos, entre ellos el Nodulisporium sylviforme, Alternaria taxi, Cladosporium cladosporioides MD2, Metarhizium anisopliae, Aspergillus candidus MD3, Mucor rouxianus, Chaetomella raphigera, Phyllosticta tabernaemontanae, Phomopsis, Pestalotiopsis pauciseta, Phyllosticta citricarpa, Podocarpus sp. , Fusarium solani, Pestalotiopsis terminaliae, Pestalotiopsis breviseta, Botryodiplodia theobromae, Gliocladium sp., Alternaria alternata var. monosporus, Cladosporium cladosporioides, Nigrospora sp., Pestalotiopsis versicolor y Taxomyces andreanae. Sin embargo, ha habido pruebas contradictorias sobre su producción por parte de los endofitos, y es poco probable que otros estudios encuentren una producción independiente.
Biosíntesis
La ruta sintética central se realiza por una vía terpenoide, algunas de cuyas partes se han transplantado con éxito a cepas productoras de E. coli y levaduras.
Síntesis total
En 1992, al menos treinta equipos de investigación académica de todo el mundo trabajaban para lograr una síntesis total de este producto natural, y la síntesis procedía de productos naturales simples y otros materiales de partida fácilmente disponibles. Este esfuerzo de síntesis total fue motivado principalmente por el deseo de generar nuevos conocimientos químicos, más que por la expectativa de la producción comercial práctica de paclitaxel.
Los primeros laboratorios en completar la síntesis total a partir de materiales de partida mucho menos complejos fueron los grupos de investigación de Robert A. Holton, que tuvo el primer artículo aceptado para su publicación, y de K. C. Nicolaou, que tuvo el primer artículo que apareció en la prensa (por una semana, el 7 de febrero de 1994). Aunque la presentación de Holton precedió a la de Nicolaou por un mes (21 de diciembre de 1993 contra 24 de enero de 1994), la casi coincidencia de las publicaciones surgidas de cada uno de estos esfuerzos masivos y plurianuales -11-18 autores que aparecen en cada una de las publicaciones de febrero de 1994- ha llevado a que el final de la carrera sea calificado como un «empate» o un «photo finish», aunque cada grupo ha argumentado que su estrategia y tácticas sintéticas eran superiores.
Hasta 2006, otros cinco grupos de investigación habían informado de la realización con éxito de síntesis totales de paclitaxel: Wender y otros en 1997, y Kuwajima y otros y Mukaiyama y otros en 1998 con más síntesis lineales, y Danishefsky y otros en 1996 y Takahashi y otros en 2006 con más síntesis convergentes. Hasta esa fecha, todas las estrategias habían tenido como objetivo preparar un núcleo de tipo 10-deacetilbaccatin que contenía el sistema de anillos ABCD, seguido generalmente por la adición en la última etapa de la «cola» al grupo 13-hidroxilo.
Para más información Taxol – Chemocare