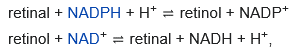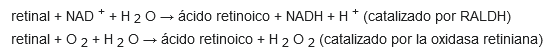Retinal
Tiempo de lectura estimado: 5 minutos
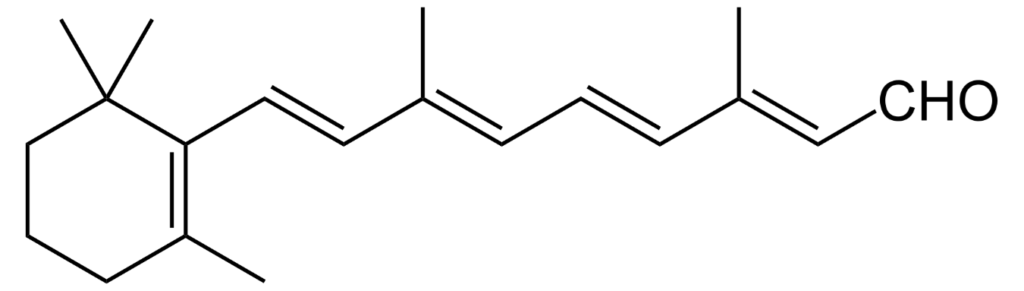
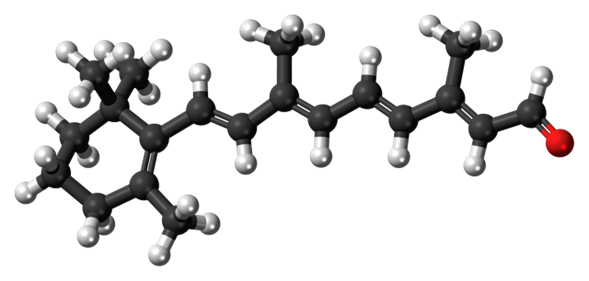
El retinal (también conocido como retinaldehído) es un cromóforo polieno. El retinal, unido a unas proteínas llamadas opsinas, es la base química de la fototransducción visual, la etapa de detección de la luz en la percepción visual (visión).
El bioquímico estadounidense George Wald y otros habían esbozado el ciclo visual en 1958. Por su trabajo, Wald ganó una parte del Premio Nobel de Fisiología o Medicina de 1967 con Haldan Keffer Hartline y Ragnar Granit
Algunos microorganismos utilizan el retinal para convertir la luz en energía metabólica.
La química de la visión
Existen muchas formas de vitamina A, todas ellas convertidas en retinal, que no puede fabricarse sin ellas. El propio retinal se considera una forma de vitamina A cuando es ingerido por un animal. El número de moléculas diferentes que pueden convertirse en retinal varía de una especie a otra. Esta molécula se llamaba originalmente retineno, y se le cambió el nombre después de que se descubriera que era un aldehído de la vitamina A.
Los animales vertebrados ingieren el retinal directamente de la carne, o lo producen a partir de los carotenoides, ya sea del α-caroteno o del β-caroteno, ambos carotenos. También la producen a partir de la β-criptoxantina, un tipo de xantofila. Estos carotenoides deben obtenerse de plantas u otros organismos fotosintéticos. Los animales no pueden convertir ningún otro carotenoide en retinal. Algunos carnívoros no pueden convertir ningún carotenoide. Las otras formas principales de vitamina A -el retinol y una forma parcialmente activa, el ácido retinoico- pueden producirse a partir de este compuesto.
Los invertebrados, como los insectos y los calamares, utilizan formas hidroxiladas de retinal en sus sistemas visuales, que derivan de la conversión de otras xantofilas.
Metabolismo de vitamina A
Los organismos vivos producen retinal por escisión oxidativa irreversible de los carotenoides, catalizada por una beta-caroteno 15,15′-monooxigenasa o una beta-caroteno 15,15′-dioxigenasa.
Al igual que los carotenoides son los precursores del retinal, el retinal es el precursor de las otras formas de vitamina A. El retinal es interconvertible con el retinol, la forma de transporte y almacenamiento de la vitamina A
catalizada por las retinol deshidrogenasas (RDHs) y las alcohol deshidrogenasas (ADHs).
El retinol se denomina alcohol de vitamina A o, más a menudo, simplemente vitamina A. El retinal también puede oxidarse a ácido retinoico catalizada por las retinal deshidrogenasas también conocidas como retinaldehído deshidrogenasas (RALDHs) así como por las retinal oxidasas.
El ácido retinoico, a veces llamado vitamina A, es una importante molécula de señalización y hormona en los animales vertebrados.
Retinal y visión
El retinal es un cromóforo conjugado. En el ojo humano, el retinal comienza con una configuración de 11-cis-retinal, que -al captar un fotón de la longitud de onda correcta- se endereza a una configuración totalmente trans-retinal. Este cambio de configuración empuja a una proteína opsina de la retina, lo que desencadena una cascada de señales químicas que puede dar lugar a la percepción de la luz o de las imágenes por parte del cerebro humano.
El espectro de absorción del cromóforo depende de sus interacciones con la proteína opsina a la que está unido, de modo que diferentes complejos retina-opsina absorberán fotones de diferentes longitudes de onda (es decir, diferentes colores de luz).
La universalidad de la visión
Pero el retinal es aún más universal que eso. Sólo hay 3 tipos de ojos que pueden resolver imágenes, los que se encuentran en moluscos, artrópodos y vertebrados. Los tres tipos de ojos son anatómicamente muy diferentes y probablemente evolucionaron de forma independiente. Sin embargo, todos utilizan el 11-cis-retinal como molécula receptora de luz.
Hay muchas razones para ello. En primer lugar, el 11-cis-retinal es extremadamente sensible a la luz y la absorbe con mucha fuerza. Además, esta absorción puede desplazarse fácilmente a la región visible del espectro. En segundo lugar, en ausencia de luz, la molécula es muy estable, es decir, no se isomera en la oscuridad. Si esto no fuera cierto, estaríamos constantemente plagados de imágenes falsas. En tercer lugar, el cambio estructural producido por la isomerización es relativamente grande (más de 7 Å), suficiente para generar un impulso nervioso. Y, por último, los precursores del 11-cis-retinal, los carotenos, están fácilmente disponibles en diversas plantas comestibles.
Para más información Retinal