Tiempo de lectura estimado: 5 minutos
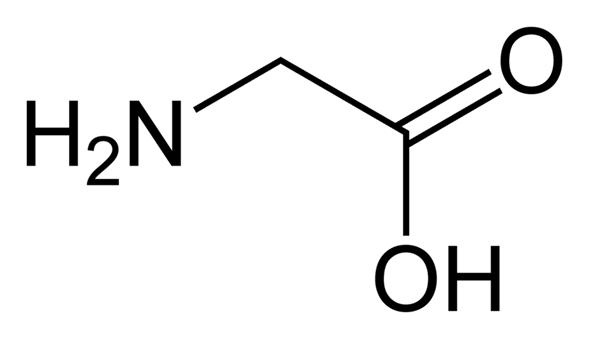
La glicina es un aminoácido que tiene un único átomo de hidrógeno como cadena lateral. Es el aminoácido estable más simple (el ácido carbámico es inestable), con la fórmula química NH2-CH2-COOH. La glicina es uno de los aminoácidos proteinogénicos. Está codificada por todos los codones que empiezan por GG (GGU, GGC, GGA, GGG).
La glicina forma parte integrante de la formación de hélices alfa en la estructura secundaria de las proteínas debido a su forma compacta. Por la misma razón, es el aminoácido más abundante en las triple-hélices del colágeno. La glicina también es un neurotransmisor inhibidor: la interferencia con su liberación en la médula espinal (como durante una infección por Clostridium tetani) puede causar parálisis espástica debido a la contracción muscular desinhibida.
Es el único aminoácido proteinogénico aquiral. Puede encajar en entornos hidrofílicos o hidrofóbicos, debido a su cadena lateral mínima de un solo átomo de hidrógeno.
Historia de la glicina
La glicina fue descubierta en 1820 por el químico francés Henri Braconnot cuando hidrolizó gelatina hirviéndola con ácido sulfúrico. Originalmente la llamó «azúcar de gelatina», pero el químico francés Jean-Baptiste Boussingault demostró que contenía nitrógeno.
El científico estadounidense Eben Norton Horsford, entonces alumno del químico alemán Justus von Liebig, propuso el nombre de «glicocola»; sin embargo, el químico sueco Berzelius sugirió el nombre más sencillo de «glicina». El nombre procede de la palabra griega γλυκύς «de sabor dulce» (que también está relacionada con los prefijos glyco- y gluco-, como en glicoproteína y glucosa). En 1858, el químico francés Auguste Cahours determinó que la glicina era una amina del ácido acético.
Síntesis y producción
Aunque la glicina se puede aislar a partir de proteínas hidrolizadas, esta vía no se utiliza para la producción industrial, ya que se puede fabricar más cómodamente mediante síntesis química. Los dos procesos principales son la aminación del ácido cloroacético con amoniaco, que da glicina y cloruro de amonio, y la síntesis de aminoácidos de Strecker, que es el principal método sintético en Estados Unidos y Japón. Anualmente se producen unas 15.000 toneladas de esta forma.
La glicina también se cogenera como impureza en la síntesis de EDTA, a partir de reacciones del coproducto amoniaco.
Biosíntesis
La glicina no es esencial para la dieta humana, ya que se biosintetiza en el cuerpo a partir del aminoácido serina, que a su vez se deriva del 3-fosfoglicerato, pero la capacidad metabólica para la biosíntesis de glicina no satisface la necesidad de síntesis de colágeno. En la mayoría de los organismos, la enzima serina hidroximetiltransferasa cataliza esta transformación a través del cofactor piridoxal fosfato.
En el hígado de los vertebrados, la síntesis de glicina es catalizada por la glicina sintasa (también llamada enzima de escisión de la glicina). Esta conversión es fácilmente reversible.
Además de sintetizarse a partir de la serina, la glicina también puede derivarse de la treonina, la colina o la hidroxiprolina a través del metabolismo interorgánico del hígado y los riñones.
Usos de la glicina
La glicina no se utiliza mucho en los alimentos por su valor nutritivo, excepto en infusiones. En cambio, la función de la glicina en la química alimentaria es como saborizante. Es ligeramente dulce y contrarresta el regusto de la sacarina. También tiene propiedades conservantes, quizá debido a su formación de complejos con iones metálicos. Los complejos de glicinato metálico, como el glicinato de cobre (II), se utilizan como suplementos para piensos.
La glicina es un intermediario en la síntesis de diversos productos químicos. Se utiliza en la fabricación de los herbicidas glifosato, iprodiona, glifosina, imiprotrina y eglinazina. Se utiliza como intermediario de medicamentos como el tianfenicol.
La glicina es un componente importante de algunas soluciones utilizadas en el método SDS-PAGE de análisis de proteínas. Sirve como agente tampón, manteniendo el pH y previniendo el daño de la muestra durante la electroforesis. La glicina también se utiliza para eliminar los anticuerpos marcadores de proteínas de las membranas de Western blot para permitir el sondeo de numerosas proteínas de interés a partir del gel SDS-PAGE. Esto permite obtener más datos de la misma muestra, lo que aumenta la fiabilidad de los datos, reduce la cantidad de procesamiento de muestras y el número de muestras necesarias. Este proceso se conoce como stripping.
Glicina en el espacio
La presencia de glicina fuera de la Tierra se confirmó en 2009, a partir del análisis de muestras que la nave espacial Stardust de la NASA había tomado en 2004 del cometa Wild 2 y posteriormente devuelto a la Tierra. La glicina había sido identificada previamente en el meteorito Murchison en 1970.
El descubrimiento de glicina en el espacio exterior reforzó la hipótesis de la llamada soft-panspermia, que afirma que los «ladrillos» de la vida están extendidos por todo el universo. En 2016, se anunció la detección de glicina en el interior del cometa 67P/Churyumov-Gerasimenko por la nave espacial Rosetta.
La detección de glicina fuera del Sistema Solar, en el medio interestelar, ha sido objeto de debate. En 2008, el Instituto Max Planck de Radioastronomía descubrió las líneas espectrales de un precursor de la glicina (aminoacetonitrilo) en la Gran Molécula Heimat, una nube de gas gigante cerca del centro galáctico en la constelación de Sagitario.
Para más información Glycine
Como citar este artículo:
APA: (2023-02-21). Glicina. Recuperado de https://quimicafacil.net/compuesto-de-la-semana/glicina/
ACS: . Glicina. https://quimicafacil.net/compuesto-de-la-semana/glicina/. Fecha de consulta 2026-03-04.
IEEE: , "Glicina," https://quimicafacil.net/compuesto-de-la-semana/glicina/, fecha de consulta 2026-03-04.
Vancouver: . Glicina. [Internet]. 2023-02-21 [citado 2026-03-04]. Disponible en: https://quimicafacil.net/compuesto-de-la-semana/glicina/.
MLA: . "Glicina." https://quimicafacil.net/compuesto-de-la-semana/glicina/. 2023-02-21. Web.
Si tiene alguna pregunta o sugerencia, escribe a administracion@quimicafacil.net, o visita Como citar quimicafacil.net