Tiempo de lectura estimado: 3 minutos
La extracción cuantitativa sirve de herramienta para estimar la cantidad de un compuesto de interés presente en una muestra.
Extracción cuantitativa simple
La hiosciamina es un alcaloide de una planta de la familia de las solanáceas (Figura 1a), y se utiliza medicinalmente para aliviar una serie de trastornos gastrointestinales. Sus datos de solubilidad se muestran en la Figura 1b.

Imagínese que una solución casi saturada de 0,50 g de hiosciamina en 150 mL de agua se va a extraer en 150 mL de éter dietílico. ¿Qué cantidad de hiosciamina se extraería en la capa de éter dietílico en este proceso?
Esta cantidad puede aproximarse utilizando los datos de solubilidad. Tomando la relación de la solubilidad del compuesto en éter dietílico en comparación con el agua se obtiene un K de 4.
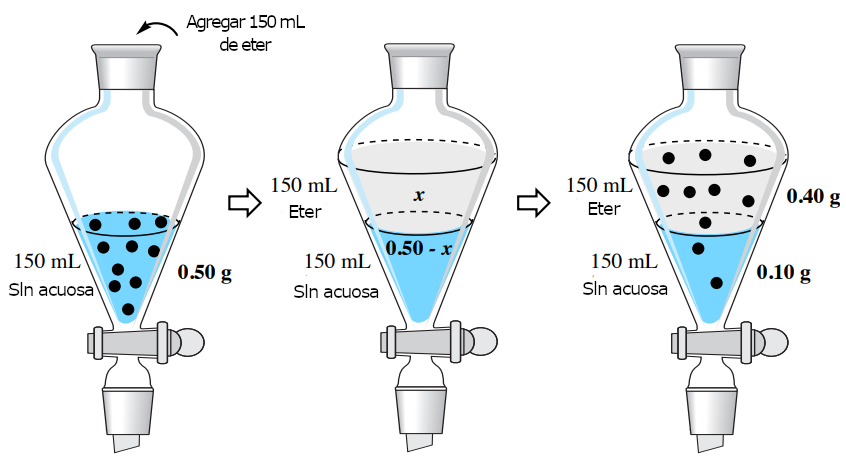
Si «x» es la cantidad en gramos de hiosciamina extraída en la capa de éter dietílico, entonces «0,50g-x» quedaría en la capa acuosa después de establecer el equilibrio. Conociendo el valor de K, se puede resolver el valor de x mediante la siguiente ecuación.
Después de resolver el álgebra, x=0,40 g. Este resultado significa que 0,40g de los 0,50g originales de hiosciamina se extraen en el éter dietílico utilizando una sola extracción. Este proceso se resume en la figura 2.
En este ejemplo, una sola extracción dio como resultado la extracción del 80% de la hiosciamina (100%×0,40g/0,50g) de la capa acuosa a la capa orgánica. La partición del compuesto entre las dos capas hizo que la muestra se extrajera de forma incompleta.
Para más información Extraction Theory
Como citar este artículo:
APA: (2021-10-20). Extracción cuantitativa. Recuperado de https://quimicafacil.net/tecnicas-de-laboratorio/extraccion-cuantitativa/
ACS: . Extracción cuantitativa. https://quimicafacil.net/tecnicas-de-laboratorio/extraccion-cuantitativa/. Fecha de consulta 2025-07-05.
IEEE: , "Extracción cuantitativa," https://quimicafacil.net/tecnicas-de-laboratorio/extraccion-cuantitativa/, fecha de consulta 2025-07-05.
Vancouver: . Extracción cuantitativa. [Internet]. 2021-10-20 [citado 2025-07-05]. Disponible en: https://quimicafacil.net/tecnicas-de-laboratorio/extraccion-cuantitativa/.
MLA: . "Extracción cuantitativa." https://quimicafacil.net/tecnicas-de-laboratorio/extraccion-cuantitativa/. 2021-10-20. Web.
Si tiene alguna pregunta o sugerencia, escribe a administracion@quimicafacil.net, o visita Como citar quimicafacil.net