Tiempo de lectura estimado: 14 minutos
El Premio Nobel de Química 2019 se otorgó a John B. Goodenough, M. Stanley Whittingham y Akira Yoshino por sus contribuciones al desarrollo de la batería de iones de litio. Esta batería recargable sentó las bases de la electrónica inalámbrica, como los teléfonos móviles y los ordenadores portátiles. También hace posible un mundo libre de combustibles fósiles, ya que se utiliza para todo, desde la propulsión de coches eléctricos hasta el almacenamiento de energía procedente de fuentes renovables.
- Desarrollaron la batería más potente del mundo
- La bruma de la gasolina revitaliza la investigación sobre baterías
- Las compañías petroleras invierten en nuevas tecnologías
- Whittingham descubre un material extremadamente denso en energía
- Litio en el electrodo negativo
- La batería explota y el precio del petróleo cae.
- La crisis del petróleo hace que Goodenough se interese por las baterías
- Altos voltajes cuando los iones de litio se esconden en el óxido de cobalto
- Las empresas japonesas quieren baterías ligeras para la nueva electrónica
- Yoshino construye la primera batería de iones de litio comercialmente viable
- La batería de iones de litio, necesaria para una sociedad sin combustibles fósiles
Desarrollaron la batería más potente del mundo
Un elemento rara vez llega a jugar un papel central en un drama, pero la historia del Premio Nobel de Química de 2019 tiene un claro protagonista: el litio, un elemento antiguo que fue creado durante los primeros minutos del Big Bang. La humanidad lo conoció en 1817, cuando los químicos suecos Johan August Arfwedson y Jöns Jacob Berzelius lo purificaron a partir de una muestra de mineral de la mina de Utö, en el archipiélago de Estocolmo.
Berzelius nombró el nuevo elemento como la palabra griega para piedra, lithos. A pesar de su nombre pesado, es el elemento sólido más ligero, por lo que apenas nos damos cuenta de los teléfonos móviles que ahora llevamos.
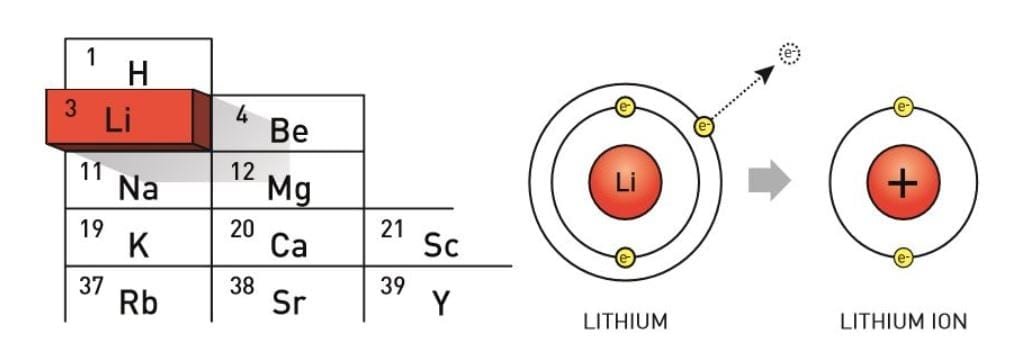
Para ser completamente correctos, los químicos suecos no encontraron litio metálico puro, sino iones de litio en forma de sal. El litio puro ha disparado muchas alarmas de incendio, sobre todo en la historia que vamos a contar aquí; es un elemento inestable que debe almacenarse en el aceite para que no reaccione con el aire.
La debilidad del litio – su reactividad – es también su fuerza. A principios de la década de 1970, Stanley Whittingham utilizó el enorme impulso del litio para liberar su electrón exterior cuando desarrolló la primera batería de litio funcional.
En 1980, John Goodenough duplicó el potencial de la batería, creando las condiciones adecuadas para una batería mucho más potente y útil. En 1985, Akira Yoshino consiguió eliminar el litio puro de la batería, basándola en su totalidad en iones de litio, que son más seguros que el litio puro. Esto hizo que la batería funcionara en la práctica.
Las baterías de iones de litio han aportado el mayor beneficio a la humanidad, ya que han permitido el desarrollo de ordenadores portátiles, teléfonos móviles, vehículos eléctricos y el almacenamiento de la energía generada por la energía solar y eólica.
Ahora retrocederemos cincuenta años en el tiempo, hasta el comienzo de la historia de la batería de iones de litio.
La bruma de la gasolina revitaliza la investigación sobre baterías
A mediados del siglo XX, el número de automóviles propulsados por gasolina en el mundo aumentó significativamente, y sus gases de escape empeoraron el nocivo smog que se encuentra en las grandes ciudades.
Esto, combinado con la creciente comprensión de que el petróleo es un recurso finito, hizo sonar una alarma tanto para los fabricantes de vehículos como para las compañías petroleras. Necesitaban invertir en vehículos eléctricos y fuentes alternativas de energía para que sus negocios pudieran sobrevivir.
Los vehículos eléctricos y las fuentes alternativas de energía requieren baterías potentes que puedan almacenar grandes cantidades de energía. En realidad, sólo había dos tipos de baterías recargables en el mercado en ese momento: la batería de plomo pesado que se había inventado en 1859 (y que todavía se utiliza como batería de arranque en los coches de gasolina) y la batería de níquel-cadmio que se desarrolló en la primera mitad del siglo XX.
Las compañías petroleras invierten en nuevas tecnologías
La amenaza de que se agotara el petróleo hizo que una empresa petrolera, Exxon, decidiera diversificar sus actividades. En una importante inversión en investigación básica, contrataron a algunos de los principales investigadores de la época en el campo de la energía, lo que les dio la libertad de hacer prácticamente lo que quisieran, siempre y cuando no se tratara de petróleo.
Stanley Whittingham fue uno de los que se mudaron a Exxon en 1972. Vino de la Universidad de Stanford, donde su investigación había incluido materiales sólidos con espacios del tamaño de un átomo en los que los iones cargados pueden adherirse. Este fenómeno se denomina intercalación.
Las propiedades de los materiales cambian cuando los iones son atrapados dentro de ellos. En Exxon, Stanley Whittingham y sus colegas comenzaron a investigar los materiales superconductores, incluyendo el disulfuro de tántalo, que puede intercalar iones. Añadieron iones al disulfuro de tántalo y estudiaron cómo se veía afectada su conductividad.
Whittingham descubre un material extremadamente denso en energía
Como ocurre a menudo en la ciencia, este experimento condujo a un descubrimiento inesperado y valioso. Resultó que los iones de potasio afectaban la conductividad del disulfuro de tántalo, y cuando Stanley Whittingham comenzó a estudiar el material en detalle observó que tenía una densidad de energía muy alta.
Las interacciones que surgieron entre los iones de potasio y el disulfuro de tántalo fueron sorprendentemente ricas en energía y, cuando midió el voltaje del material, fue de un par de voltios. Esto era mejor que muchas de las baterías de esa época.
Stanley Whittingham se dio cuenta rápidamente de que era hora de cambiar de rumbo, pasando al desarrollo de nuevas tecnologías que pudieran almacenar energía para los vehículos eléctricos del futuro. Sin embargo, el tántalo es uno de los elementos más pesados y el mercado no necesitaba baterías más pesadas, por lo que reemplazó el tántalo por titanio, un elemento que tiene propiedades similares, pero es mucho más ligero.
Litio en el electrodo negativo
¿No se supone que el litio ocupa un lugar de honor en esta historia? Bueno, aquí es donde el litio entra en la narración, como el electrodo negativo de la innovadora batería de Stanley Whittingham.
El litio no fue una elección aleatoria; en una batería, los electrones deben fluir desde el electrodo negativo – el ánodo – hasta el positivo – el cátodo. Por lo tanto, el ánodo debe contener un material que desprenda fácilmente sus electrones y, de todos los elementos, el litio es el que más voluntariamente libera electrones.
El resultado fue una batería recargable de litio que funcionaba a temperatura ambiente y que, literalmente, tenía un gran potencial. Stanley Whittingham viajó a la sede de Exxon en Nueva York para hablar sobre el proyecto. La reunión duró unos quince minutos, y el grupo de gestión tomó una decisión rápida: desarrollarían una batería comercialmente viable utilizando el descubrimiento de Whittingham.
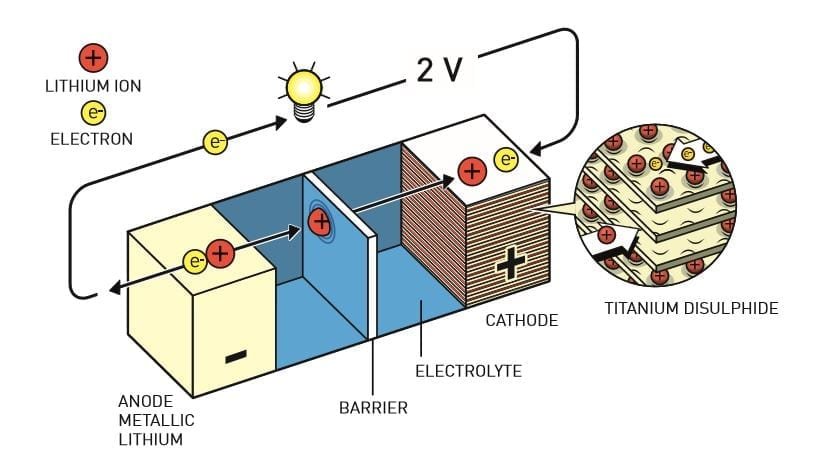
La batería explota y el precio del petróleo cae.
Desafortunadamente, el grupo que iba a empezar a producir la batería sufrió algunos contratiempos. A medida que la nueva batería de litio se cargaba repetidamente, delgados bigotes (whiskers) de litio crecían a partir del electrodo de litio.
Al llegar al otro electrodo, la batería se cortocircuitó, lo que podría provocar una explosión. Los bomberos tuvieron que apagar varios incendios y finalmente amenazaron con hacer pagar al laboratorio por los productos químicos especiales utilizados para extinguir los incendios de litio.
Para hacer la batería más segura, se añadió aluminio al electrodo metálico de litio y se cambió el electrolito entre los electrodos. Stanley Whittingham anunció su descubrimiento en 1976 y la batería comenzó a fabricarse a pequeña escala para un relojero suizo que quería utilizarla en relojes solares.
El siguiente objetivo era aumentar la escala de la batería de litio recargable para que pudiera alimentar a un coche. Sin embargo, el precio del petróleo cayó drásticamente a principios de la década de 1980 y Exxon tuvo que hacer recortes. El trabajo de desarrollo se interrumpió y la tecnología de baterías de Whittingham fue licenciada a tres compañías diferentes en tres partes diferentes del mundo.
Sin embargo, esto no significa que el desarrollo se haya detenido. Cuando Exxon se rindió, John Goodenough se hizo cargo.
La crisis del petróleo hace que Goodenough se interese por las baterías
De niño, John Goodenough tuvo problemas significativos para aprender a leer, lo cual fue una de las razones por las que se sintió atraído por las matemáticas y eventualmente – después de la Segunda Guerra Mundial – también por la física.
Trabajó durante muchos años en el Lincoln Laboratory del Massachusetts Institute of Technology, MIT. Mientras estuvo allí, contribuyó al desarrollo de la memoria de acceso aleatorio (RAM), que sigue siendo un componente fundamental de la informática.
John Goodenough, como tantas otras personas en la década de 1970, se vio afectado por la crisis del petróleo y quería contribuir al desarrollo de fuentes alternativas de energía. Sin embargo, el Laboratorio Lincoln era financiado por la Fuerza Aérea de los Estados Unidos y no permitió todo tipo de investigación, por lo que cuando se le ofreció un puesto como profesor de química inorgánica en la Universidad de Oxford en Gran Bretaña, aprovechó la oportunidad y entró en el importante mundo de la investigación energética.
Altos voltajes cuando los iones de litio se esconden en el óxido de cobalto
John Goodenough conocía la revolucionaria batería de Whittingham, pero su conocimiento especializado del interior de la materia le dijo que su cátodo podría tener un mayor potencial si se construyera utilizando un óxido de metal en lugar de un sulfuro de metal. A algunas personas de su grupo de investigación se les asignó la tarea de encontrar un óxido metálico que produjera un alto voltaje cuando intercalaba iones de litio, pero que no colapsara cuando se retiraban los iones.
Esta búsqueda sistemática fue más exitosa de lo que John Goodenough se había atrevido a esperar. La batería de Whittingham generó más de dos voltios, pero Goodenough descubrió que la batería con óxido de litio y cobalto en el cátodo era casi el doble de potente, a cuatro voltios.
Una de las claves de este éxito fue que John Goodenough se dio cuenta de que las baterías no tenían que fabricarse en su estado cargado, como ya se había hecho anteriormente. En cambio, podrían ser cargadas después.
En 1980, publicó el descubrimiento de este nuevo material catódico de alta densidad energética que, a pesar de su bajo peso, dio lugar a baterías potentes y de gran capacidad. Este fue un paso decisivo hacia la revolución inalámbrica.

Las empresas japonesas quieren baterías ligeras para la nueva electrónica
Sin embargo, en Occidente, a medida que el petróleo se abarató, el interés se centró en las inversiones en tecnología de energía alternativa y en el desarrollo de vehículos eléctricos.
Las cosas eran diferentes en Japón; las empresas de electrónica estaban desesperadas por baterías ligeras y recargables que pudieran alimentar a la electrónica innovadora, como cámaras de video, teléfonos inalámbricos y computadoras. Una persona que vio esta necesidad fue Akira Yoshino de la Corporación Asahi Kasei. O como él dijo: «Me di cuenta de la dirección en la que se movían las tendencias. Se podría decir que tengo buen olfato».
Yoshino construye la primera batería de iones de litio comercialmente viable
Cuando Akira Yoshino decidió desarrollar una batería recargable funcional, tenía el óxido de litio y cobalto de Goodenough como cátodo e intentó usar varios materiales a base de carbono como ánodo.
Los investigadores habían demostrado anteriormente que los iones de litio podían intercalarse en las capas moleculares del grafito, pero el grafito se descomponía por el electrolito de la batería. El momento eureka de Akira Yoshino llegó cuando en su lugar intentó usar coque de petróleo, un subproducto de la industria petrolera.
Cuando cargó el coque de petróleo con electrones, los iones de litio fueron introducidos en el material. Luego, cuando encendió la batería, los electrones y los iones de litio fluyeron hacia el óxido de cobalto en el cátodo, que tiene un potencial mucho mayor.
La batería desarrollada por Akira Yoshino es estable, ligera, tiene una gran capacidad y produce unos notables cuatro voltios. La mayor ventaja de la batería de iones de litio es que los iones están intercalados en los electrodos.
La mayoría de las demás baterías se basan en reacciones químicas en las que los electrodos se cambian de forma lenta pero segura. Cuando se carga o se utiliza una batería de iones de litio, los iones fluyen entre los electrodos sin reaccionar con su entorno. Esto significa que la batería tiene una larga vida útil y puede cargarse cientos de veces antes de que se deteriore su rendimiento.

Otra gran ventaja es que la batería no tiene litio puro. En 1986, cuando Akira Yoshino estaba probando la seguridad de la batería, tomó precauciones y utilizó una instalación diseñada para probar artefactos explosivos.
Dejó caer un gran pedazo de hierro sobre la batería, pero no pasó nada. Sin embargo, al repetir el experimento con una batería que contenía litio puro, se produjo una violenta explosión.
La aprobación de las pruebas de seguridad fue fundamental para el futuro de la batería. Akira Yoshino dice que este fue «el momento en que nació la batería de iones de litio».
La batería de iones de litio, necesaria para una sociedad sin combustibles fósiles
En 1991, una importante empresa japonesa de electrónica comenzó a vender las primeras baterías de iones de litio, lo que dio lugar a una revolución en la electrónica. Los teléfonos móviles se encogieron, los ordenadores se convirtieron en portátiles y se desarrollaron reproductores de MP3 y tabletas.
Posteriormente, investigadores de todo el mundo han buscado a través de la tabla periódica en busca de baterías aún mejores, pero nadie ha tenido éxito en inventar algo que supere la alta capacidad y voltaje de la batería de litio.
Sin embargo, la batería de iones de litio ha sido cambiada y mejorada; entre otras cosas, John Goodenough ha reemplazado el óxido de cobalto por fosfato de hierro, lo que hace que la batería sea más ecológica.
Como casi todo lo demás, la producción de baterías de iones de litio tiene un impacto en el medio ambiente, pero también existen enormes beneficios medioambientales. La batería ha permitido el desarrollo de tecnologías energéticas más limpias y de vehículos eléctricos, contribuyendo así a reducir las emisiones de gases de efecto invernadero y de partículas.
A través de su trabajo, John Goodenough, Stanley Whittingham y Akira Yoshino han creado las condiciones adecuadas para una sociedad inalámbrica y libre de combustibles fósiles, y así han traído el mayor beneficio a la humanidad.
Articulo original: Popular information. NobelPrize.org. Nobel Media AB 2019. Thu. 10 Oct 2019. https://www.nobelprize.org/prizes/chemistry/2019/popular-information/. Traducido y adaptado por quimicafacil.net