Las Leyes de los Gases Explicadas Paso a Paso
Estimated reading time: 4 minutos
Desde el aire que infla los neumáticos de tu coche hasta el vapor que hace pitar una olla a presión, los gases están en todas partes. Aunque a simple vista parezcan caóticos e invisibles, su comportamiento está regido por reglas matemáticas sorprendentemente elegantes y precisas.
En química y física termodinámica, para entender a un gas solo necesitas dominar tres variables fundamentales: Presión (P), Volumen (V) y Temperatura (T). Cuando cambias una de ellas, las otras reaccionan en consecuencia.
Para hacer este tema mucho más fácil de digerir, hemos preparado esta guía visual dividida en tres módulos. ¡Prepárate para dominar el estado gaseoso!
1. Las Tres Leyes Fundamentales: Relaciones Directas e Inversas
Antes de meternos con fórmulas complejas, debemos entender cómo interactúan las variables de dos en dos, manteniendo una tercera «congelada» (constante). Estas son las reglas clásicas que rigen el día a día.
- Ley de Boyle (Temperatura Constante): Imagina que aprietas un globo con las manos. Al reducir el espacio (Volumen), el gas choca más veces contra las paredes, aumentando la fuerza (Presión). Son inversamente proporcionales: si una sube, la otra baja.
- Fórmula: P1V1=P2V2
- Ley de Charles (Presión Constante): Si dejas un balón al sol, el calor hace que las partículas se muevan más rápido y se alejen entre sí. A más Temperatura, mayor Volumen. Son directamente proporcionales.
- Fórmula: T1V1=T2V2
- Ley de Gay-Lussac (Volumen Constante): Piensa en una lata de aerosol cerrada. Si la calientas (aumentas T), el gas no puede expandirse porque el recipiente es rígido (Volumen fijo), por lo que la Presión se dispara.
- Fórmula: T1P1=T2P2
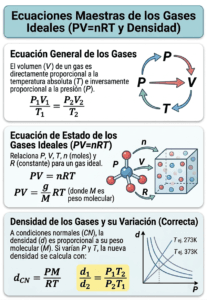
2. La Ecuación Maestra: El Gas Ideal
En el mundo real, rara vez cambia solo una cosa a la vez. ¿Qué pasa si cambian la presión, el volumen y la temperatura simultáneamente? Aquí es donde la ciencia une todas las piezas del rompecabezas.
Al combinar las tres leyes anteriores, obtenemos la Ley Combinada de los Gases. Pero los científicos fueron un paso más allá para crear una ecuación que lo describe todo en un momento exacto: la Ecuación de Estado de los Gases Ideales.
- La Fórmula Rey: PV=nRT
- ¿Qué significa? La Presión por el Volumen es igual al número de moles (n) por la Constante universal de los gases (R) por la Temperatura absoluta.
Esta ecuación es tan poderosa que, si la reescribimos un poco, nos permite calcular incluso la densidad (d) de un gas invisible o descubrir cuál es su peso molecular. ¡Es la herramienta definitiva en el laboratorio!
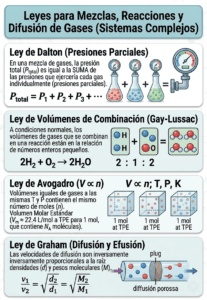
3. Comportamiento en Grupo: Mezclas, Reacciones y Difusión
Hasta ahora hemos hablado de un solo gas aislado. Pero la atmósfera que respiramos es una mezcla de nitrógeno, oxígeno y otros gases. ¿Cómo se comportan cuando están todos juntos o cuando tienen que moverse a través de un espacio?
- Ley de Dalton (Presiones Parciales): Dalton descubrió que los gases son «educados». En una mezcla, cada gas ejerce su propia presión como si estuviera solo. La presión total del recipiente es simplemente la suma matemática de todas esas presiones individuales.
- Ley de Avogadro: Una de las deducciones más brillantes de la química. Establece que si tienes dos cajas del mismo tamaño, a la misma temperatura y presión, ambas tendrán exactamente la misma cantidad de moléculas adentro, sin importar si una está llena de hidrógeno ligero y la otra de radón pesado.
- Ley de Graham (Difusión): ¿Por qué hueles el perfume de alguien al otro lado de la habitación? Por la difusión. Graham demostró que los gases más «ligeros» (menor densidad o peso molecular) viajan mucho más rápido que los gases «pesados».