Ácidos carboranos
Tiempo de lectura estimado: 11 minutos
Entre los llamados superácidos unos de los más fuertes son los llamados ácidos carboranos
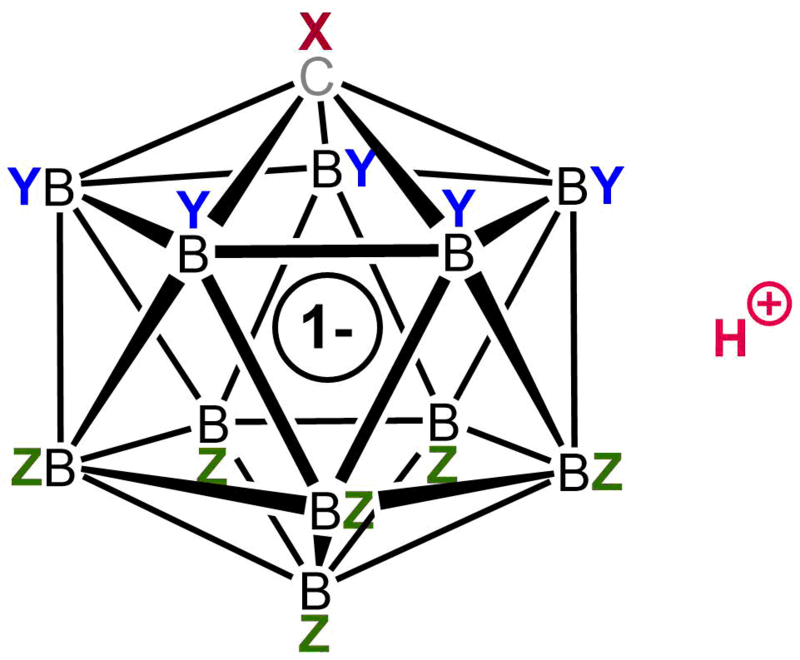
Los ácidos carboranos H(CXB11Y5Z6) (X, Y, Z = H, Alk, F, Cl, Br, CF3) son una clase de superácidos, algunos de los cuales se estima que son al menos un millón de veces más fuertes que el ácido sulfúrico 100% en términos de sus valores de función de acidez de Hammett (H0 ≤ -18) y poseen valores pKa calculados muy por debajo de -20, estableciéndolos como algunos de los ácidos Brønsted más fuertes conocidos.
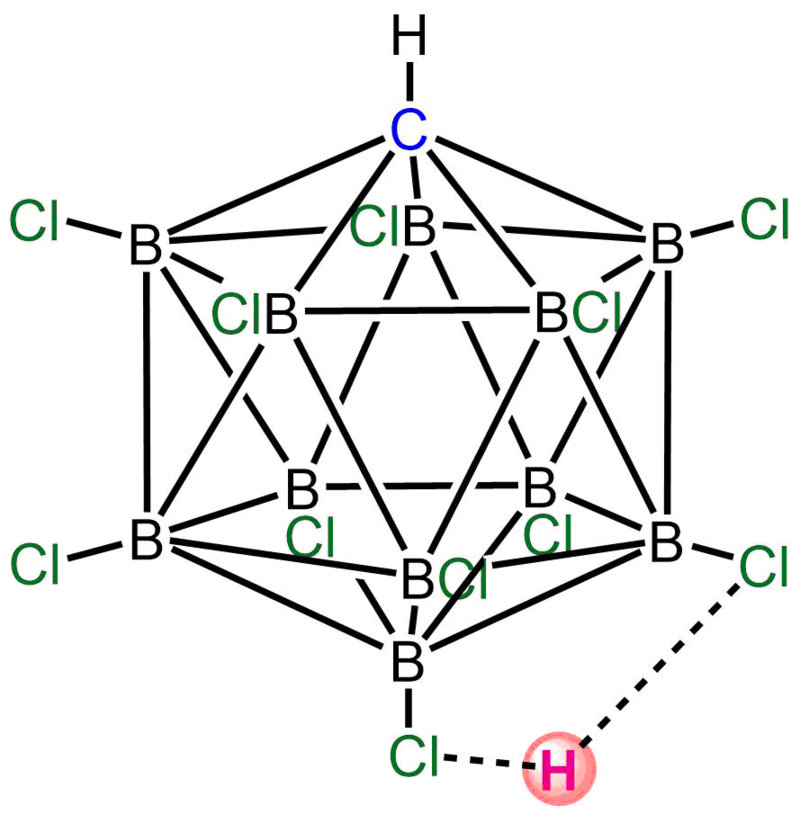
![Modelo de bolas y palos de [CHB11Cl11]-. (No se muestra el protón ácido). hidrógeno - blanco, cloro - verde, boro - rosa, carbono - negro.](https://wp.quimicafacil.net/wp-content/uploads/2020/04/Acidos-carboranos-1.png)
El ejemplo más estudiado es el derivado altamente clorado H(CHB11Cl11). Se descubrió que la acidez del H(CHB11Cl11) superaba ampliamente la del ácido triflico, CF3SO3H, y la bistriflimida, (CF3SO2)2NH, compuestos considerados anteriormente como los ácidos aislables más fuertes.
Su elevada acidez proviene de la extensa deslocalización de sus bases conjugadas, los aniones carboranato (CXB11Y5Z6–), que normalmente se estabilizan aún más por grupos electronegativos como el Cl, el F y el CF3. Debido a la falta de propiedades oxidantes y a la excepcionalmente baja nucleofilia y alta estabilidad de sus bases conjugadas, son los únicos superácidos conocidos que protonan el C60 fullereno sin descomponerlo. Además, forman sales estables y aislables con benceno protonado, C6H7+, el compuesto matriz de los intermediarios de Wheland que se encuentran en las reacciones de sustitución aromática electrofílica.
El ácido carborano fluorado, H(CHB11F11), es incluso más fuerte que el ácido carborano clorado. Es capaz de protonar el butano para formar un catión terc-butil a temperatura ambiente y es el único ácido conocido para protonar el dióxido de carbono para dar el catión puente, [H(CO2)2]+, lo que lo convierte posiblemente en el ácido más fuerte conocido. En particular, el CO2 no sufre una protonación observable cuando se trata con los superácidos mezclados HF-SbF5 o HSO3F-SbF5.
Comparación con otros superácidos
Como clase, los ácidos carboranos forman el grupo más ácido de las sustancias aislables bien definidas conocidas, mucho más ácido que los ácidos fuertes de un solo componente conocidos anteriormente, como el ácido triflico o el ácido perclórico.
En ciertos casos, como los derivados casi perhalogenados mencionados anteriormente, sus acideces rivalizan (y posiblemente superan) las de los superácidos tradicionales mezclados Lewis-Brønsted como el ácido mágico y el ácido fluoroantimónico. (Sin embargo, hasta ahora no ha sido posible una comparación cara a cara, debido a la falta de una medida de la acidez que sea adecuada para ambas clases de ácidos: los valores pKa están mal definidos para los ácidos mixtos químicamente complejos, mientras que los valores H0 no pueden medirse para los ácidos carboranos de fusión muy alta).
Acidez
La fuerza de un ácido Brønsted-Lowry corresponde a su capacidad de liberar un ion de hidrógeno. Una medida común de la fuerza del ácido para medios líquidos concentrados y superácidos es la función de acidez de Hammett, H0.
Basándose en su capacidad de protonar cuantitativamente el benceno, se estimó conservadoramente que el ácido carborano clorado H(CHB11Cl11) tenía un valor H0 igual o inferior a -18, lo que llevó a la afirmación común de que los ácidos carboranos son al menos un millón de veces más fuertes que el ácido sulfúrico 100% (H0 = -12).
Sin embargo, dado que el valor H0 mide la capacidad de protonación de un medio líquido, la naturaleza cristalina y de alta fusión de estos ácidos impide la medición directa de este parámetro.
En términos de pKa, una medida ligeramente diferente de la acidez definida como la capacidad de un determinado soluto para someterse a la ionización en un disolvente, se estima que los ácidos carboranos tienen valores pKa inferiores a -20, incluso sin sustitutos de retirada de electrones en los átomos de boro (por ejemplo, H(CHB11H11) se estima que tiene una pKa de -24), con el análogo H(CFB11F11) totalmente fluorado (aún desconocido) teniendo una pKa calculada de -46. Se espera que el ácido conocido H(CHB11F11) con un flúor menos sea sólo ligeramente más débil (pKa < -40).
En la fase gaseosa, el H(CHB11F11) tiene una acidez calculada de 216 kcal/mol, en comparación con una acidez determinada experimentalmente de 241 kcal/mol (en razonable acuerdo con el valor calculado de 230 kcal/mol) para el H(CHB11Cl11). En cambio, HSbF6 (un modelo simplificado para la especie donante de protones en el ácido fluoroantimónico) tiene una acidez calculada en fase gaseosa de 255 kcal/mol, mientras que el anterior titular del registro determinado experimentalmente era (C4F9SO2)2NH, un congénere de la bistriflimida, a 291 kcal/mol.
Así pues, el H(CHB11F11) es probablemente la sustancia más ácida sintetizada hasta ahora en grandes cantidades, en términos de su acidez en fase gaseosa. En vista de su singular reactividad, también es un fuerte competidor por ser la sustancia más ácida en la fase de condensación. Se han previsto algunos derivados aún más fuertemente ácidos, con una acidez en fase gaseosa < 200 kcal/mol.
Peculiaridad de los carboranos
Los ácidos carboranos se diferencian de los superácidos clásicos por ser sustancias de un solo componente bien definidas. Por el contrario, los superácidos clásicos suelen ser mezclas de un ácido Brønsted y un ácido Lewis (por ejemplo, HF/SbF5). A pesar de ser el ácido más fuerte, los ácidos carboranos a base de boro se describen como «suaves», que protonan limpiamente sustancias básicas débiles sin más reacciones secundarias.
Mientras que los superácidos convencionales descomponen los fullerenos debido a su componente ácido de Lewis fuertemente oxidante, el ácido carborano tiene la capacidad de protonar los fullerenos a temperatura ambiente para producir una sal aislable. Además, el anión que se forma como resultado de la transferencia de protones es casi completamente inerte. Esta propiedad es la que hace que los ácidos carboranos sean las únicas sustancias comparables en acidez a los superácidos mezclados que también pueden ser almacenados en una botella de vidrio, ya que no están presentes o se generan varias especies donantes de flúor (que atacan al vidrio).
Historia
El ácido carborano fue descubierto y sintetizado por primera vez por el profesor Christopher Reed y sus colegas en 2004 en la Universidad de California, Riverside. Antes del descubrimiento del ácido carborano, el antiguo registro de «los ácidos más fuertes como compuestos aislados simples» estaba en manos de los dos superácidos, el ácido fluorosulfónico y el ácido trifluorometanosulfónico, con pKa de -14 y -16 respectivamente. La molécula madre de la que se deriva el ácido carborano, un anión icosaédrico carboranato, HCB11H11–, fue sintetizada por primera vez en DuPont en 1967 por Walter Knoth.
La investigación de las propiedades de esta molécula se puso en pausa hasta mediados de los años 80, cuando el grupo checo de científicos del boro, Plešek, ÿtíbr, y Heřmánek mejoraron el proceso de halogenación de las moléculas de carborano. Estos hallazgos fueron decisivos para desarrollar el procedimiento actual para la síntesis de ácido carborano. El proceso consiste en tratar Cs+[HCB11H11]– con SO2Cl2, refluyendo bajo argón seco para clorar completamente la molécula que produce el ácido carborano, pero se ha demostrado que sólo se clora completamente bajo condiciones selectas.
Síntesis de ácidos carboranos
En 2010, Reed publicó una guía que ofrece procedimientos detallados para la síntesis de los ácidos carboranos y sus derivados. Sin embargo, la síntesis de los ácidos carboranos sigue siendo larga y difícil y requiere una guantera bien mantenida y algún equipo especializado.
![Síntesis de ácido carborano de Cs+[HCB11H11]- hasta Cs+[HCB11Cl11]-.](https://wp.quimicafacil.net/wp-content/uploads/2020/04/Acidos-carboranos-4.png)
El material de partida es el decaborano(14), una sustancia altamente tóxica disponible en el mercado. El ácido carborano H(CHB11Cl11) más estudiado se prepara en 13 pasos. Los últimos pasos son especialmente sensibles y requieren una guantera a < 1 ppm de H2O sin ningún tipo de vapores de disolvente débilmente básicos, ya que bases tan débiles como el benceno o el diclorometano reaccionarán con los electrofilos a base de carborano y los ácidos Brønsted. El paso final de la síntesis es la metátesis de la sal de carboranato de hidridodisilicio-μ con exceso de líquido, cloruro de hidrógeno anhidro, presumiblemente impulsado por la formación de fuertes enlaces Si-Cl y H-H en los subproductos volátiles:
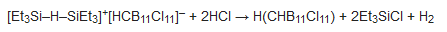
El producto fue aislado por evaporación de los subproductos y se caracterizó por sus espectros de infrarrojos (νCH = 3023 cm-1) y de resonancia magnética nuclear (δ 4,55 (s, 1H, CH), 20,4 (s, 1H, H+) en SO2 líquido) (obsérvese el desplazamiento químico extremadamente descendente del protón ácido).
Aunque las reacciones utilizadas en la síntesis son análogas, la obtención de una muestra pura del H(CHB11F11) más ácido resultó ser aún más difícil, ya que requirió procedimientos extremadamente rigurosos para excluir los rastros de impurezas débilmente básicas.
Estructura
El ácido carbónico está formado por 11 átomos de boro; cada átomo de boro está unido a un átomo de cloro. Los átomos de cloro sirven para aumentar la acidez y actúan como escudos contra los ataques del exterior debido al obstáculo estérico que forman alrededor del cúmulo. El cúmulo, que consiste en los 11 boros, 11 cloros, y un solo átomo de carbono, está emparejado con un átomo de hidrógeno, unido al átomo de carbono. Los átomos de boro y carbono pueden formar seis enlaces debido a la capacidad del boro de formar enlaces de tres centros y dos electrones.
Aunque la estructura del ácido carborano difiere enormemente de la de los ácidos convencionales, ambos distribuyen la carga y la estabilidad de manera similar. El anión carboranato distribuye su carga deslocalizando los electrones a través de los 12 átomos de la jaula. Esto se demostró en un estudio de difracción de rayos X de un solo cristal que reveló longitudes de enlace acortadas en la porción heterocíclica del anillo, lo que sugiere una deslocalización electrónica.
El anión clorado carba-closo-dodecaborato HCB11Cl11– es un anión extraordinariamente estable con lo que se ha descrito anteriormente como vértices B-Cl «sustitutivamente inertes».
El descriptor closo indica que la molécula se deriva formalmente (por sustitución de B a C+) de un borano de estequiometría y carga [BnHn]2- (n = 12 para los ácidos carboranos conocidos).
La estructura en forma de jaula formada por los 11 átomos de boro y 1 átomo de carbono permite que los electrones se deslocalicen en gran medida a través de la jaula tridimensional (la estabilización especial del sistema de carborano se ha denominado «aromaticidad-ancha»), y la alta energía necesaria para perturbar la porción de cúmulo de boro de la molécula es lo que da al anión su notable estabilidad.
Debido a que el anión es extremadamente estable, no se comportará como un nucleófilo hacia el sustrato protonado, mientras que el ácido en sí mismo es completamente no oxidante, a diferencia de los componentes ácidos de Lewis de muchos superácidos como el pentafluoruro de antimonio. Por lo tanto, las moléculas sensibles como la C60 pueden protonar sin descomponerse.
Usos potenciales
Hay muchas aplicaciones propuestas para los ácidos carboranos basados en el boro. Por ejemplo, se han propuesto como catalizadores para el craqueo de hidrocarburos y la isomerización de n-alcanos para formar isoalcanos ramificados («isooctano», por ejemplo). Los ácidos carboranos también pueden utilizarse como ácidos Brønsted fuertes y selectivos para la síntesis química fina, en la que puede ser ventajosa la baja nucleofilicidad del contratiro.
En la química orgánica mecanicista pueden utilizarse en el estudio de intermediarios catiónicos reactivos. En la síntesis inorgánica, su inigualable acidez puede permitir el aislamiento de especies exóticas como las sales de xenón protonado.
Para más información Reed, Christopher A. (2010-01-19). «H+, CH3+, and R3Si+Carborane Reagents: When Triflates Fail». Accounts of Chemical Research. 43 (1): 121–128. doi:10.1021/ar900159e