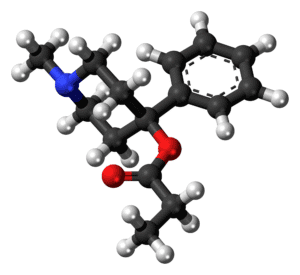
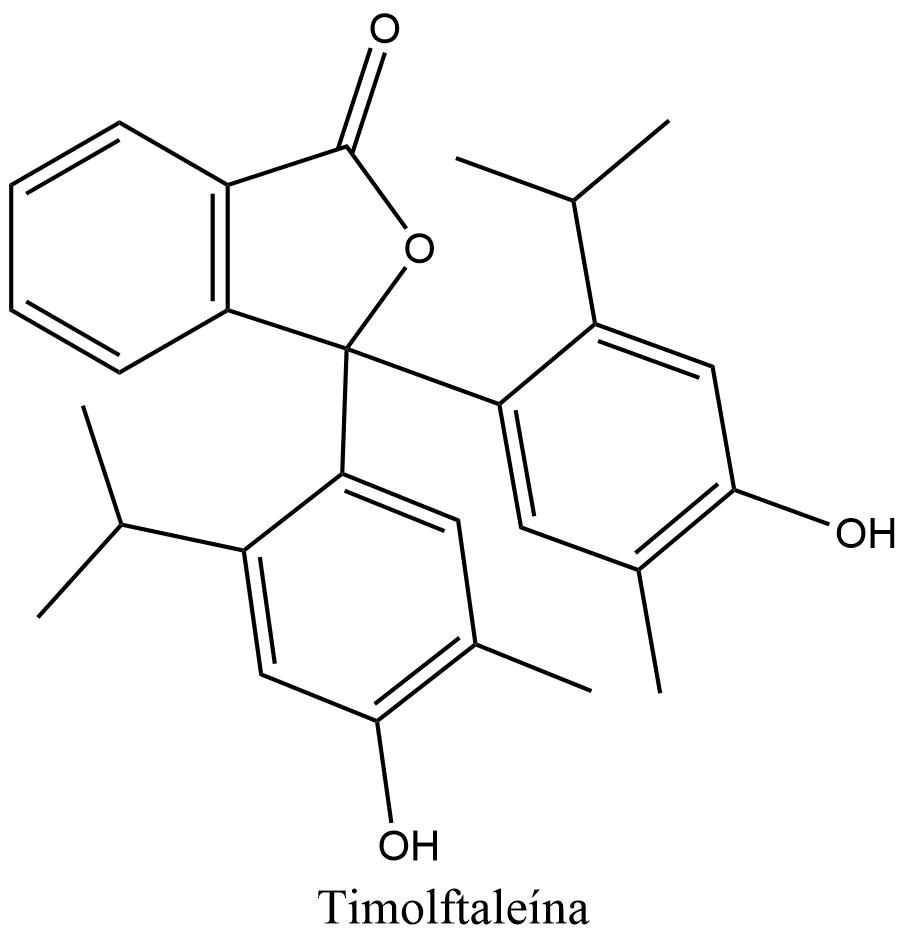
Timolftaleína
Tiempo de lectura estimado: 3 minutos
La timolftaleína es un indicador de pH empleado en la valoración ácido-base que se deriva del anhídrido ftálico y del timol. Su intervalo de transición de pH es aproximadamente entre 9.3 – 10.5, virando de incoloro a azul en dicho rango. Por debajo de pH 9.3 es incoloro, y a valores de pH muy bajos se torna de color rojo intenso.
Usos de la timolftleína
Se presenta normalmente en forma de un polvo blanco que funde entre 248 a 252 °C. A nivel laboratorio, no es de un uso tan frecuente como indicador de pH (siendo ampliamente utilizada para propósitos de valoración ácido-base su homólogo Fenolftaleína).
En soluciones moderadamente ácidas permanece incoloro, pero en presencia de soluciones moderadamente básicas se torna color azul.
En química se utiliza en análisis de laboratorio, investigación, y como indicador de valoraciones ácido-base, siendo su punto de viraje alrededor del rango de pH entre 9.3 a 10.5, realizando la transición cromática de incoloro a azul.
El reactivo se prepara usualmente en soluciones al 1 % p/v en alcohol de 90° y tiene duración indefinida. Hace décadas la Timolftaleína se empleaba como laxante (al igual que la fenolftaleína) y actualmente se suele comercializar como ingrediente para la fabricación de tinta invisible o desvanecedora.
Es de los pocos indicadores ácido base que no presenta color a valores de pH bajos, al igual que lo hacen la Fenolftaleína y el 4-Nitrofenol, respectivamente, lo que los hace especialmente útiles cuando son mezclados entre sí para demostración básica experimental de laboratorio conocida como arcoíris químico.
El coeficiente de extinción molar para el dianión de timolftaleína azul es de 38,000 M−1 cm−1 a 595 nm.
Síntesis de la timolftleína
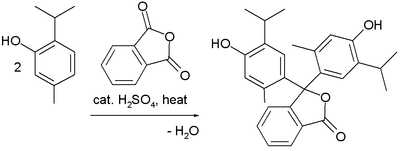
La timolftleína se prepara de acuerdo con la reacción de alquilación de Friedel-Crafts entre timol y anhídrido ftálico con apenas unas gotas de ácido sulfúrico como catalizador, en presencia de calor y con agitación constante, formando un sólido.
Química del viraje de la timolftleína
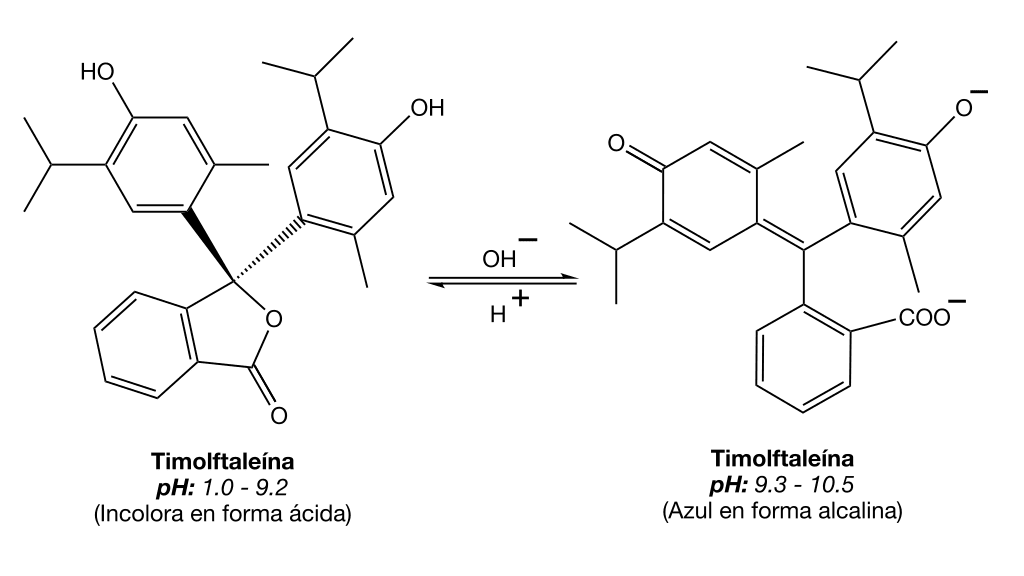

Para más información Thymolphthalein