Tiempo de lectura estimado: 6 minutos
Visión general de las extracciones múltiples
Dependiendo del coeficiente de partición de un compuesto en un disolvente, una sola extracción puede ser todo lo que se necesita para extraer eficazmente un compuesto. Sin embargo, la mayoría de las veces un procedimiento requiere que se extraiga una solución varias veces para aislar un compuesto deseado, ya que este método es más eficiente que una sola extracción (véase el artículo de la revista en la Figura 1b para ver un ejemplo de cómo se utiliza este proceso).

En un procedimiento de extracción múltiple, se utiliza una cantidad de disolvente para extraer una capa (a menudo la capa acuosa) varias veces seguidas. La extracción se repite dos o tres veces, o quizás más si el compuesto tiene un bajo coeficiente de partición en el disolvente orgánico. La figura 2 muestra un diagrama de una solución acuosa que se extrae dos veces con éter dietílico. El éter dietílico tiene una densidad inferior a 1g/mL, por lo que es la capa orgánica superior del embudo.

En una extracción múltiple de una capa acuosa, el procedimiento de la primera extracción es idéntico al de una extracción simple. En la segunda extracción, la capa acuosa de la primera extracción se devuelve al embudo de separación (Figura 2b), con el objetivo de extraer más compuestos. Dado que la capa orgánica de la primera extracción ya ha alcanzado el equilibrio con la capa acuosa, de poco serviría devolverla al embudo de separación y exponerla de nuevo a la capa acuosa. En su lugar, se añade éter dietílico fresco a la capa acuosa, ya que tiene el potencial de extraer más compuestos.
El proceso suele repetirse con una tercera extracción (no mostrada en la figura 2), en la que la capa acuosa de la segunda extracción se devuelve al embudo de separación, seguida de otra porción de disolvente orgánico fresco. En las extracciones múltiples, las capas orgánicas se combinan entre sí, ya que el objetivo es extraer el compuesto en el disolvente orgánico.
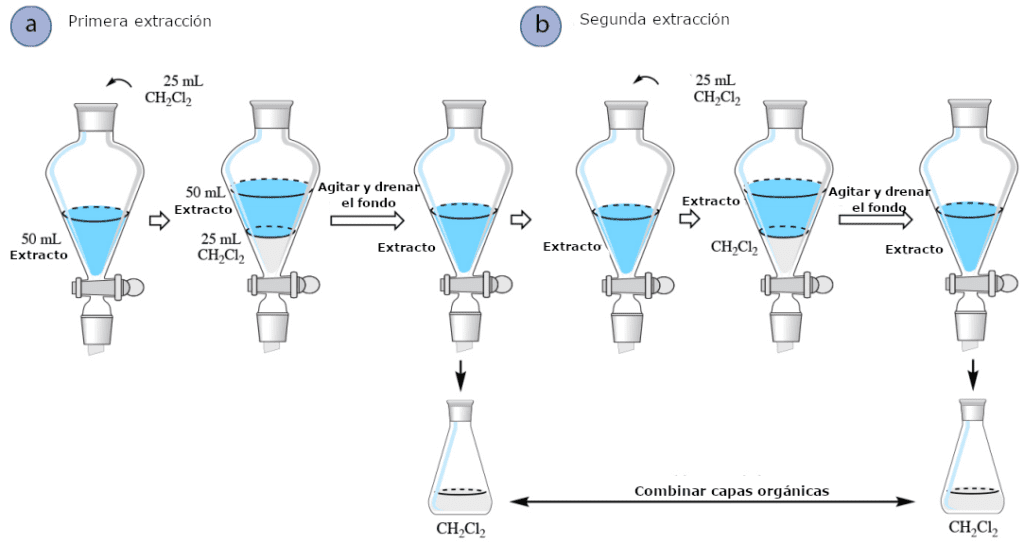
Cuando se extrae una solución acuosa con un disolvente orgánico más denso que el agua (por ejemplo, diclorometano, CH2Cl2), la única diferencia de procedimiento es que no es necesario drenar nunca la capa acuosa del embudo de separación. Después de drenar la capa orgánica de la primera extracción, se puede añadir disolvente fresco a la capa acuosa que queda en el embudo para comenzar la segunda extracción (Figura 3b).
Cuantificación en extracción múltiple
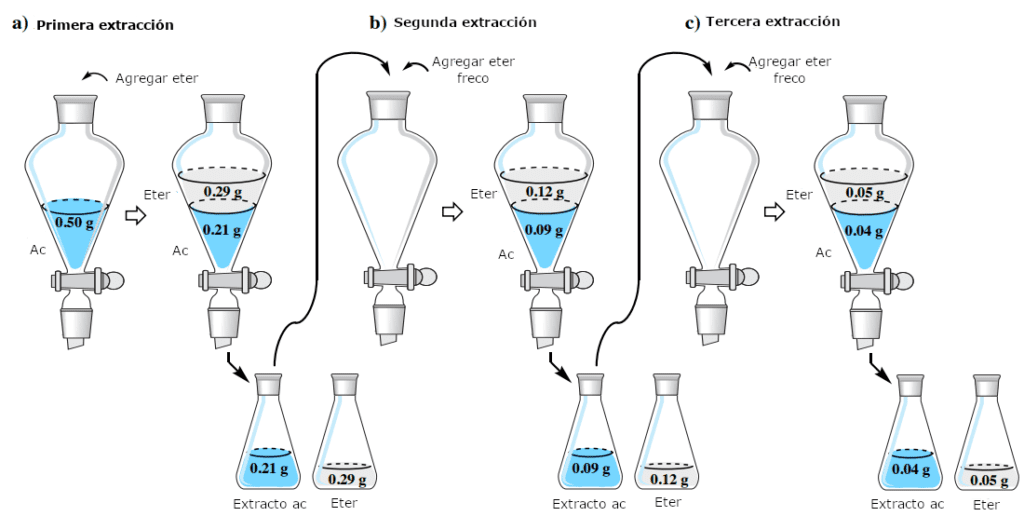
Para demostrar la eficacia de una extracción múltiple, volvamos al problema de la sección de extracción simple, donde una solución de 0,50 g de hiosciamina en 150 mL de agua debe extraerse en éter dietílico. En lugar de utilizar una porción de 150 mL, dividamos el disolvente en tres porciones de 50mL de éter dietílico. ¿Qué cantidad de hiosciamina se extraería con este método?
En la sección anterior, se utilizaron los datos de solubilidad para estimar el coeficiente de partición K y se encontró que era de 4,07. Como antes, podemos asignar a la cantidad de hiosciamina extraída en el éter dietílico el valor «x», lo que dejaría «0,50 g – x» restantes en la capa acuosa de la primera extracción. Utilizando K, el cálculo es idéntico al anterior, diferenciándose únicamente en el menor volumen de la capa orgánica (50 mL en lugar de 150 mL).
Tras resolver el álgebra, x=0,29 g. Este resultado significa que en la primera extracción se extraen 0,29g en el éter dietílico y que quedan 0,21 g en la capa acuosa (0,50 g-0,29 g). Como la capa acuosa se devuelve al embudo de separación, los 0,21 g restantes son la cantidad que debe extraerse de nuevo, lo que altera el cálculo para la segunda extracción sustituyendo el valor de 0,50 g.
Tras resolver el álgebra, x=0,12 g. Este resultado significa que 0,12 g se extraen en el éter dietílico en la segunda extracción y 0,09 g permanecen en la capa acuosa (0,21 g – 0,12 g). El cálculo para la tercera extracción es el siguiente:
Tras resolver el álgebra, x=0,05 g. Este resultado significa que quedan 0,04g en la capa acuosa (0,09 g – 0,05 g) después de la tercera extracción. Los resultados de los cálculos de esta sección se resumen en la Figura 4.
Figura 4: Extracciones múltiples de hiosciamina (K∼4) del agua en éter dietílico.
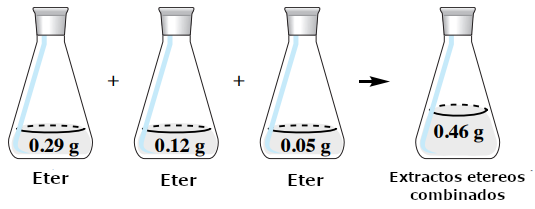
Si se combinan los extractos de éter dietílico de 50mL en este ejemplo (Figura 5), habría un total de 0.46 g de hiosciamina en los extractos orgánicos combinados. De los 0,50 g de hiosciamina en la capa acuosa original, el 92 % del material se extrae en la capa orgánica (100% × 0,46 g/0,50 g). Esta es una cantidad mayor que la obtenida utilizando una sola extracción de 150mL de éter dietílico, que dio como resultado sólo 0,40 g de hiosciamina extraída (80 %).
Estos cálculos demuestran que el uso de múltiples porciones de un disolvente maximiza el poder de extracción de este. En general, tres extracciones son el compromiso óptimo entre el esfuerzo gastado y la maximización de la recuperación de material.
Para más información Extraction Theory
Como citar este artículo:
APA: (). Extracciones múltiples. Recuperado de https://quimicafacil.net/tecnicas-de-laboratorio/extracciones-multiples/
ACS: . Extracciones múltiples. https://quimicafacil.net/tecnicas-de-laboratorio/extracciones-multiples/. Fecha de consulta 2026-04-06.
IEEE: , "Extracciones múltiples," https://quimicafacil.net/tecnicas-de-laboratorio/extracciones-multiples/, fecha de consulta 2026-04-06.
Vancouver: . Extracciones múltiples. [Internet]. [citado 2026-04-06]. Disponible en: https://quimicafacil.net/tecnicas-de-laboratorio/extracciones-multiples/.
MLA: . "Extracciones múltiples." https://quimicafacil.net/tecnicas-de-laboratorio/extracciones-multiples/. . Web.
Si tiene alguna pregunta o sugerencia, escribe a administracion@quimicafacil.net, o visita Como citar quimicafacil.net