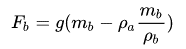Tiempo de lectura estimado: 7 minutos
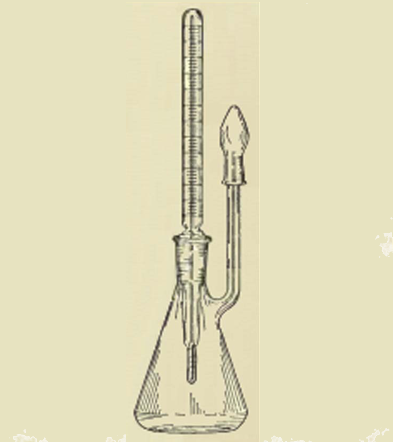
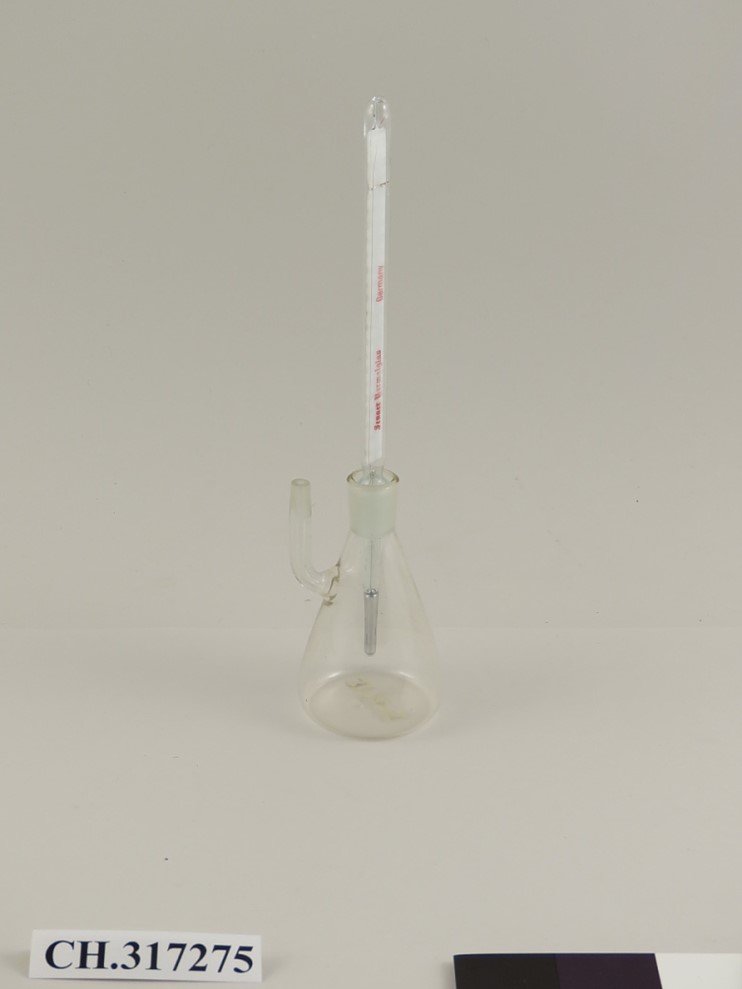
Un picnómetro (del griego: πυκνός (puknos) que significa «denso»), también llamado botella de gravedad específica, es un dispositivo utilizado para determinar la densidad de un líquido. Un picnómetro suele ser de vidrio, con un tapón de vidrio esmerilado ajustado con un tubo capilar que lo atraviesa, para que las burbujas de aire puedan salir del aparato. Este dispositivo permite medir con precisión la densidad de un líquido por referencia a un fluido de trabajo apropiado, como el agua o el mercurio, utilizando una balanza analítica.
Un poco de la historia del picnómetro
Un picnómetro (a veces denominado frasco de gravedad específica de Geissler) es un frasco de vidrio que en alguna de sus variantes tiene un termómetro preciso y delicado, que determina la densidad de un líquido y su variación con la temperatura. Fue ideado en 1859 por el vidriero alemán Heinrich Geissler (1814-1879) y el químico ruso Dmitri Ivanovich Mendeleev (1834-1907).
Uso del picnómetro
Para determinar la densidad de un líquido empleando el picnómetro se debe utilizar un líquido de referencia y tener en cuenta la temperatura. Si el matraz se pesa vacío, lleno de agua y lleno de un líquido cuya densidad relativa se desea, se puede calcular fácilmente la densidad relativa del líquido.
La densidad de las partículas de un polvo, al que no se puede aplicar el método habitual de pesaje, también se puede determinar con un picnómetro. El polvo se añade al picnómetro, que se pesa a continuación, dando el peso de la muestra de polvo. A continuación, se llena el picnómetro con un líquido de densidad conocida, en el que el polvo es completamente insoluble. El peso del líquido desplazado puede entonces determinarse y, por tanto, la densidad relativa del polvo.
Teoría detrás de la medición del volumen
Cuando un picnómetro se llena hasta un volumen específico, pero no necesariamente conocido con exactitud, V y se coloca sobre una balanza, ejercerá una fuerza
donde mb es la masa de la botella y g la aceleración gravitatoria en el lugar en el que se realizan las mediciones. ρa es la densidad del aire a la presión ambiente y ρb es la densidad del material del que está hecha la botella (normalmente vidrio), de modo que el segundo término es la masa de aire desplazada por el vidrio de la botella cuyo peso, por el Principio de Arquímedes, debe restarse. La botella está, por supuesto, llena de aire, pero como ese aire desplaza una cantidad igual de aire, el peso de ese aire se cancela por el peso del aire desplazado. Ahora llenamos la botella con el fluido de referencia, por ejemplo, agua pura. La fuerza ejercida sobre el platillo de la balanza pasa a ser:
Si a esto le restamos la fuerza medida en la botella vacía (o taramos la balanza antes de hacer la medición del agua) obtenemos.
donde el subíndice n indica que esta fuerza es neta de la fuerza de la botella vacía. Ahora se vacía la botella, se seca bien y se vuelve a llenar con la muestra. La fuerza, neta de la botella vacía, es ahora:
donde ρs es la densidad de la muestra. La relación entre las fuerzas de la muestra y del agua es:
Esto se llama Densidad Relativa Aparente, denotada por el subíndice A, porque es lo que obtendríamos si tomáramos la relación de las pesadas netas en aire de una balanza analítica o utilizáramos un hidrómetro (el vástago desplaza el aire). Nótese que el resultado no depende de la calibración de la balanza. El único requisito que se le exige es que su lectura sea lineal con la fuerza. La RDA tampoco depende del volumen real del picnómetro.
Una nueva manipulación y, finalmente, la sustitución de RDV, la verdadera densidad relativa (se utiliza el subíndice V porque a menudo se denomina densidad relativa en el vacío), por ρs/ρw da la relación entre la densidad relativa aparente y la verdadera.
Dado que la densidad del aire seco a 101,325 kPa a 20 °C es 0,001205 g/cm3 y la del agua es 0,998203 g/cm3, vemos que la diferencia entre las densidades relativas verdadera y aparente para una sustancia con una densidad relativa (20 °C/20 °C) de aproximadamente 1,100 sería de 0,000120. Cuando la densidad relativa de la muestra se aproxima a la del agua (por ejemplo, soluciones diluidas de etanol) la corrección es aún menor.
El picnómetro se utiliza en la norma ISO ISO 1183-1:2004, ISO 1014-1985 y la norma ASTM: ASTM D854.
Tipos de picnómetro
- Gay-Lussac, es el picnometro clásico de laboratorio, en forma de pera, con tapón perforado, ajustado, capacidad 1, 2, 5, 10, 25, 50 y 100 mL
- Igual que el Gay-Lussac, con termómetro incorporado, ajustable, tubo lateral con tapa
- Hubbard, para bitumen y aceites crudos pesados, tipo cilíndrico, ASTM D 70, 24 mL
- Hubbard de tipo cónico, ASTM D 115 y D 234, 25 mL



Para más información Things You Should Know About Pycnometer
Como citar este artículo:
APA: (). Picnómetro. Recuperado de https://quimicafacil.net/infografias/material-de-laboratorio/picnometro/
ACS: . Picnómetro. https://quimicafacil.net/infografias/material-de-laboratorio/picnometro/. Fecha de consulta 2026-04-04.
IEEE: , "Picnómetro," https://quimicafacil.net/infografias/material-de-laboratorio/picnometro/, fecha de consulta 2026-04-04.
Vancouver: . Picnómetro. [Internet]. [citado 2026-04-04]. Disponible en: https://quimicafacil.net/infografias/material-de-laboratorio/picnometro/.
MLA: . "Picnómetro." https://quimicafacil.net/infografias/material-de-laboratorio/picnometro/. . Web.
Si tiene alguna pregunta o sugerencia, escribe a administracion@quimicafacil.net, o visita Como citar quimicafacil.net