Estimated reading time: 7 minutos
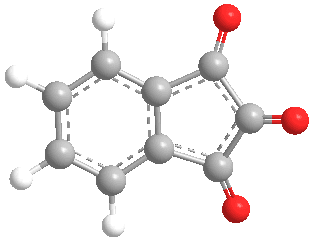
La ninhidrina (2,2-dihidroxiindano-1,3-diona) es un compuesto orgánico con la fórmula C6H4(CO)2C(OH)2. Se utiliza para detectar amoníaco y aminas. Al reaccionar con estas aminas, la ninhidrina se convierte en derivados de color azul intenso o púrpura, conocidos como púrpura de Ruhemann.
La ninhidrina es utilizada principalmente en la detección de huellas dactilares en casos forenses, ya que las aminas terminales de los residuos de lisina en los péptidos y proteínas presentes en las huellas reaccionan con la ninhidrina.
La ninhidrina es un sólido blanco soluble en etanol y acetona. Se puede considerar como la forma hidratada del indano-1,2,3-triona.
Historia
La ninhidrina fue descubierta en 1910 por el químico germano-británico Siegfried Ruhemann (1859–1943). En ese mismo año, Ruhemann observó la reacción de la ninhidrina con los aminoácidos. En 1954, los investigadores suecos Oden y von Hofsten propusieron el uso de la ninhidrina para desarrollar huellas dactilares latentes.
¿Cómo reacciona la ninhidrina con los aminoácidos?
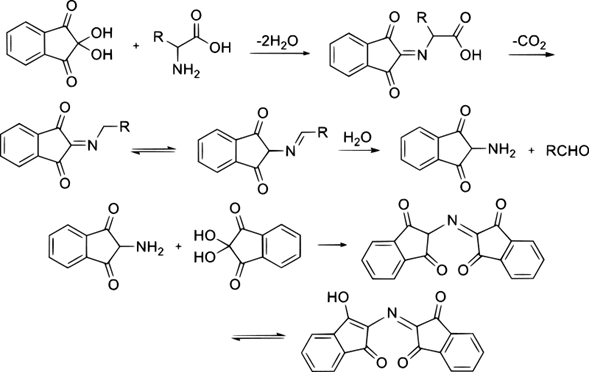
Al examinar en mayor detalle la reacción de la ninhidrina con los aminoácidos alfa, primero la ninhidrina se deshidrata y reacciona con un aminoácido, formando una base de Schiff. Luego, sufre una descarboxilación, liberando dióxido de carbono. Finalmente, al reaccionar con agua, el enlace con la cadena lateral (grupo R) se desprende rápidamente del intermedio imino, formando un aldehído y dicetohidrindamina.
Dado que la dicetohidrindamina es una amina primaria, se condensa nuevamente con la ninhidrina, formando el derivado imino dimérico final, comúnmente llamado púrpura de Ruhemann.
El padre de la ninhidrina
Siegfried Ruhemann fue un químico prácticamente desconocido para la comunidad científica actual. En 1910, a los 51 años, descubrió accidentalmente la ninhidrina mientras era conferenciante de química en la Universidad de Cambridge.
Unos meses después, también observó la reacción de la ninhidrina con amoníaco y aminoácidos, señalando: «Es de especial interés la acción del amoníaco sobre la triketona. Si la solución acuosa de la mezcla de ambas sustancias se deja reposar por un corto tiempo, adquiere un color violeta rojizo intenso».
Sin embargo, sus investigaciones fueron interrumpidas cuando, a raíz del aumento de la histeria anti-alemana en Gran Bretaña durante la Primera Guerra Mundial, se vio obligado a renunciar a su puesto en Cambridge y regresar a Alemania. Allí trabajó en el laboratorio de Emil Fischer durante algunos años y, en 1921, obtuvo un puesto como director de un pequeño instituto de investigación industrial, donde trabajó en la química de la lignita y la turba.
La ninhidrina y el color purpura
A finales del siglo XIX, muchos químicos se dedicaron a investigar y reproducir tintes naturales, especialmente aquellos difíciles de obtener como el púrpura, muy valorado debido a su escasez. Tras el descubrimiento accidental de la mauveína por el químico William Henry Perkin en 1856, numerosos científicos comprendieron la importancia de los tintes sintéticos. Incluso desempeñaron un papel en la política de la época.
En 1878, Adolf von Baeyer sintetizó la indigotina, de color azul, a partir de isatina, y más tarde recibió el Premio Nobel de Química en 1905 por sus trabajos en tintes orgánicos y compuestos hidroaromáticos.
La púrpura de Ruhemann, con una estructura molecular similar a la de la indigotina, podría haber sido un tinte potencialmente viable. Sin embargo, la ninhidrina era tan costosa que resultaba impráctico utilizarla como material de partida para la producción masiva de dicho tinte.
La ninhidrina para revelar huellas
Aunque no es práctico utilizar ninhidrina en la industria de tintes, su reacción de color es extremadamente útil en diversas disciplinas como la bioquímica, la industria alimentaria, la microbiología, la histoquímica y la ciencia de las proteínas.
Además de su aplicación común como reactivo para localizar aminoácidos en cromatogramas, se han desarrollado numerosas técnicas y mejoras para detectar y analizar diversos compuestos químicos, tejidos, alimentos y fármacos.
La ninhidrina también es un reactivo esencial en el campo de la ciencia forense. Lla ninhidrina se ha utilizado ampliamente para visualizar huellas dactilares latentes. En series de televisión como CSI o Silent Witness, los científicos forenses suelen mencionar la ninhidrina cuando buscan huellas dactilares.
En 1913, unos años después del descubrimiento de la ninhidrina, los científicos Emil Abderhalden y H.S. Schmidt comentaron: «El sudor contiene sustancias que dializan y reaccionan con la ninhidrina. El hecho de que el sudor dé una reacción intensa es importante para realizar la prueba. Se debe tener cuidado de no tocar nada que luego entre en contacto con el reactivo». Aunque la reacción de la ninhidrina con el sudor ha sido conocida desde entonces, no fue hasta la década de 1950 que comenzó a emplearse en la ciencia forense.
Las huellas dactilares están compuestas en su mayoría por sudor, que contiene principalmente agua, junto con algunas sales, lípidos y aminoácidos, muchos de los cuales pueden ser utilizados para desarrollar huellas. Por ejemplo, la mayoría de los lípidos pueden teñirse con vapores de yodo, y las sales pueden reaccionar con nitrato de plata para formar haluros de plata fotosensibles; y, por supuesto, la ninhidrina puede reaccionar con los grupos amina de las huellas dactilares.
Aunque existen varios reactivos que cumplen este propósito, la ninhidrina es especialmente útil porque puede desarrollar huellas dactilares latentes en superficies porosas como el papel. En la práctica, la ninhidrina suele disolverse en un disolvente volátil, como acetona o etanol, y se pulveriza sobre una superficie. Tras reaccionar con los grupos amina terminales en los aminoácidos y proteínas presentes en los residuos de las huellas, se forma la púrpura de Ruhemann.
Desde la década de 1980, se han desarrollado muchos análogos de ninhidrina con la misma parte activa de tricetona vicinal cíclica para mejorar el color y la fluorescencia de la púrpura de Ruhemann original. Sin embargo, la ninhidrina sigue siendo el reactivo universal en la ciencia forense debido a que la mayoría de los análogos son demasiado costosos y no están disponibles comercialmente.
Otras aplicaciones
La ninhidrina es un material de partida importante en la síntesis orgánica. Se utiliza en el diseño y la síntesis de diversas estructuras, particularmente en la preparación de compuestos heterocíclicos, algunos de los cuales tienen potencial como agentes anticancerígenos. La ninhidrina también es una herramienta útil en la geocronología, una ciencia que determina la edad de los fósiles.
Cuando la ninhidrina reacciona con el colágeno de los huesos fósiles, se libera gas dióxido de carbono. Dado que la fuente de carbono del dióxido de carbono se obtiene del colágeno, se puede aplicar una técnica de datación radiométrica convencional llamada conteo proporcional de gases para determinar la edad del fósil midiendo las partículas beta del decaimiento del radiocarbono.
Como citar este artículo:
APA: (2025-02-25). Ninhidrina. Recuperado de https://quimicafacil.net/compuesto-de-la-semana/ninhidrina/
ACS: . Ninhidrina. https://quimicafacil.net/compuesto-de-la-semana/ninhidrina/. Fecha de consulta 2026-03-14.
IEEE: , "Ninhidrina," https://quimicafacil.net/compuesto-de-la-semana/ninhidrina/, fecha de consulta 2026-03-14.
Vancouver: . Ninhidrina. [Internet]. 2025-02-25 [citado 2026-03-14]. Disponible en: https://quimicafacil.net/compuesto-de-la-semana/ninhidrina/.
MLA: . "Ninhidrina." https://quimicafacil.net/compuesto-de-la-semana/ninhidrina/. 2025-02-25. Web.
Si tiene alguna pregunta o sugerencia, escribe a administracion@quimicafacil.net, o visita Como citar quimicafacil.net