Estimated reading time: 8 minutos
El linezolid es un antibiótico utilizado para el tratamiento de infecciones causadas por bacterias Gram-positivas resistentes a otros antibióticos. El linezolid es activo contra la mayoría de las bacterias Gram-positivas que causan enfermedades, incluidos los estreptococos, los enterococos resistentes a la vancomicina (VRE) y el Staphylococcus aureus resistente a la meticilina (MRSA). Los principales usos son las infecciones de la piel y la neumonía, aunque puede utilizarse para otras infecciones, como la tuberculosis resistente a los medicamentos.
Cuando se administra durante periodos cortos, el linezolid es un antibiótico relativamente seguro. Puede utilizarse en personas de todas las edades y en personas con enfermedades hepáticas o con una función renal deficiente. Los efectos secundarios más comunes con el uso a corto plazo incluyen dolor de cabeza, diarrea, sarpullido y náuseas.
Los efectos secundarios graves pueden incluir el síndrome de la serotonina, la supresión de la médula ósea y los niveles elevados de lactato en la sangre, en particular cuando se utiliza durante más de dos semanas. Si se utiliza durante períodos más prolongados, puede causar daños en los nervios, incluido el nervio óptico, que pueden ser irreversibles.
Historia del linezolid
Las oxazolidinonas se conocen como inhibidores de la monoaminooxidasa desde finales de los años cincuenta. Sus propiedades antimicrobianas fueron descubiertas por investigadores de E.I. duPont de Nemours en los años 70.
En 1978, DuPont patentó una serie de derivados de la oxazolidinona por su eficacia en el tratamiento de enfermedades bacterianas y fúngicas de las plantas, y en 1984, otra patente describió su utilidad en el tratamiento de infecciones bacterianas en mamíferos. En 1987, los científicos de DuPont presentaron una descripción detallada de las oxazolidinonas como una nueva clase de antibióticos con un nuevo mecanismo de acción.
Pharmacia & Upjohn (ahora parte de Pfizer) inició su propio programa de investigación sobre las oxazolidinonas en la década de 1990. Los estudios de las relaciones estructura-actividad de los compuestos condujeron al desarrollo de varias subclases de derivados de oxazolidinona, con distintos perfiles de seguridad y actividad antimicrobiana. Se consideraron dos compuestos candidatos a fármacos: eperezolid (nombre en clave PNU-100592) y linezolid (PNU-100766).
En las fases preclínicas de desarrollo, eran similares en cuanto a seguridad y actividad antibacteriana, por lo que se llevaron a ensayos clínicos de fase I para identificar cualquier diferencia en la farmacocinética. Se descubrió que el linezolid tenía una ventaja farmacocinética – sólo requería una dosis de dos veces al día, mientras que el eperezolid debía administrarse tres veces al día para lograr una exposición similar- y, por tanto, se procedió a realizar más ensayos.
La Administración de Alimentos y Medicamentos (FDA) de EE.UU. aprobó el linezolid el 18 de abril de 2000. A continuación, se aprobó en Brasil (junio de 2000), el Reino Unido (enero de 2001), Japón y Canadá (abril de 2001), Europa (a lo largo de 2001) y otros países de América Latina y Asia.
En 2009, el linezolid era el único antibiótico de oxazolidinona disponible. Otros miembros de esta clase han entrado en fase de desarrollo, como el posizolid (AZD2563), el ranbezolid (RBx 7644), y el radezolid (RX-1741). En 2014, la FDA aprobó el fosfato de tedizolid, un derivado de la oxazolidinona de segunda generación, para la infección bacteriana aguda de la piel y de las estructuras cutáneas.
Química
A pH fisiológico (7,4), el linezolid existe en estado no cargado. Es moderadamente soluble en agua (aproximadamente 3 mg/mL), con un logP de 0,55.
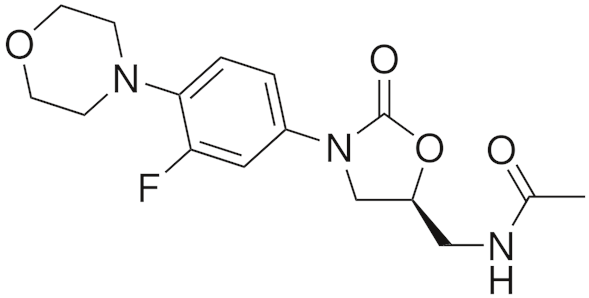
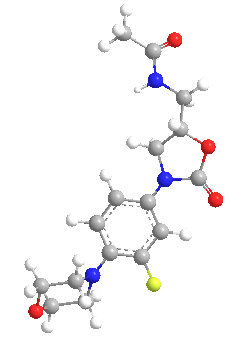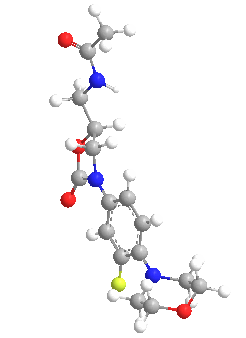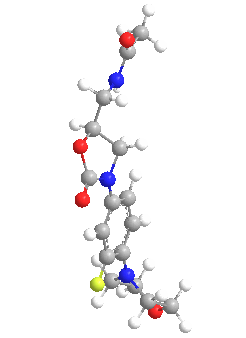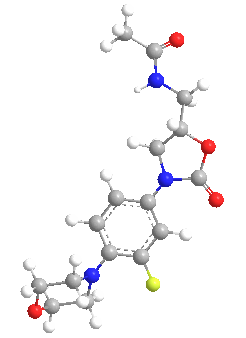
El farmacóforo de la oxazolidinona -la «plantilla» química esencial para la actividad antimicrobiana- consiste en una molécula de 1,3-oxazolidina-2-ona con un grupo arilo en la posición 3 y un grupo S-metilo, con otro sustituyente unido a él, en la posición 5 (los enantiómeros R de todas las oxazolidinonas carecen de propiedades antibióticas).
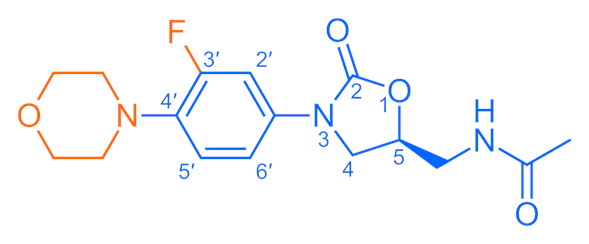
Además de este núcleo esencial, el linezolid también contiene varias características estructurales que mejoran su eficacia y seguridad. Un sustituyente acetamida en el grupo 5-metilo es la mejor opción en términos de eficacia antibacteriana, y se utiliza en todas las oxazolidinonas más activas desarrolladas hasta ahora; de hecho, alejarse demasiado de un grupo acetamida en esta posición hace que el fármaco pierda su poder antimicrobiano, aunque se mantiene una actividad de débil a moderada cuando se utilizan algunos grupos isostéricos.
Un átomo de flúor en la posición 3′ prácticamente duplica la actividad in vitro e in vivo, y el átomo de nitrógeno donador de electrones en el anillo de morfolina ayuda a mantener una alta potencia antibiótica y un perfil de seguridad aceptable.
El anticoagulante rivaroxabán (Xarelto) presenta una sorprendente similitud estructural con el linezolid; ambos fármacos comparten el farmacóforo de la oxazolidinona, diferenciándose únicamente en tres aspectos (una cetona y un clorotiofeno adicionales, y la ausencia del átomo de flúor). Sin embargo, esta similitud no parece tener importancia clínica.
Síntesis
El linezolid es un fármaco completamente sintético: no se encuentra en la naturaleza (a diferencia de la eritromicina y muchos otros antibióticos) y no se desarrolló a partir de un esqueleto natural (a diferencia de la mayoría de los betalactámicos, que son semisintéticos).
A pesar de los buenos rendimientos, el método original (desarrollado por Upjohn para la producción a escala de planta piloto de linezolid y eperezolid) es largo, requiere el uso de productos químicos caros -como el paladio sobre carbono y los reactivos altamente sensibles cloruro de metanosulfonilo y n-butilitio- y necesita condiciones de baja temperatura. Gran parte del elevado coste del linezolid se ha atribuido a lo costoso de su síntesis. Una ruta algo más concisa y rentable, más adecuada para la producción a gran escala, fue patentada por Upjohn en 1998.
Entre las síntesis posteriores se encuentran un método «atómico-económico» que parte del D-manitol, desarrollado por la empresa farmacéutica india Dr. Reddy’s y comunicado en 1999, y una ruta que parte del acetónido de (S)-gliceraldehído (preparado a partir del ácido ascórbico), desarrollada por un equipo de investigadores de la Universidad Normal de Hunan en Changsha, Hunan, China.
El 25 de junio de 2008, durante la 12ª Conferencia Anual de Química Verde e Ingeniería en Nueva York, Pfizer informó del desarrollo de su síntesis de «segunda generación» de linezolid: una síntesis convergente y verde a partir de (S)-epiclorhidrina, con un mayor rendimiento y una reducción del 56% de los residuos totales.
Resistencia al linezolid
La resistencia adquirida al linezolid se notificó ya en 1999, en dos pacientes con una infección grave por Enterococcus faecium multirresistente que recibieron el fármaco a través de un programa de uso compasivo. El Staphylococcus aureus resistente al linezolid se aisló por primera vez en 2001.
En Estados Unidos, la resistencia al linezolid se ha monitorizado y rastreado desde 2004 a través de un programa denominado LEADER, que (a partir de 2007) se llevó a cabo en 60 instituciones médicas de todo el país. La resistencia se ha mantenido estable y extremadamente baja: menos de la mitad del uno por ciento de los aislados en general, y menos de una décima parte del uno por ciento de las muestras de S. aureus.
Desde 2002 se ha llevado a cabo un programa mundial similar, el «Estudio de Evaluación Anual de la Potencia y el Espectro de Zyvox», o ZAAPS. En 2007, la resistencia global al linezolid en 23 países era inferior al 0,2%, y no existía entre los estreptococos. Sólo se encontró resistencia en Brasil, China, Irlanda e Italia, entre los estafilococos coagulasa-negativos (0,28% de las muestras resistentes), los enterococos (0,11%) y el S. aureus (0,03%).
En el Reino Unido e Irlanda, no se encontró resistencia en los estafilococos recogidos de casos de bacteriemia entre 2001 y 2006, aunque se ha informado de resistencia en los enterococos. Algunos autores han predicho que la resistencia en E. faecium aumentará si el uso de linezolid continúa en los niveles actuales o aumenta. No obstante, el linezolid sigue siendo un importante agente antimicrobiano con una actividad casi completa (0,05% de resistencia).
Para más información Linezolid