Estimated reading time: 9 minutos
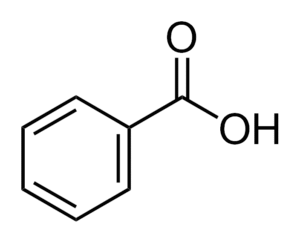
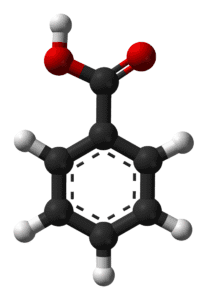
El ácido benzoico, cuya fórmula química es C₇H₆O₂ (o C₆H₅COOH), es el ácido carboxílico aromático más simple. Se presenta como un sólido cristalino, incoloro y con un ligero olor característico. Esta molécula es ampliamente conocida no solo en el ámbito de la química, sino también en la vida cotidiana, principalmente por su uso como conservante alimentario, identificado en Europa con el código E210.
Sin embargo, sus aplicaciones van mucho más allá, abarcando desde la medicina y la cosmética hasta su papel como un intermediario crucial en la síntesis de una vasta gama de productos químicos industriales.
Presente de forma natural en numerosas plantas y resinas, el ácido benzoico y sus sales (los benzoatos) desempeñan un papel fundamental en la protección contra el deterioro microbiano.
Su historia se remonta al siglo XVI, y desde entonces, su estudio y aplicación han evolucionado hasta convertirlo en un compuesto indispensable en múltiples industrias, siendo a la vez un precursor vital para la producción de plásticos, tintes y productos farmacéuticos.
Historia
El descubrimiento del ácido benzoico precede en varios siglos al desarrollo formal de la química orgánica, lo que lo convierte en uno de los compuestos orgánicos conocidos desde hace más tiempo.
Primeras Descripciones
La primera descripción documentada del ácido benzoico data de 1556 y se atribuye al famoso médico, boticario y astrólogo francés Nostradamus. En sus escritos, describió un método para obtener una sustancia sólida mediante la sublimación por calentamiento en seco de la goma de benjuí (gum benzoin).
La goma de benjuí es una resina balsámica obtenida de la corteza de varias especies de árboles del género Styrax, nativos de las regiones tropicales de Asia. Esta resina, conocida por su aroma dulce similar a la vainilla, se ha utilizado durante siglos en perfumería, incienso (especialmente en iglesias ortodoxas) y medicina tradicional. Nostradamus recogía los vapores que se desprendían al calentar la resina y los condensaba para obtener el producto cristalino, que hoy conocemos como ácido benzoico.
Elucidación Estructural y Síntesis
A pesar de su temprano aislamiento, la composición química y la estructura del ácido benzoico permanecieron como un misterio hasta el advenimiento de la química orgánica moderna en el siglo XIX. Fue entonces cuando químicos prominentes de la época, entre ellos el alemán Justus von Liebig, se dedicaron a analizar el compuesto.
A través de sus meticulosos trabajos, determinaron su fórmula empírica y su estructura molecular, estableciendo que consistía en un anillo de benceno unido a un grupo carboxilo (-COOH). Estos estudios fueron fundamentales para comprender la naturaleza de los compuestos aromáticos y sentaron las bases para su futura síntesis en el laboratorio.
Fuentes Naturales y Biosíntesis
El ácido benzoico no es solo un producto de síntesis química; se encuentra abundantemente en la naturaleza como parte del metabolismo de muchas plantas y microorganismos.
Presencia en Alimentos y Plantas
El compuesto y sus sales, los benzoatos, están presentes de forma natural en una gran variedad de alimentos. Las concentraciones más altas se encuentran en bayas, especialmente en arándanos rojos (cranberries), arándanos azules (blueberries) y arándanos negros (bilberries), donde puede alcanzar hasta 1300 mg por kilogramo. También se encuentra en otras frutas como las fresas y en especias y hierbas como el clavo, el tomillo, la canela y el anís estrellado. Además, productos lácteos fermentados como el yogur y algunos quesos pueden contener ácido benzoico como resultado del metabolismo microbiano.
La goma de benjuí sigue siendo una fuente natural importante, de la cual se extrae no solo ácido benzoico, sino también otros compuestos aromáticos conocidos como la vainillina, el cinamaldehído y el ácido cinámico.
Biosíntesis en Plantas
Las plantas sintetizan el ácido benzoico a través de complejas rutas metabólicas como parte de sus mecanismos de defensa contra patógenos. Aunque existen varias vías, una de las principales comienza con el aminoácido esencial fenilalanina. El proceso enzimático implica los siguientes pasos clave:
- La fenilalanina sufre modificaciones en su cadena lateral para formar sucesivamente ácido cinámico y luego ácido 3-hidroxi-3-fenilpropanoico.
- En un paso posterior, la cadena lateral se acorta para producir benzaldehído.
- Finalmente, diferentes enzimas pueden oxidar el benzaldehído para formar ácido benzoico o reducirlo para formar alcohol bencílico.
Dentro de la planta, el ácido benzoico puede ser modificado posteriormente. Por ejemplo, una enzima metiltransferasa puede convertirlo en su éster, el benzoato de metilo. Otra enzima puede catalizar su reacción con el alcohol bencílico para formar el éster benzoato de bencilo. Ambos ésteres, junto con el ácido benzoico, se encuentran en la resina de benjuí.
Síntesis
Aunque se puede extraer de fuentes naturales, la inmensa mayoría del ácido benzoico utilizado hoy en día se produce sintéticamente a escala industrial y en el laboratorio.
Síntesis Industrial
El método industrial predominante es la oxidación catalítica en fase gaseosa del tolueno con oxígeno atmosférico. Este proceso es económicamente muy favorable debido al bajo costo del tolueno. La reacción se lleva a cabo utilizando catalizadores basados en metales de transición, como naftenatos de cobalto (II) o manganeso (IV).
Síntesis en el Laboratorio
En un entorno de laboratorio, un método clásico y pedagógicamente importante es a través de un reactivo de Grignard. El proceso comienza con bromobenceno, que se hace reaccionar con virutas de magnesio en éter anhidro para formar bromuro de fenilmagnesio.
Este reactivo de Grignard se vierte luego sobre hielo seco (dióxido de carbono sólido). El carbono nucleofílico del reactivo de Grignard ataca al carbono electrofílico del CO₂, formando una sal de carboxilato de magnesio. Finalmente, la adición de un ácido acuoso (acidificación) protona el anión carboxilato para producir ácido benzoico.
Otro método de laboratorio consiste en la oxidación del fenilacetileno utilizando ozono y ácido trifluoroacético.
Estructura y Propiedades
El ácido benzoico es un sólido cristalino que presenta varias propiedades físicas y estructurales notables.
- Solubilidad y Cristalización: Es poco soluble en agua fría pero considerablemente más soluble en agua caliente. Esta diferencia de solubilidad lo hace ideal para ser purificado mediante recristalización, un procedimiento común en los laboratorios de química orgánica. Al disolver el ácido impuro en agua caliente y luego enfriar la solución lentamente, se forman cristales puros de ácido benzoico.
- Punto de Fusión: Tiene un punto de fusión bien definido y reproducible de 122 °C, lo que lo convierte en un estándar comúnmente utilizado para la calibración de aparatos de punto de fusión.
- Estructura Dímérica: En estado sólido y también en fase gaseosa o en disolventes no polares, el ácido benzoico no existe como moléculas individuales, sino que forma dímeros. Dos moléculas de ácido benzoico se asocian a través de dos puentes de hidrógeno entre sus grupos carboxilo. Esta estructura dímérica es energéticamente muy estable y explica su punto de ebullición relativamente alto en comparación con otras moléculas de peso similar.
Usos y Aplicaciones
El ácido benzoico es un compuesto versátil con un amplio espectro de aplicaciones.
Conservante Alimentario
El uso más extendido del ácido benzoico es como conservante de alimentos. Se le asigna el código E210. Sin embargo, debido a su baja solubilidad en agua, se utilizan más comúnmente sus sales, que son mucho más solubles:
- Benzoato de sodio (E211)
- Benzoato de potasio (E212)
- Benzoato de calcio (E213)
Su acción conservante es más efectiva en condiciones ácidas (pH < 4.5), ya que es la forma no disociada del ácido la que posee la actividad antimicrobiana. Se cree que el ácido benzoico interfiere con la integridad de las membranas celulares de los microorganismos, inhibiendo su crecimiento y previniendo la proliferación de levaduras, mohos y algunas bacterias. Se utiliza en bebidas carbonatadas, zumos de frutas, encurtidos, mermeladas y salsas.
Aplicaciones Médicas y Farmacéuticas
Las propiedades antifúngicas del ácido benzoico se conocen desde hace más de un siglo. Su aplicación más famosa en dermatología es el Ungüento de Whitfield, desarrollado por el dermatólogo británico Arthur Whitfield hace casi 120 años. Esta pomada, que contiene una mezcla de 6% de ácido benzoico y 3% de ácido salicílico en una base de vaselina o lanolina, sigue siendo un tratamiento eficaz y de bajo costo para infecciones fúngicas de la piel como la tiña y el pie de atleta. Además, sus propiedades antimicrobianas lo convierten en un ingrediente común en productos para el cuidado de la piel, cosméticos, pastas de dientes y productos para el cabello.
Precursor Químico Industrial
Uno de los usos más importantes del ácido benzoico en términos de volumen es como precursor para la síntesis de fenol. El fenol se produce mediante la descarboxilación oxidativa del ácido benzoico.
El fenol es una materia prima industrial masiva, utilizada en la producción de resinas fenólicas, plásticos como los policarbonatos y las resinas epoxi, detergentes, herbicidas y productos farmacéuticos como la aspirina. También es un precursor del caprolactama, que se utiliza para fabricar nailon.
Seguridad y Toxicología
Aunque el ácido benzoico y sus sales están aprobados como aditivos alimentarios y se consideran seguros en las concentraciones permitidas, surgió una preocupación en la década de 1990.
Se descubrió que, bajo ciertas condiciones, el ácido benzoico puede reaccionar con el ácido ascórbico (Vitamina C)en presencia de iones de metales de transición (como cobre (II) o hierro (III)) para formar trazas de benceno, un conocido carcinógeno. Esta reacción puede ocurrir en bebidas que contienen ambos aditivos.
Desde este descubrimiento, las agencias reguladoras y los fabricantes han monitoreado de cerca los niveles de benceno en las bebidas, y se ha encontrado que, si se detecta, está muy por debajo de los límites de seguridad establecidos (generalmente < 5 ppb).
Derivados Relevantes
Varios ésteres del ácido benzoico tienen propiedades y aplicaciones interesantes.
Benzoato de Metilo
Este éster, que se puede sintetizar mediante la esterificación de Fischer del ácido benzoico con metanol, tiene un agradable olor afrutado y especiado. Es emitido por las flores de plantas como el dragón y la petunia para atraer a insectos polinizadores como las abejas.
Curiosamente, también es el compuesto que detectan los perros rastreadores de la policía entrenados para encontrar cocaína. La cocaína clorhidrato se hidroliza lentamente en presencia de humedad, liberando el olor volátil del benzoato de metilo.
Benzoato de Bencilo
Este éster es mucho menos volátil que el de metilo (punto de ebullición ~320 °C), lo que lo convierte en un excelente fijador de perfumes, ayudando a que las fragancias duren más tiempo en la piel. También tiene aplicaciones médicas como acaricida para tratar la sarna y la pediculosis (piojos).
Como citar este artículo:
APA: (2026-04-07). Ácido Benzoico. Recuperado de https://quimicafacil.net/compuesto-de-la-semana/acido-benzoico/
ACS: . Ácido Benzoico. https://quimicafacil.net/compuesto-de-la-semana/acido-benzoico/. Fecha de consulta 2026-04-07.
IEEE: , "Ácido Benzoico," https://quimicafacil.net/compuesto-de-la-semana/acido-benzoico/, fecha de consulta 2026-04-07.
Vancouver: . Ácido Benzoico. [Internet]. 2026-04-07 [citado 2026-04-07]. Disponible en: https://quimicafacil.net/compuesto-de-la-semana/acido-benzoico/.
MLA: . "Ácido Benzoico." https://quimicafacil.net/compuesto-de-la-semana/acido-benzoico/. 2026-04-07. Web.
Si tiene alguna pregunta o sugerencia, escribe a administracion@quimicafacil.net, o visita Como citar quimicafacil.net