Tiempo de lectura estimado: 10 minutos
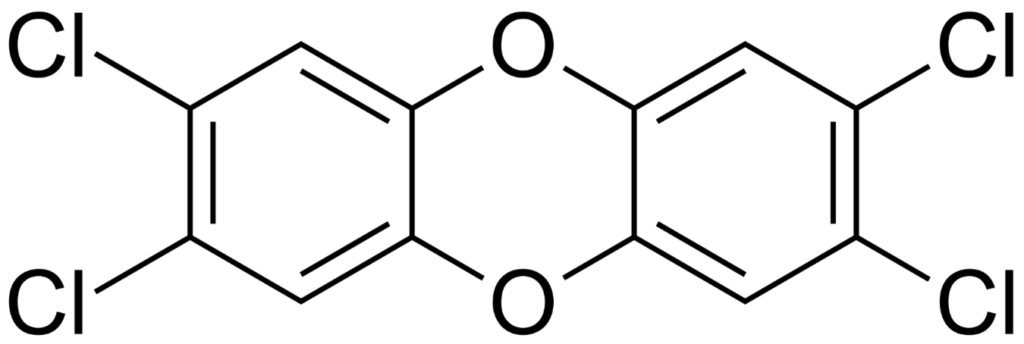
La dioxina, nombre abreviado de la 2,3,7,8-tetraclorodibenzo-para-dioxina (2,3,7,8-TCDD), se considera uno de los compuestos más peligrosos que contaminan nuestro entorno. Su estructura química está formada por dos anillos aromáticos unidos a través de un par de átomos de oxígeno.
Cuatro átomos de cloro, dos en cada anillo aromático, están unidos en las posiciones 2, 3, 7 y 8. Toda la molécula es plana y posee simetría D2h. Si tenemos en cuenta que se pueden unir hasta ocho átomos de cloro al esqueleto de la dibenzodioxina (DD), se pueden concebir 75 isómeros de DD sustituidos por cloro.
La dioxina está inextricablemente ligada a la contaminación ambiental por incineración de residuos y a su formación incidental en las plantas químicas dedicadas a la producción de pesticidas.
Estructura química de las dibenzo-1,4-dioxinas
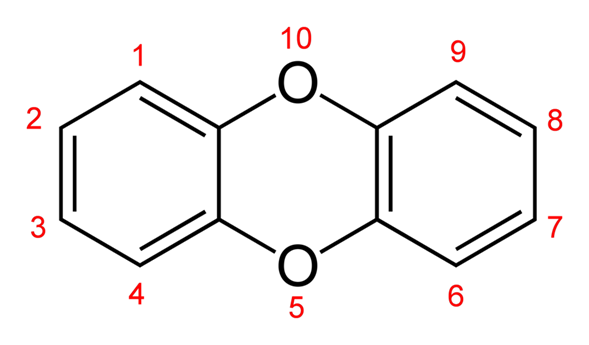
La estructura de la dibenzo-1,4-dioxina consiste en dos anillos de benceno unidos por dos puentes de oxígeno. Esto hace que el compuesto sea un diéter aromático. El nombre de dioxina se refiere formalmente al anillo central dioxigenado, que está estabilizado por los dos anillos bencénicos que lo flanquean.
En los PCDD, los átomos de cloro se unen a esta estructura en cualquiera de los 8 lugares diferentes de la molécula, en las posiciones 1-4 y 6-9. Existen 75 congéneres diferentes de PCDD (es decir, compuestos de dioxina relacionados).
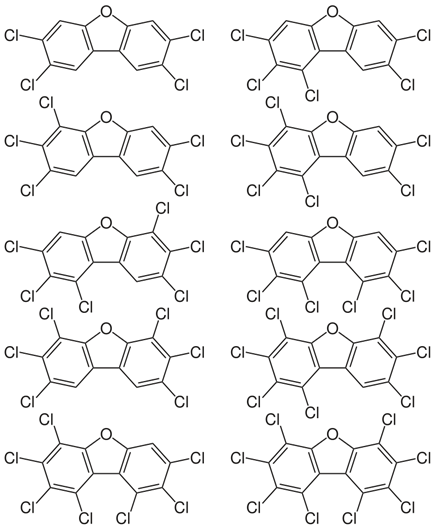
La toxicidad de los PCDD depende del número y la posición de los átomos de cloro. Se ha comprobado que los congéneres que tienen cloro en las posiciones 2, 3, 7 y 8 son significativamente tóxicos. De hecho, 7 congéneres tienen átomos de cloro en las posiciones pertinentes que fueron considerados tóxicos por el esquema de equivalentes tóxicos de la Organización Mundial de la Salud (EQT de la OMS).
Un poco de historia
Antes de la industrialización existían bajas concentraciones de dioxinas en la naturaleza como resultado de la combustión natural y de los procesos geológicos. Las dioxinas se produjeron por primera vez de forma no intencionada como subproductos a partir de 1848, cuando empezaron a funcionar las plantas de proceso de Leblanc en Alemania.
La primera síntesis intencionada de dibenzodioxina clorada fue en 1872. Hoy en día, las concentraciones de dioxinas se encuentran en todos los seres humanos, con niveles más altos comúnmente encontrados en las personas que viven en los países más industrializados. La dioxina más tóxica, la 2,3,7,8-tetraclorodibenzodioxina (TCDD), se dio a conocer como contaminante del Agente Naranja, un herbicida utilizado en la emergencia de Malasia y en la guerra de Vietnam.
Más tarde, se encontraron dioxinas en Times Beach, Missouri y Love Canal, Nueva York y en Seveso, Italia. Más recientemente, las dioxinas han sido noticia por el envenenamiento del presidente ucraniano Viktor Yushchenko en 2004, la crisis de la mozzarella de Nápoles, la crisis de la carne de cerdo irlandesa de 2008 y el incidente de los piensos alemanes de 2010.
Una catástrofe provocada por el hombre
La dioxina fue el actor principal de uno de los desastres más grandes de la historia de la industria química. A continuación, se ofrece un breve relato del incidente de Seveso, ocurrido hace más de cuarenta años en el norte de Italia y relatado con gran detalle por el profesor Paolo Mocarelli, médico y profesor universitario que ha dedicado muchos años de su vida a estudiar los efectos de la dioxina en la salud humana.
La mañana del 10 de julio (sábado) de 1976 fue una mañana corriente como cualquier otra. A las 12:37 una nube sale de una de las muchas chimeneas de ICMESA, una fábrica de productos químicos situada cerca del pequeño pueblo de Meda, no muy lejos de la ciudad de Seveso.
Al día siguiente, los alcaldes de Meda y Seveso son alertados por los representantes de ICMESA sobre la nube tóxica. Poco después, los ciudadanos se dan cuenta de que las hojas de los árboles se vuelven amarillas y los animales pequeños empiezan a morir. Más aterradoras aún son las quemaduras que aparecen en las caras de los niños.
Después de más de una semana del incidente, la gente sigue preguntándose qué está pasando. Se baraja la hipótesis de la presencia de dioxina en el ambiente, que posteriormente se confirmó el 20 de julio. ¿Cómo es posible que la dioxina se haya escapado de la planta química? ICMESA producía 2,4,5-triclorofenol (TCP), un compuesto que posee propiedades bactericidas y que se utiliza como pesticida. Su síntesis emplea el 1,2,4,5-tetracloro-benceno (TCB) como compuesto base:
Lo que sucedió dentro de la planta
La reacción exotérmica aumentó excesivamente la presión del recipiente que contenía los reactivos y, como consecuencia del mal funcionamiento de una válvula de seguridad, varios compuestos, entre los que se encontraban unos 30 Kg de TCDD, escaparon directamente a la atmósfera.
En los días siguientes al incidente, las autoridades tuvieron que estimar el alcance real de la catástrofe para emprender rápidamente los procedimientos necesarios de evacuación y asistencia médica, además de asegurar la zona contaminada. Los procedimientos de emergencia se basan siempre en datos técnicos y científicos, como la medición de la cantidad de TCDD en la sangre, las frutas, las verduras y el suelo.
Sin embargo, ésta fue la primera catástrofe medioambiental a gran escala relacionada con la contaminación por TCDD y en ese momento se disponía de poca o ninguna información. Como señala el profesor Mocarelli, «la ciencia admite su ignorancia dentro de su ámbito. Admitirla públicamente es más difícil”.
Efectos de la dioxina en el ambiente
Se organizaron varios comités y se llevó a cabo una gran actividad científica y técnica. Los efectos inmediatos de la TCDD en los seres humanos fueron (a) lesiones en la piel como resultado del contacto con los diversos compuestos presentes en la nube tóxica, y (b) cloracné, una afección cutánea similar al acné que resulta de la exposición a los hidrocarburos clorados.


El cloracné se manifiesta con la formación de pequeñas protuberancias, denominadas comedones, y quistes en las mejillas y detrás de las orejas. Los estudios estadísticos realizados durante varios años en mujeres embarazadas no mostraron un aumento significativo de las malformaciones, aunque la proporción de sexos al nacer parece estar sesgada hacia las mujeres. Además, también se ha observado un aumento del riesgo de tumores del sistema linfático. En 2003 se publicó un estudio toxicológico exhaustivo del incidente de Seveso.
Además de los aspectos médicos relacionados con el incidente, un problema importante que había que resolver en aquel momento era la limpieza de las zonas contaminadas cerca de Seveso y Meda. En un principio se sugirió la incineración y fue apoyada tanto por los científicos como por los políticos. Finalmente, bajo la presión de la opinión pública, las autoridades optaron por la escarificación del suelo y su eliminación en cuencas especialmente construidas.
Finalmente se creó un parque en estas cuencas y los ciudadanos pueden ahora estar orgullosos de la belleza y la resurrección de su tierra. Esta breve historia concluye con las reveladoras palabras del profesor Mocarelli: «Seveso nos enseña que debemos tener una perspectiva sobre nuestros límites, es decir, sobre los efectos que se producen en los sistemas naturales que se han construido a lo largo de miles o millones de años, efectos de nuestro comportamiento que crean cambios de gran alcance e incluso destrucción».
Toxicología
Se ha establecido que la TCDD se une al receptor de hidrocarburos de arilo (AHR) en los tejidos humanos. A partir de aquí, el complejo AHR-TCDD entra en el núcleo celular para interactuar con una secuencia específica de ADN. Se cree que el complejo actúa como un factor de transcripción de la familia alfa-beta-alfaque inicia una cascada de señalización que provoca los cambios tisulares observados (por ejemplo, el cloracné). La caracterización de la estructura tridimensional de la AHR (o de parte de ella) ayudará en gran medida a arrojar más luz sobre los mecanismos moleculares que subyacen a los efectos toxicológicos de la TCDD (y otros hidrocarburos clorados), así como a encontrar posibles remedios (fármacos, terapias, etc.) para el tratamiento de la intoxicación por dioxinas.
Estructura electrónica
La estructura electrónica de las moléculas surge de la física de los electrones y los núcleos. En el marco de la mecánica cuántica, la rama de la física dedicada al estudio de las partículas microscópicas, la ecuación de Schrödinger no relativista e independiente del tiempo (Hy=Ey) acoplada a la aproximación de Born-Oppenheimer (que establece que el movimiento del electrón puede desacoplarse del de los núcleos como resultado de sus diferentes masas) representa un buen punto de partida para modelar la estructura electrónica de las moléculas poliatómicas.
La figura siguiente muestra los gráficos de cuatro orbitales moleculares (MOs) de la TCDD cuyas energías (propias) son las soluciones numéricas de la ecuación de Schrödinger. Los MOs que abarcan los niveles HOMO (MO más ocupado) y LUMO (MO más desocupado) son los que interesan a los químicos investigadores, ya que están relacionados con propiedades importantes de la molécula, como su reactividad química.
En la parte superior izquierda, el nivel HOMO-1 que muestra dos pares de «labios» que surgen de la combinación de orbitales atómicos de tipo p del carbono que se encuentran perpendiculares al plano molecular. El nivel HOMO (arriba a la derecha) muestra la contribución de cuatro pares de orbitales atómicos de tipo p de los átomos de carbono. Tanto el HOMO como el HOMO-1 poseen un carácter antienlace con respecto a los enlaces C-O centrales.
En la parte inferior izquierda, el nivel LUMO que surge de los orbitales de tipo p de ocho átomos de carbono y posee carácter antienlace con respecto a los cuatro enlaces C-C. El nivel LUMO+1 (abajo a la derecha) muestra las contribuciones de los orbitales de tipo p de los átomos de cloro y tiene carácter antienlace con respecto a los cuatro enlaces C-Cl. Poblarlo con electrones (tras la reducción química o electroquímica de la TCDD) podría ayudar a lograr la decloración (parcial o total) de la TCDD.
Se han predicho varias propiedades fisicoquímicas a partir de los resultados de los cálculos de la estructura electrónica (química cuántica computacional). Por ejemplo, la afinidad electrónica adiabática (EA) de la TCDD corresponde a 0,259 eV según los cálculos realizados en el nivel teórico B3LYP/aug-cc-pvDZ. Además, los cálculos teóricos realizados sobre la molécula DD simple (con átomos de hidrógeno en lugar de átomos de cloro) predicen que la sustitución de ambos átomos de oxígeno por azufre y selenio produce moléculas fruncidas caracterizadas por altas barreras de inversión. Los resultados se han interpretado como una consecuencia directa de la estructura electrónica de estas moléculas.
Para más información Dioxins and their effects on human health
Como citar este artículo:
APA: (). Dioxina. Recuperado de https://quimicafacil.net/compuesto-de-la-semana/dioxina/
ACS: . Dioxina. https://quimicafacil.net/compuesto-de-la-semana/dioxina/. Fecha de consulta 2026-04-15.
IEEE: , "Dioxina," https://quimicafacil.net/compuesto-de-la-semana/dioxina/, fecha de consulta 2026-04-15.
Vancouver: . Dioxina. [Internet]. [citado 2026-04-15]. Disponible en: https://quimicafacil.net/compuesto-de-la-semana/dioxina/.
MLA: . "Dioxina." https://quimicafacil.net/compuesto-de-la-semana/dioxina/. . Web.
Si tiene alguna pregunta o sugerencia, escribe a administracion@quimicafacil.net, o visita Como citar quimicafacil.net