Estimated reading time: 15 minutos
Susumu Kitagawa, Richard Robson y Omar M. Yaghi son galardonados con el Premio Nobel de Química 2025 por el desarrollo de un nuevo tipo de arquitectura molecular. Las construcciones que crearon —estructuras metal-orgánicas (MOF)— contienen grandes cavidades en las que las moléculas pueden entrar y salir. Los investigadores las han utilizado para recolectar agua del aire del desierto, extraer contaminantes del agua, capturar dióxido de carbono y almacenar hidrógeno.
- Han creado nuevos espacios para la química
- Un simple modelo de madera de una molécula genera una idea
- Robson construye creaciones químicas innovadoras
- Robson despierta un espíritu pionero en la química
- El lema de Kitagawa: incluso las cosas inútiles pueden volverse útiles
- Kitagawa ve la singularidad de sus creaciones
- Una visita secreta a la biblioteca abre los ojos de Yaghi a la química
- Solo unos pocos gramos de la estructura de Yaghi pueden contener un campo de fútbol
- El grupo de investigación de Yaghi obtiene agua potable del aire del desierto
- Materiales MOF que capturan dióxido de carbono y gases tóxicos
Han creado nuevos espacios para la química
Un atractivo y muy espacioso apartamento tipo estudio, diseñado específicamente para tu vida como molécula de agua; así es como un agente inmobiliario podría describir una de todas las estructuras metal-orgánicas que los laboratorios de todo el mundo han desarrollado en las últimas décadas. Otras construcciones de este tipo están hechas a medida para capturar dióxido de carbono, separar PFAS del agua, administrar fármacos en el cuerpo o manejar gases extremadamente tóxicos. Algunas pueden atrapar el gas etileno de la fruta —para que maduren más lentamente— o encapsular enzimas que descomponen trazas de antibióticos en el medio ambiente.
En pocas palabras, las estructuras metal-orgánicas son excepcionalmente útiles. Susumu Kitagawa, Richard Robson y Omar Yaghi son galardonados con el Premio Nobel de Química 2025 porque crearon las primeras estructuras metal-orgánicas (MOF) y demostraron su potencial. Gracias al trabajo de los laureados, los químicos han podido diseñar decenas de miles de MOF diferentes, facilitando nuevas maravillas químicas.
Como sucede a menudo en las ciencias, la historia del Premio Nobel de Química 2025 comienza con alguien que pensó de manera innovadora. Esta vez, la inspiración surgió durante los preparativos de una clase de química clásica, en la que los estudiantes debían construir moléculas a partir de varillas y bolas.
Un simple modelo de madera de una molécula genera una idea
Era 1974. A Richard Robson, que enseñaba en la Universidad de Melbourne, Australia, se le había encargado convertir bolas de madera en modelos de átomos, para que los estudiantes pudieran crear estructuras moleculares. Para que esto funcionara, necesitaba que el taller de la universidad les hiciera agujeros, para que las varillas de madera —los enlaces químicos— pudieran unirse a los átomos. Sin embargo, los agujeros no podían colocarse al azar. Cada átomo —como el carbono, el nitrógeno o el cloro— forma enlaces químicos de una manera específica. Robson necesitaba marcar dónde debían perforarse los agujeros.
Cuando el taller le devolvió las bolas de madera, probó a construir algunas moléculas. Fue entonces cuando tuvo un momento de revelación: había una gran cantidad de información implícita en la posición de los agujeros. Las moléculas del modelo tenían automáticamente la forma y estructura correctas, debido a la ubicación de los agujeros.
Esta idea lo llevó a su siguiente planteamiento: ¿qué pasaría si utilizara las propiedades inherentes de los átomos para unir diferentes tipos de moléculas, en lugar de átomos individuales? ¿Podría diseñar nuevos tipos de construcciones moleculares?
Robson construye creaciones químicas innovadoras
Cada año, cuando Robson sacaba los modelos de madera para enseñar a nuevos estudiantes, se le ocurría la misma idea. Sin embargo, pasó más de una década antes de que decidiera ponerla a prueba. Comenzó con un modelo muy simple, inspirado en la estructura de un diamante, en la que cada átomo de carbono se une a otros cuatro, formando una pequeña pirámide (figura 2). El objetivo de Robson era construir una estructura similar, pero la suya se basaría en iones de cobre con carga positiva, Cu+. Al igual que el carbono, prefieren tener otros cuatro átomos a su alrededor.
Combinó los iones de cobre con una molécula que tiene cuatro brazos: 4′,4″,4″‘,4″»-tetracianotetrafenilmetano. No es necesario recordar su complicado nombre, pero es importante que la molécula al final de cada brazo tuviera un grupo químico, el nitrilo, que se sintiera atraído por los iones de cobre cargados positivamente (figura 2).
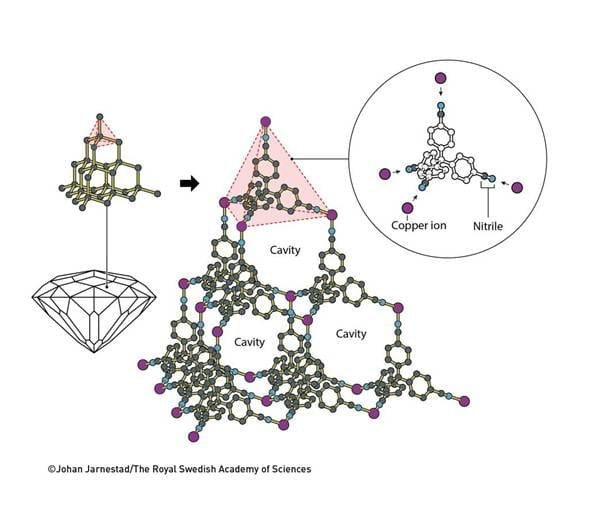
En aquel momento, la mayoría de los químicos habrían asumido que combinar iones de cobre con las moléculas de cuatro brazos daría como resultado un nido de pájaros de iones y moléculas. Pero las cosas salieron como Robson esperaba. Como había predicho, la atracción inherente de los iones y las moléculas entre sí fue importante, por lo que se organizaron en una gran construcción molecular. Al igual que los átomos de carbono en un diamante, formaron una estructura cristalina regular. Sin embargo, a diferencia del diamante —que es un material compacto— este cristal contenía un gran número de cavidades grandes (figura 2).
En 1989, Robson presentó su innovadora creación química en el Journal of the American Chemical Society. En su artículo, especula sobre el futuro y sugiere que esto podría ofrecer una nueva forma de construir materiales. Estos, escribe, podrían tener propiedades nunca vistas, potencialmente beneficiosas. Al final, resultó que había previsto el futuro.
Robson despierta un espíritu pionero en la química
Apenas un año después de la publicación de su trabajo pionero, Robson presentó varios tipos nuevos de construcciones moleculares con cavidades que estaban llenas de diversas sustancias. Usó una de ellas para intercambiar iones. Sumergió la construcción llena de iones en un fluido que contenía un tipo diferente de ion. El resultado fue que los iones intercambiaron sus lugares, demostrando que las sustancias podían entrar y salir de la construcción.
En sus experimentos, Robson demostró que el diseño racional se puede utilizar para construir cristales con interiores espaciosos optimizados para productos químicos específicos. Sugirió que esta nueva forma de construcción molecular —cuando se diseña correctamente— podría usarse para catalizar reacciones químicas, por ejemplo.
Sin embargo, las construcciones de Robson eran bastante frágiles y tendían a desmoronarse. Muchos químicos pensaron que eran inútiles, pero algunos pudieron ver que estaba en lo cierto y, para ellos, sus ideas sobre el futuro despertaron un espíritu pionero. Quienes sentarían una base estable para sus visiones fueron Susumu Kitagawa y Omar Yaghi. Entre 1992 y 2003 realizaron por separado una serie de descubrimientos revolucionarios. Comenzaremos en la década de 1990, con Kitagawa, que trabajaba en la Universidad de Kindai, Japón.
El lema de Kitagawa: incluso las cosas inútiles pueden volverse útiles
A lo largo de su carrera investigadora, Susumu Kitagawa ha seguido un principio importante: tratar de ver «la utilidad de lo inútil». Siendo un joven estudiante, leyó un libro del premio Nobel Hideki Yukawa. En él, Yukawa se refiere a un antiguo filósofo chino, Zhuangzi, quien dice que debemos cuestionar lo que creemos que es útil. Incluso si algo no aporta un beneficio inmediato, aún puede resultar valioso.
En consecuencia, cuando Kitagawa comenzó a investigar el potencial de crear estructuras moleculares porosas, no creía que debieran tener un propósito específico. Cuando presentó su primera construcción molecular en 1992, en realidad no fue particularmente útil: un material bidimensional con cavidades en las que las moléculas de acetona podían esconderse. Sin embargo, había resultado de una nueva forma de pensar sobre el arte de construir con moléculas. Al igual que Robson, utilizó iones de cobre como piedras angulares que se unían mediante moléculas más grandes.
Kitagawa quería seguir experimentando con esta nueva tecnología de construcción, pero cuando solicitó subvenciones, los financiadores de la investigación no creyeron que sus ambiciones tuvieran ningún sentido en particular. Los materiales que creaba eran inestables y no tenían ningún propósito, por lo que muchas de sus propuestas fueron rechazadas.
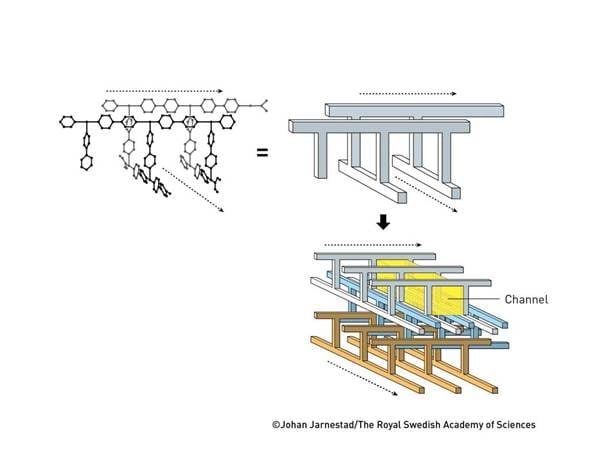
Sin embargo, no se rindió y en 1997 tuvo su primer gran avance. Usando iones de cobalto, níquel o zinc y una molécula llamada 4,4′-bipiridina, su grupo de investigación creó estructuras metal-orgánicas tridimensionales que estaban atravesadas por canales abiertos (figura 3). Cuando secaron uno de estos materiales —vaciándolo de agua—, era estable y los espacios incluso podían llenarse con gases. El material podía absorber y liberar metano, nitrógeno y oxígeno, sin cambiar de forma.
Kitagawa ve la singularidad de sus creaciones
Las construcciones de Kitagawa eran estables y tenían una función, pero los financiadores de la investigación aún no podían ver su encanto. Una razón era que los químicos ya tenían zeolitas, materiales estables y porosos, que podían construir a partir de dióxido de silicio. Estas pueden absorber gases, entonces, ¿por qué alguien desarrollaría un material similar que no funcionaba tan bien?
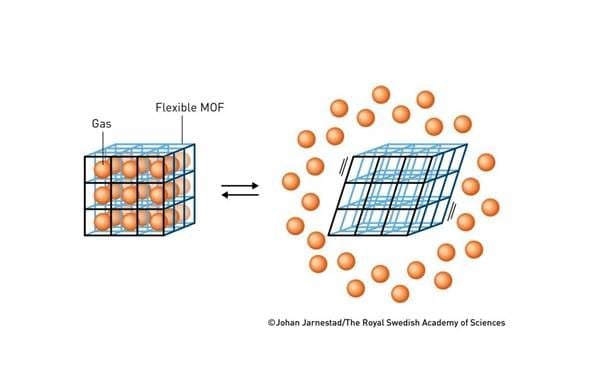
Susumu Kitagawa entendió que, si quería recibir alguna subvención importante, tenía que definir qué hacía únicas a las estructuras metal-orgánicas. Así que, en 1998, describió su visión en el Bulletin of the Chemical Society of Japan. Presentó varias ventajas de las MOF. Por ejemplo, pueden crearse a partir de muchos tipos de moléculas, por lo que existe un enorme potencial para integrar diferentes funciones. Además —y esto es importante— se dio cuenta de que las MOF pueden formar materiales blandos. A diferencia de las zeolitas, que suelen ser materiales duros, las MOF contienen bloques de construcción moleculares flexibles (figura 4) que pueden crear un material maleable. Después de esto, todo lo que tuvo que hacer fue poner sus ideas en práctica.
Kitagawa, junto con otros investigadores, comenzó a desarrollar MOF flexibles. Mientras ellos trabajan en esto, nos trasladaremos a los EE. UU., donde Omar Yaghi también estaba ocupado llevando la arquitectura molecular a nuevas alturas.
Una visita secreta a la biblioteca abre los ojos de Yaghi a la química
Estudiar química no fue una elección obvia para Omar Yaghi. Él y sus muchos hermanos se criaron en una sola habitación en Amán, Jordania, sin electricidad ni agua corriente. La escuela era un refugio de su vida, por lo demás desafiante. Un día, cuando tenía diez años, se coló en la biblioteca de la escuela, que solía estar cerrada, y escogió un libro al azar de la estantería. Al abrirlo, sus ojos se sintieron atraídos por imágenes ininteligibles pero cautivadoras: su primer encuentro con las estructuras moleculares.
A la edad de 15 años —y por orden estricta de su padre— Yaghi se mudó a los EE. UU. para estudiar. Se sintió atraído por la química y, finalmente, por el arte de diseñar nuevos materiales, pero encontró que la forma tradicional de construir nuevas moléculas era demasiado impredecible. Normalmente, los químicos combinan sustancias que deben reaccionar entre sí en un recipiente. Luego, para iniciar la reacción química, calientan el recipiente. La molécula deseada se forma, pero a menudo también va acompañada de una serie de subproductos contaminantes.
En 1992, cuando Yaghi comenzó su primer puesto como líder de grupo de investigación, en la Universidad Estatal de Arizona, quiso encontrar formas más controladas de crear materiales. Su objetivo era utilizar el diseño racional para conectar diferentes componentes químicos, como piezas de Lego, para hacer grandes cristales. Esto resultó ser un desafío, pero finalmente tuvieron éxito cuando el grupo de investigación comenzó a combinar iones metálicos con moléculas orgánicas.
En 1995, Yaghi publicó la estructura de dos materiales bidimensionales diferentes; estos eran como redes y se mantenían unidos por cobre o cobalto. El último podía albergar moléculas invitadas en sus espacios y, cuando estos estaban completamente ocupados, era tan estable que podía calentarse a 350°C sin colapsar. Yaghi describe este material en un artículo en Nature donde acuña el nombre de «estructura metal-orgánica» (metal-organic framework); este término ahora se usa para describir estructuras moleculares extendidas y ordenadas que potencialmente contienen cavidades, y están construidas a partir de metales y moléculas orgánicas (basadas en carbono).
Solo unos pocos gramos de la estructura de Yaghi pueden contener un campo de fútbol
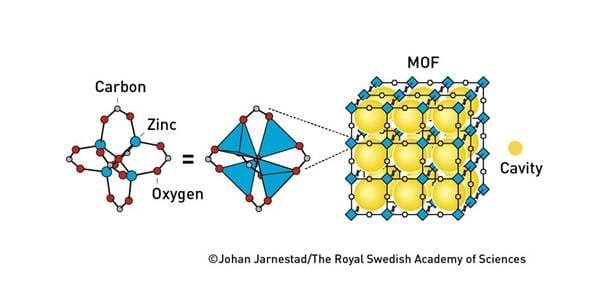
Yaghi estableció el siguiente hito en el desarrollo de las estructuras metal-orgánicas en 1999, cuando presentó MOF-5 al mundo. Este material se ha convertido en un clásico en el campo. Es una construcción molecular excepcionalmente espaciosa y estable. Incluso cuando está vacía, puede calentarse a 300°C sin colapsar. Sin embargo, lo que hizo que muchos investigadores levantaran las cejas fue el área enorme que se esconde dentro de los espacios cúbicos del material. Un par de gramos de MOF-5 albergan un área tan grande como un campo de fútbol, lo que significa que puede absorber mucho más gas que una zeolita (figura 5).
Hablando de las diferencias entre las zeolitas y las MOF, los investigadores tardaron solo unos años en lograr desarrollar MOF blandas. Uno de los que pudo presentar un material flexible fue el propio Susumu Kitagawa. Cuando su material se llenaba de agua o metano, cambiaba de forma, y cuando se vaciaba, volvía a su forma original. El material se comportaba de alguna manera como un pulmón que puede inhalar y exhalar gas, cambiante pero estable.
El grupo de investigación de Yaghi obtiene agua potable del aire del desierto
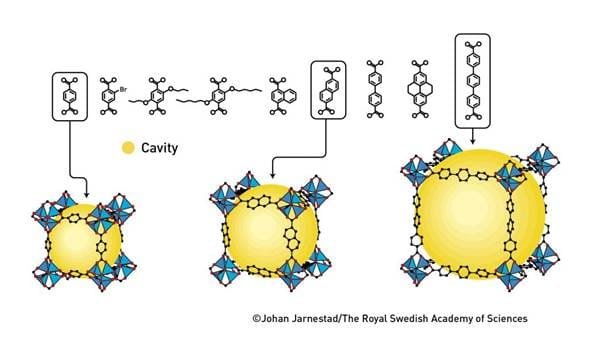
Omar Yaghi sentó los últimos ladrillos en la fundación de las estructuras metal-orgánicas en 2002 y 2003. En dos artículos, en Science y Nature, muestra que es posible modificar y cambiar las MOF de manera racional, dándoles diferentes propiedades. Una de las cosas que hizo fue producir 16 variantes de MOF-5, con cavidades que eran tanto más grandes como más pequeñas que las del material original (figura 6). Una variante podía almacenar enormes volúmenes de gas metano, que Yaghi sugirió que podría usarse en vehículos impulsados por GNR (gas natural renovable).
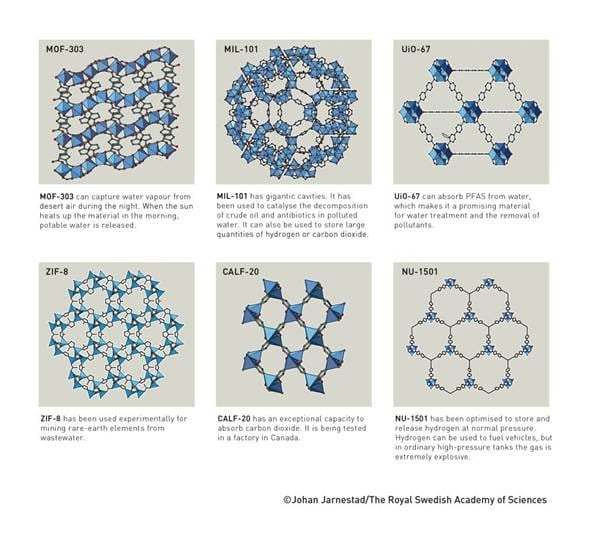
Posteriormente, las estructuras metal-orgánicas han conquistado el mundo. Los investigadores han desarrollado un kit molecular con una amplia gama de piezas diferentes que se pueden utilizar para crear nuevas MOF. Estas tienen diferentes formas y caracteres, lo que proporciona un potencial increíble para el diseño racional —o basado en IA— de MOF para diferentes propósitos. La Figura 7 proporciona ejemplos de cómo se pueden utilizar las MOF.
Por ejemplo, el grupo de investigación de Yaghi ha recolectado agua del aire del desierto de Arizona. Durante la noche, su material MOF capturó vapor de agua del aire. Cuando llegó el amanecer y el sol calentó el material, pudieron recolectar el agua.
Materiales MOF que capturan dióxido de carbono y gases tóxicos
Los investigadores han creado numerosas MOF diferentes y funcionales. Hasta ahora, en la mayoría de los casos, los materiales solo se han utilizado a pequeña escala. Para aprovechar los beneficios de los materiales MOF para la humanidad, muchas empresas están invirtiendo ahora en su producción en masa y comercialización. Algunas han tenido éxito. Por ejemplo, la industria electrónica ahora puede usar materiales MOF para contener algunos de los gases tóxicos necesarios para producir semiconductores. Otro MOF puede, en cambio, descomponer gases nocivos, incluidos algunos que pueden usarse como armas químicas. Numerosas empresas también están probando materiales que pueden capturar dióxido de carbono de fábricas y centrales eléctricas, para reducir las emisiones de gases de efecto invernadero.
MOF-303 puede capturar vapor de agua del aire del desierto durante la noche. Cuando el sol calienta el material por la mañana, se libera agua potable.
MIL-101 tiene cavidades gigantescas. Se ha utilizado para catalizar la descomposición de petróleo crudo y antibióticos en agua contaminada. También se puede utilizar para almacenar grandes cantidades de hidrógeno o dióxido de carbono.
UiO-67 puede absorber PFAS del agua, lo que lo convierte en un material prometedor para el tratamiento del agua y la eliminación de contaminantes.
ZIF-8 se ha utilizado experimentalmente para la extracción de elementos de tierras raras de aguas residuales.
CALF-20 tiene una capacidad excepcional para absorber dióxido de carbono. Se está probando en una fábrica en Canadá.
NU-1501 ha sido optimizado para almacenar y liberar hidrógeno a presión normal. El hidrógeno se puede utilizar para alimentar vehículos, pero en tanques ordinarios de alta presión el gas es extremadamente explosivo.
Algunos investigadores creen que las estructuras metal-orgánicas tienen un potencial tan enorme que serán el material del siglo XXI. El tiempo lo dirá, pero a través del desarrollo de las estructuras metal-orgánicas, Susumu Kitagawa, Richard Robson y Omar Yaghi han brindado a los químicos nuevas oportunidades para resolver algunos de los desafíos que enfrentamos. De este modo, han traído —como dice el testamento de Alfred Nobel— el mayor beneficio para la humanidad.
Texto traducido y adaptado por quimicafacil.net a partir de su fuente original que está disponible acá They have created new rooms for chemistry
Como citar este artículo:
APA: (2025-10-08). Premio Nobel de Química 2025. Recuperado de https://quimicafacil.net/premios-nobel/premio-nobel-de-quimica-2025/
ACS: . Premio Nobel de Química 2025. https://quimicafacil.net/premios-nobel/premio-nobel-de-quimica-2025/. Fecha de consulta 2026-02-27.
IEEE: , "Premio Nobel de Química 2025," https://quimicafacil.net/premios-nobel/premio-nobel-de-quimica-2025/, fecha de consulta 2026-02-27.
Vancouver: . Premio Nobel de Química 2025. [Internet]. 2025-10-08 [citado 2026-02-27]. Disponible en: https://quimicafacil.net/premios-nobel/premio-nobel-de-quimica-2025/.
MLA: . "Premio Nobel de Química 2025." https://quimicafacil.net/premios-nobel/premio-nobel-de-quimica-2025/. 2025-10-08. Web.
Si tiene alguna pregunta o sugerencia, escribe a administracion@quimicafacil.net, o visita Como citar quimicafacil.net