Estimated reading time: 6 minutos
La reacción de Cannizzaro es un método fundamental en la química orgánica para la transformación de aldehídos que no poseen hidrógenos en posición alfa.
En esta reacción, dos moléculas de un aldehído reaccionan en presencia de una base fuerte, como el hidróxido de sodio (NaOH), para producir un alcohol primario y la sal de un ácido carboxílico mediante un proceso de auto-oxidación-reducción.
El objetivo de esta práctica es sintetizar ácido benzoico a partir de benzaldehído. El ácido benzoico es un sólido cristalino que funde a 121°C y es ampliamente utilizado como conservante de alimentos por sus propiedades antisépticas.
Marco Teórico
Cuando un aldehído que carece de hidrógenos en el carbono adyacente al grupo carbonilo (carbono alfa) se expone a un álcali concentrado, sufre una desproporción o dismutación. Una molécula del aldehído se reduce para formar un alcohol, mientras que la otra molécula se oxida para formar una sal de ácido carboxílico.
La reacción general para el benzaldehído es la siguiente:
El mecanismo de la reacción ocurre en dos pasos principales:
1. Adición Nucleofílica: El ion hidróxido ($OH^{-}$) ataca al carbono carbonílico del aldehído, que es electrófilo, formando un intermediario tetraédrico.
2. Transferencia de Hidruro: El intermediario tetraédrico transfiere un ion hidruro ($H^{-}$) a una segunda molécula de aldehído. Esta transferencia es el paso determinante de la velocidad y es facilitada por la carga negativa del intermediario.El resultado es la formación de un anión carboxilato y una molécula de alcohol.
Finalmente, la sal de ácido carboxílico (benzoato de sodio en este caso) se protona en un paso posterior con un ácido para obtener el ácido benzoico final.
Materiales
- Mechero Bunsen
- Vaso de precipitado de 100 ml
- Pera de decantación (o embudo de separación)
- Soporte universal y pinza de aro
- Probeta de 10 ml y 50 ml
- 6 tubos de ensayo
- Varilla de agitación
- Papel filtro
Reactivos
- Benzaldehído ($C_{7}H_{6}O$), 5 ml
- Hidróxido de sodio (NaOH) en pastillas
- Agua destilada ($H_{2}O$), 50 ml
- Éter de petróleo
- Ácido clorhídrico ($HCl$) concentrado o ácido sulfúrico ($H_{2}SO_{4}$)
- Ácido acético ($CH_{3}COOH$)
- Dicromato de potasio ($K_{2}Cr_{2}O_{7}$)
- Cloruro férrico ($FeCl_{3}$)
Procedimiento – Reacción de Cannizzaro
1. Preparación de la Solución de NaOH: En un vaso de precipitado, disolver 2.5 g de hidróxido de sodio en 25 ml de agua destilada caliente. Agitar constantemente hasta la disolución completa.
2. Reacción de Cannizzaro: Agregar 5 ml de benzaldehído a la solución de NaOH. Agitar la mezcla vigorosamente durante 10-15 minutos hasta que se forme una emulsión espesa.
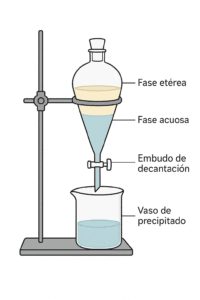
3. Extracción de Productos: Verter la mezcla de reacción en una pera de decantación. Añadir 20 ml de éter de petróleo, tapar y agitar cuidadosamente, liberando la presión interna periódicamente.
4. Separación de Fases: Dejar reposar la mezcla hasta que se separen claramente dos fases. La fase superior (eterea) contendrá el alcohol bencílico, mientras que la fase inferior (acuosa) contendrá el benzoato de sodio. Recoger la fase acuosa inferior en un vaso de precipitado limpio.
5. Identificación del Alcohol Bencílico (Opcional): A una pequeña alícuota de la fase etérea, agregar una solución ácida de dicromato de potasio. Un cambio de color de naranja a verdeazulado indica la oxidación del alcohol bencílico a benzaldehído, confirmando su presencia.
6. Precipitación del Ácido Benzoico: Enfriar la fase acuosa recogida en un baño de hielo. Con agitación constante, agregar lentamente ácido clorhídrico concentrado hasta que la solución sea ácida (verificar con papel pH). Se observará la formación de un precipitado blanco de ácido benzoico.
7. Aislamiento y Purificación: Filtrar el precipitado de ácido benzoico usando un embudo Büchner y papel filtro. Lavar el sólido con una pequeña cantidad de agua helada para eliminar impurezas. Dejar secar el producto al aire.
Después del Experimento
Cálculos
1. Reactivo Limitante: Determinar el reactivo limitante de la reacción. La estequiometría de la reacción es de 2 moles de benzaldehído por cada mol de ácido benzoico producido.
2. Rendimiento Teórico: Calcular la masa máxima de ácido benzoico que podría obtenerse a partir de la cantidad inicial de benzaldehído.
* Volumen de benzaldehído:
* Densidad del benzaldehído:
* Masa molar del benzaldehído
* Masa molar del ácido benzoico
Masa de benzaldehído:
Moles de benzaldehído:
Moles de ácido benzoico (según estequiometría 2:1):
Rendimiento teórico ($m_{teorico}$):
3. Rendimiento Porcentual: Pesar el ácido benzoico seco obtenido (rendimiento experimental, $m_{exp}$) y calcular el rendimiento porcentual de la reacción.
Cuestionario
1. ¿Por qué el benzaldehído es susceptible a la reacción de Cannizzaro, mientras que el acetaldehído ($CH_{3}CHO$) no lo es en las mismas condiciones?
2. ¿Cuál es el propósito de realizar la extracción con éter de petróleo? ¿En qué propiedad física se basa esta separación?
3. Explique por qué la reacción de Cannizzaro es considerada una reacción de desproporción (o dismutación). Indique qué molécula se oxida y cuál se reduce.
4. ¿Qué es la «reacción de Cannizzaro cruzada»? Proporcione un ejemplo.
5. ¿Por qué es necesario acidificar la fase acuosa para obtener el ácido benzoico? Escriba la reacción química de este paso.
Recomendaciones de Seguridad
* Hidróxido de Sodio (NaOH): Es un reactivo altamente corrosivo y puede causar quemaduras graves en la piel y los ojos. Manipular con guantes y gafas de seguridad.
* Benzaldehído: Es un compuesto irritante y nocivo por ingestión. Evitar el contacto con la piel y los ojos.
* Éter de Petróleo: Es extremadamente inflamable y volátil. Trabajar siempre dentro de una campana de extracción de gases y lejos de cualquier fuente de ignición, como el mechero Bunsen.
* Ácidos (HCl, $H_{2}SO_{4}$): Son corrosivos. Manipular con precaución, utilizando guantes y gafas de seguridad. Añadir siempre el ácido al agua, y nunca al revés.
* Equipo de Protección Personal (EPP): Es obligatorio el uso de bata de laboratorio, gafas de seguridad y guantes en todo momento durante la práctica.
Como citar este artículo:
APA: (2026-01-28). Síntesis de Ácido Benzoico – Reacción de Cannizzaro. Recuperado de https://quimicafacil.net/manual-de-laboratorio/sintesis-de-acido-benzoico-reaccion-de-cannizzaro/
ACS: . Síntesis de Ácido Benzoico – Reacción de Cannizzaro. https://quimicafacil.net/manual-de-laboratorio/sintesis-de-acido-benzoico-reaccion-de-cannizzaro/. Fecha de consulta 2026-03-30.
IEEE: , "Síntesis de Ácido Benzoico – Reacción de Cannizzaro," https://quimicafacil.net/manual-de-laboratorio/sintesis-de-acido-benzoico-reaccion-de-cannizzaro/, fecha de consulta 2026-03-30.
Vancouver: . Síntesis de Ácido Benzoico – Reacción de Cannizzaro. [Internet]. 2026-01-28 [citado 2026-03-30]. Disponible en: https://quimicafacil.net/manual-de-laboratorio/sintesis-de-acido-benzoico-reaccion-de-cannizzaro/.
MLA: . "Síntesis de Ácido Benzoico – Reacción de Cannizzaro." https://quimicafacil.net/manual-de-laboratorio/sintesis-de-acido-benzoico-reaccion-de-cannizzaro/. 2026-01-28. Web.
Si tiene alguna pregunta o sugerencia, escribe a administracion@quimicafacil.net, o visita Como citar quimicafacil.net